Clear Sky Science · ru
Клональное расширение цитотоксических CD8⁺ Т‑клеток при ARIA, связанной с лечением ликанемабом
Почему это важно для людей с болезнью Альцгеймера
Ликанемаб — одно из первых средств, способных удалять амилоид из мозга и умеренно замедлять утрату памяти при болезни Альцгеймера. Однако у части пациентов на этой терапии развивается отёк мозга или мелкие кровоизлияния, изменения, видимые на МРТ и объединяемые термином amyloid‑related imaging abnormalities (ARIA). В этом исследовании поставлен ключевой для пациентов и их семей вопрос: что происходит в иммунной системе при появлении ARIA и может ли простой анализ крови в будущем помочь предсказать, кто находится в наибольшей группе риска?
Надежда и риск нового лечения болезни Альцгеймера
Ликанемаб — это антитело, вводимое инфузионно, нацеленное на скопления белка амилоид‑β, характерного для болезни Альцгеймера. Помогая организму удалять амилоид, оно может умеренно замедлять когнитивный спад. Но этот эффект сопряжён с проблемой безопасности: у некоторых людей развивается ARIA, которое может включать очаги отёка мозга или точечные кровоизлияния. Эти побочные явления требуют частого мониторинга МРТ и ограничивают круг пациентов, которым можно назначать препарат. Не все одинаково уязвимы — носители варианта гена APOE4 имеют более высокий риск — но одной генетики недостаточно, чтобы объяснить появление ARIA, особенно в ранние сроки после начала лечения. Поскольку ликанемаб вводится через кровь, авторы предположили, что внимательное изучение иммунных клеток в крови может выявить ранние предупредительные признаки или механизмы, связывающие терапию с сосудистым повреждением в мозге. 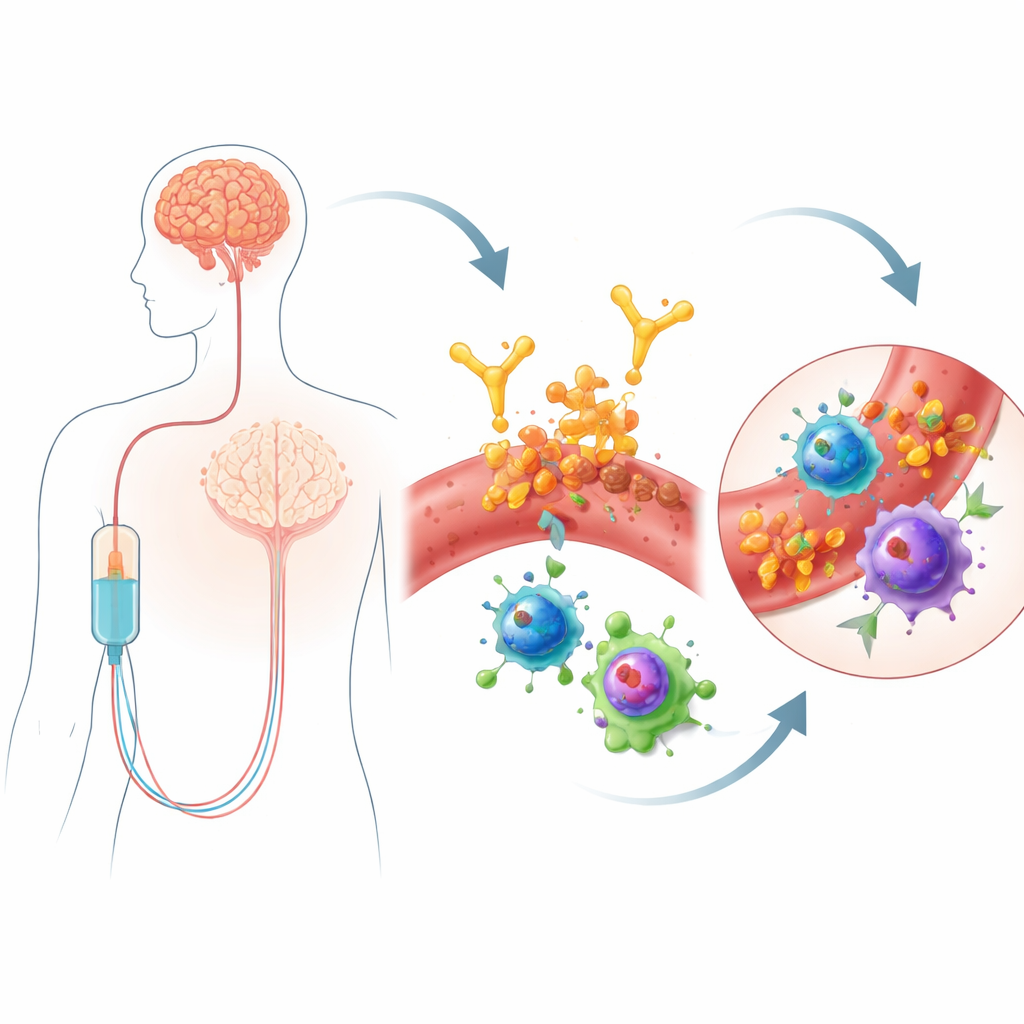
Отслеживание иммунных клеток у пациентов с ARIA и без него
Исследователи изучили шесть людей с болезнью Альцгеймера, получавших ликанемаб в региональной клинике памяти. У троих развились разные формы ARIA, у троих сопоставимых пациентов (по возрасту, полу, генотипу APOE и числу инфузий) изменений не наблюдалось. Кровь брали непосредственно перед инфузиями, и команда применила интенсивный «мультиомный» подход: секвенирование РНК по одной клетке, чтобы определить, какие гены активированы в тысячах отдельных иммунных клеток; антителозависимые метки для типирования клеток; секвенирование Т‑клеточных рецепторов для отслеживания клонов; и таргетный метаболомный анализ сотен малых молекул, участвующих в метаболизме. Это позволило не только установить, какие типы клеток присутствуют, но и оценить их активность, используемое топливо и расширение конкретных семейств Т‑клеток в ответ на некий триггер.
Расширение вооружённых киллерных Т‑клеток
У пациентов, у которых развилась ARIA, обнаружилась чёткая закономерность. По сравнению с контрольной группой у них была большая доля CD8 «киллерных» Т‑клеток и меньше CD4 помощников. В пуле CD8 выделялись две подгруппы: эффекторные клетки памяти и терминально дифференцированная форма, известная как TEMRA. Эти TEMRA‑клетки похожи на бывалых солдат — высокоспециализированные в атаке, с мощным аппаратом для уничтожения целей. У пациентов с ARIA TEMRA‑клеток было больше, они демонстрировали клональное расширение (то есть определённые семьи Т‑клеток размножались) и экспрессировали программы генов, связанные с цитотоксичностью, миграцией через сосуды и признаками хронической стимуляции. Подобные состояния Т‑клеток наблюдали при старении, хронических инфекциях, рассеянном склерозе и в спинномозговой жидкости людей с болезнью Альцгеймера, где они могут накапливаться рядом с сосудами и поверхностью мозга.
Перепрофилирование метаболизма и взаимодействие с другими иммунными клетками
Команда также обнаружила, что эти CD8 эффекторные клетки перепрограммировали свой метаболизм. Вместо опоры в основном на эффективное производство энергии в митохондриях они переключились на гликолиз — более быстрый, но менее эффективный путь генерации энергии, поддерживающий кратковременную интенсивную активность. Измерения метаболитов в клетках крови подтвердили это: уровни лактата и пировиноградной кислоты были повышены, тогда как ключевые компоненты цикла Кребса снижены — характерный паттерн для воспалительных иммунных клеток. Моноциты, другой тип лейкоцитов, показали комплементарные изменения: у пациентов с ARIA они усиливали экспрессию генов, ответственных за презентацию антигенов, адгезию и выработку хемокинов — химических сигналов, привлекающих Т‑клетки. Вычислительное моделирование пар лиганд‑рецептор предположило, что моноциты посылают более сильные активирующие и адресующие сигналы CD8 эффекторным клеткам, создавая среду, благоприятную для взаимодействия киллерных клеток со стенкой сосудов.
«Адресные коды», направляющие Т‑клетки к сосудам мозга
Поскольку в этом исследовании анализировали лишь кровь, авторы обратились к независимому набору данных с секвенированием по одной клетке из мозга пациентов, леченных ликанемабом, чтобы выяснить, связаны ли те же Т‑клеточные программы с сосудистыми нишами в мозге. При наложении их подмножеств CD8 на карту мозга TEMRA и эффекторные клетки памяти из пациентов с ARIA показали транскрипционные «адресные коды» — комбинации молекул адгезии и хемокиновых рецепторов, совпадающие с эндотелиальными (сосудистыми) клетками в поражённом мозге. Эти сигнатуры указывают на то, что расширенные киллерные Т‑клетки не только сильно вооружены и метаболически активны, но и запрограммированы на гоминг к стрессированным сосудам мозга и взаимодействие с ними в местах удаления амилоида. 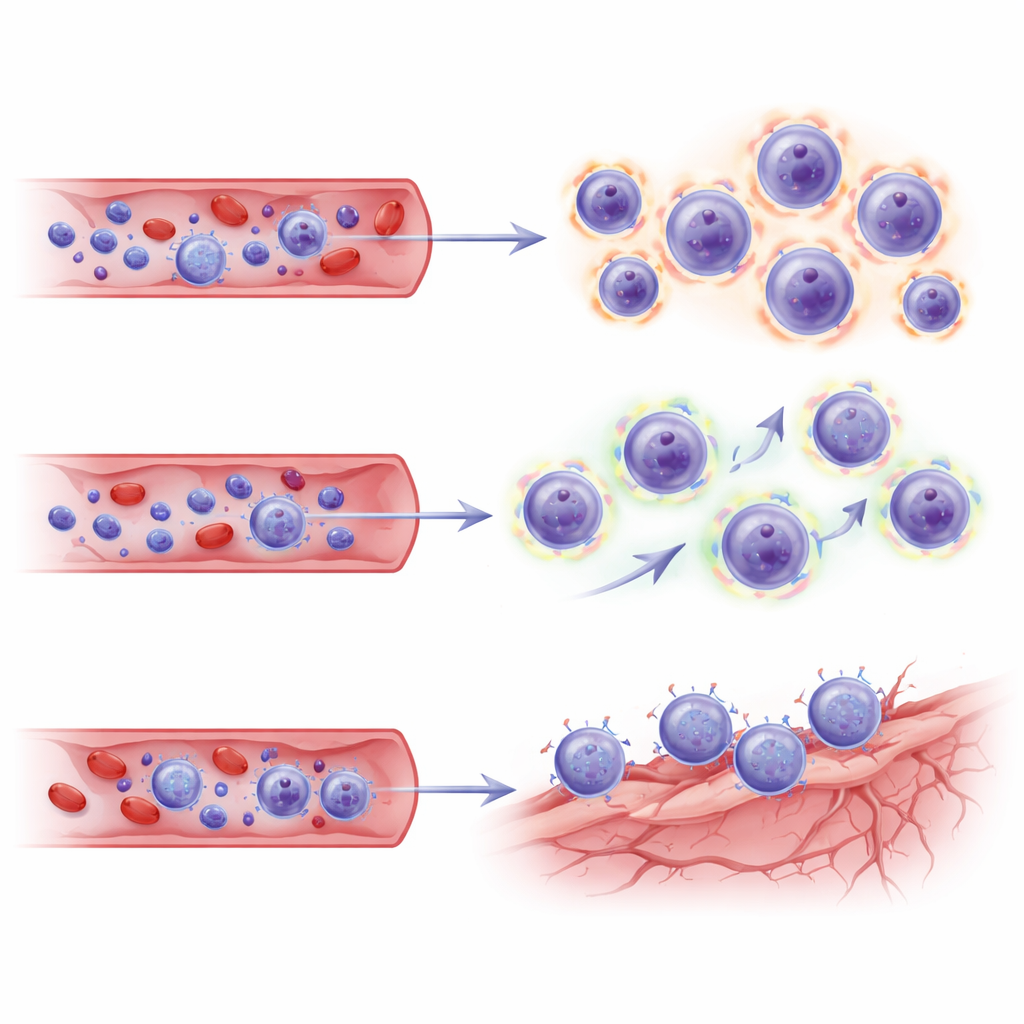
Что это может означать для пациентов и дальнейшей помощи
В целом это небольшое, но детализированное исследование представляет ARIA как явление, выходящее за рамки пассивного побочного эффекта удаления амилоида. Скорее всего, оно связано с координированным иммунным ответом в крови: расширением и метаболической активацией специфических клонов киллерных Т‑клеток, усилением сигналов со стороны моноцитов и молекулярными признаками, облегчающими взаимодействие с сосудами мозга. Работа не доказывает, что эти клетки являются непосредственной причиной ARIA — иммунные изменения могут быть реакцией на сосудистое повреждение, а не его источником — но она предлагает проверяемые гипотезы и план по созданию биомаркеров в крови. В будущем измерение числа и метаболического состояния CD8 TEMRA‑клеток вместе с ключевыми сигнальными молекулами может помочь выявлять пациентов с наивысшим риском ARIA, корректировать графики наблюдения или даже вдохновить целевые стратегии временной модуляции иммунного ответа, сохраняя при этом пользу от терапий, удаляющих амилоид.
Цитирование: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Ключевые слова: Болезнь Альцгеймера, ликанемаб, клетки иммунной системы, сосуды мозга, побочные эффекты лечения