Clear Sky Science · ru
Белки TMEM63 действуют как механически активируемые скремблазы липидов, модифицируемые холестерином, и способствуют механической стойкости мембраны
Как клетки сохраняют целостность при физическом стрессе
Клетки нашего организма постоянно подвергаются сжатию, растяжению и толчкам — будь то в бьющемся сердце, работающих мышцах или опухолях, проталкивающихся через ткань. В этом исследовании показано, как семейство мембранных белков, называемое OSCA/TMEM63, помогает клеткам переживать такие сильные механические воздействия за счёт перераспределения жиров в их наружной оболочке. Понимание этой встроенной амортизирующей системы может открыть новые пути в изучении нарушений слуха, миелина нервов и даже распространения рака.
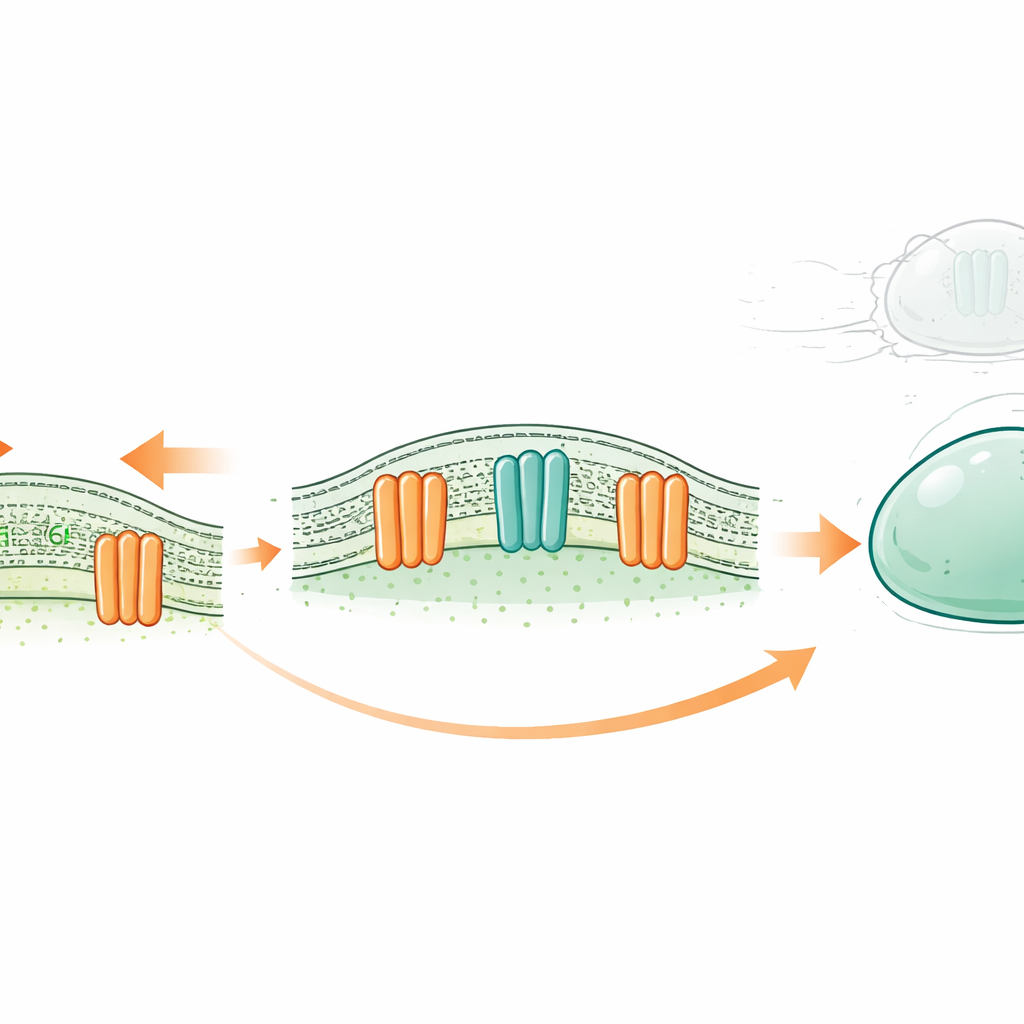
Новый тип клеточного амортизатора
Каждая клетка окружена тонкой маслянистой мембраной, состоящей из двух слоёв молекул, подобных жирам, — липидов. Традиционно некоторые мембранные белки считали только ионными каналами — крошечными клапанами, которые пропускают заряженные частицы при воздействии стимулов, таких как растяжение. Семейство OSCA/TMEM63, встречающееся от растений до человека, известно тем, что открывается в ответ на напряжение мембраны. Ранее полученные структурные данные намекали, что, в отличие от классических ионных каналов, их поры частично выстланы самими липидами. Это породило провокационную гипотезу: могут ли эти каналы также действовать как «скремблазы», перелистывая липиды между внутренним и внешним слоями мембраны, когда клетка испытывает механическое воздействие?
Наблюдение за перелистыванием липидов через мембрану
Чтобы проверить эту идею, авторы объединили компьютерное моделирование с редукционистскими лабораторными системами, собранными из очищенных компонентов. В моделях открытые варианты нескольких белков OSCA и TMEM63 встраивали в модельные мембраны. Липидные молекулы спонтанно перемещались через желобок в этих белках с одной стороны бимолекулярного слоя на другую, образуя «пояс», связывающий оба листка и одновременно оставляющий заполненный водой путь для ионов. Параллельно в экспериментах команда создавала гигантские искусственные «пузыри» (везикулы), содержащие флуоресцентные липиды и заданные белки. Когда внешний агент тушил флуоресценцию на наружной поверхности, любое дальнейшее снижение сигнала можно было объяснить только перелистыванием липидов из внутреннего слоя наружу. Везикулы с OSCA1.1, OSCA1.2, OSCA2.2 или TMEM63A/B демонстрировали такое дополнительное падение флуоресценции, указывающее на активное перемешивание, тогда как контрольные каналы, не способные перемешивать липиды, этого не показывали.
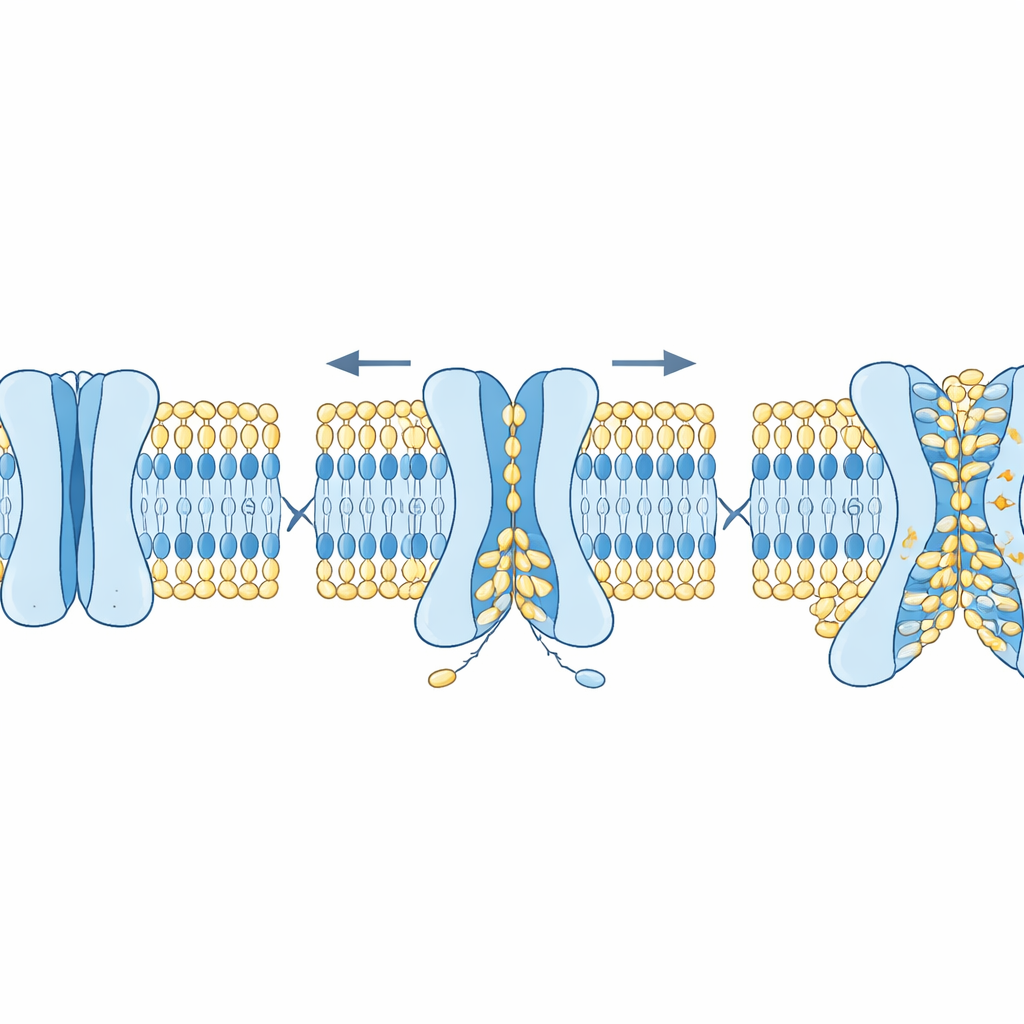
Как структура и холестерин настраивают процесс
Затем исследователи изучили, какие особенности TMEM63 контролируют это двойное поведение. С помощью AlphaFold2 они сгенерировали множество правдоподобных конфигураций белков TMEM63 человека, от закрытых до всё более открытых. Моделирование показало, что несколько объёмных аминокислот действуют как «узкие места» в желобке. Одна из остатков в основном ограничивает поток ионов, тогда как другие блокируют движение липидов. Мутация, ослабляющая ионное «узкое место», увеличивала электрическую проводимость, почти не влияя на перемешивание липидов, тогда как мутация «врат» для липидов облегчала их перелистывание и даже приводила к появлению на поверхности клетки «сигналов съедания» без дополнительного стимула. Ещё одним ключевым регулятором оказался холестерин — жёсткий компонент мембран. Добавление холестерина в модельные мембраны заметно замедляло перемешивание липидов и стабилизировало закрытое состояние TMEM63A как в моделях, так и в данных крио-электронной микроскопии, где холестерин располагался в специфических сайтах на белке.
Механическая сила как выключатель
Если холестерин обычно сдерживает перемешивание в клетках, то что включает его в нужный момент? Команда использовала кольцевые сахарные молекулы — циклодекстрины, чтобы выборочно удалять липиды из мембран и таким образом увеличивать напряжение без удаления холестерина. В везикулах размером с клетки добавление циклодекстрина активировало перемешивание липидов TMEM63A только при наличии белка, доказывая, что одной механической нагрузки достаточно, чтобы вызвать перелистывание. Похожие подходы в живых клетках показали, что мягкое удаление холестерина само по себе недостаточно; требовалось последующее механическое испытание, чтобы наблюдать сильное перемешивание. Когда клетки, экспрессирующие TMEM63A, многократно растягивали, они быстро выставляли определённые липиды на наружную поверхность — признак скремблинга, тогда как клетки без этих белков демонстрировали гораздо меньшие изменения.
Защита клеток от разрыва
Кроме перелистывания липидов, механически активируемый скремблинг изменял физическое поведение мембран при экстремальной нагрузке. В искусственных везикулах, подвергнутых сильной нагрузке, те, у которых не было скремблаз, склонны были разрываться, тогда как везикулы с TMEM63A или известной скремблазой сжимались, образовывали тонкие трубочки и в основном оставались целыми. В линии клеток человеческой опухоли мозга, которая натурально экспрессирует TMEM63A и TMEM63B, снижение уровня любого из этих белков делало клетки более склонными к разрыву при сильном механическом воздействии. В совокупности эти данные поддерживают модель, где белки OSCA/TMEM63 действуют как клапаны, которые открываются под напряжением и временно размывают обычное различие между внутренней и внешней поверхностями мембраны. Позволяя липидам быстро перераспределяться, они помогают уравновешивать напряжения и предотвращают катастрофические разрывы.
Что это значит для здоровья и болезней
Говоря просто, эта работа показывает, что некоторые чувствительные к растяжению каналы делают больше, чем проводят электрические сигналы: они также реорганизуют «кожу» клетки, помогая ей выживать при сжатии. Белки TMEM63 выступают как механически активируемые скремблазы липидов, чья активность тонко настраивается составом мембраны, особенно холестерином. Этот механизм механической стойкости может быть важен в тех местах, где клетки подвергаются большим силам — от изоляции нервных волокон и слуховых клеток до раковых клеток, перемещающихся в плотной ткани. Понимание и, в перспективе, целенаправленная модуляция этой двойной функции ионного канала и скремблазы могут открыть новые пути для защиты уязвимых тканей или, наоборот, для повышения уязвимости трудноустранимых раковых клеток.
Цитирование: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Ключевые слова: механочувствительные ионные каналы, перемешивание липидов, механика клеточной мембраны, регуляция холестерина, белки TMEM63 / OSCA