Clear Sky Science · ru
Нейротоксичный криптический пептид, возникающий вследствие криптического сплайсинга PKN1, зависящего от TDP-43
Скрытые угрозы внутри клеток мозга
Во многих заболеваниях мозга, включая боковой амиотрофический склероз (БАС) и болезнь Альцгеймера, наблюдаются скопления белка TDP-43. Ученые знают, что при нарушении функции этого белка нейроны теряют важные сообщения и в конечном итоге погибают. В этом исследовании показан более неожиданный поворот: потеря функции TDP-43 также может привести к тому, что клетки мозга начнут синтезировать ранее неизвестный токсичный мини‑белок, который в свою очередь повреждает цепи, ответственные за память. Понимание роли этого скрытого участника может открыть новые пути для диагностики и лечения разрушительных деменций.
Как клеточный корректировщик следит за порядком в РНК
Внутри нейронов TDP-43 действует как корректировщик для РНК — промежуточных сообщений между ДНК и белками. Он связывается со специфическими короткими последовательностями и блокирует вставку лишних «фрагментов» в эти сообщения. Когда TDP-43 теряется или смещается из нормального местоположения, как при БАС и во многих случаях Альцгеймера, эти лишние фрагменты — так называемые криптические экзоны — могут проникнуть в РНК. До сих пор большинство известных криптических экзонов просто вызывали потерю нормального белка, делая сообщение нестабильным и быстро разрушаемым. Оставался неясным вопрос, могут ли такие события также порождать новые, вредные белки.
Криптический сплайс создает токсичный фрагмент
Авторы сосредоточились на гене PKN1, который помогает поддерживать внутренний каркас и передачу сигналов в нейронах. В моделях клеток с пониженным уровнем TDP-43 они обнаружили ранее нераспознанный криптический экзон, названный PKN1‑5a1, вставленный между двумя нормальными участками РНК PKN1. Эта вставка вводит ранний стоп‑сигнал, давая укороченную РНК. Поразительно, часть этого дефектного сообщения уходит от контроля качества клетки и транслируется в стабильный фрагмент белка PKN1, содержащий только первые 207 аминокислот. Команда назвала этот укороченный продукт PKN207. Они показали, что TDP-43 обычно предотвращает эту ошибку, связываясь с несколькими UG‑богатыми регионами, окружающими криптический экзон; при утрате такого связывания экзон включается, и возникает PKN207.
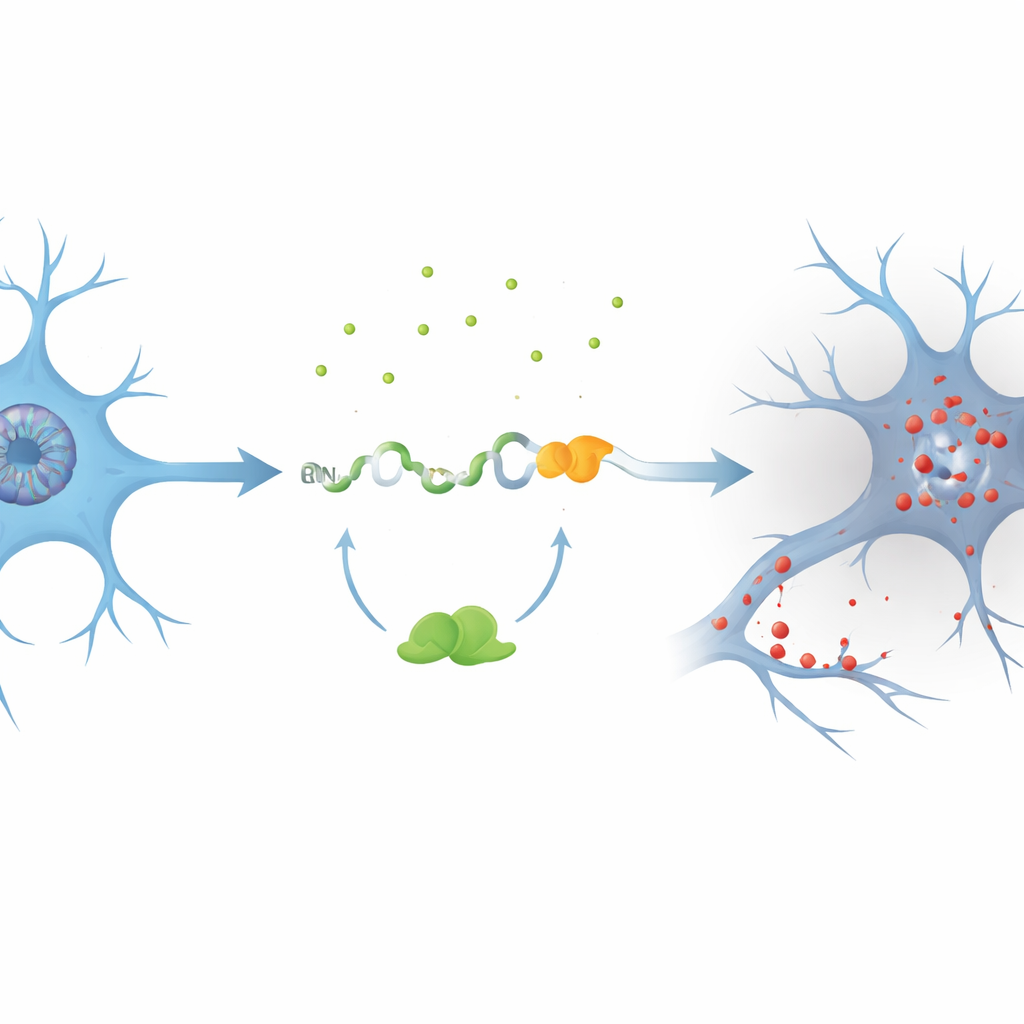
Данные из тканей пациентов и крупных наборов данных
Чтобы установить, происходит ли это явление при человеческих заболеваниях, исследователи проанализировали данные РНК‑секвенирования сотен образцов мозга и спинного мозга пациентов с БАС. Они обнаружили широкую активацию криптического экзона PKN1‑5a1 в областях, известных поражением TDP-43, таких как моторная кора и спинной мозг, но не в относительно сохранном мозжечке. Затем они получили высокоспецифичные антитела, распознающие только уникальный хвост PKN207, а не полноразмерный белок PKN1. В ткани гиппокампа пациентов с болезнью Альцгеймера, у которых также наблюдался аномальный фосфорилированный TDP-43, эти антитела обнаружили отчетливую полосу, соответствующую PKN207, тогда как в контрольных образцах такая полоса отсутствовала. Дополнительные наборы данных по болезни Альцгеймера подтвердили, что криптический экзон включается даже на ранних стадиях заболевания, что указывает на то, что эта молекулярная ошибка может начинаться задолго до появления явных симптомов.
Мини‑белок с большим влиянием на память
Обнаружение PKN207 в больном человеческом мозге подняло ключевой вопрос: вреден ли он? Чтобы проверить это, команда использовала вирусы для экспрессии либо нормального PKN1, либо PKN207 специально в гиппокампе — области мозга, критической для памяти — у молодых мышей. Спустя несколько месяцев у обеих групп мышей наблюдались нарушения обучения в тесте Морриса (водяной лабиринт): они дольше искали скрытую платформу. В их спинномозговой жидкости были повышены уровни легкой цепи нейрофиламента, маркера повреждения аксонов. В культивируемых нейронах усиление экспрессии PKN207 вызывало повреждение клеток, о чем свидетельствовал выход фермента, указывающего на нарушение мембраны. Детальное протеомное профилирование гиппокампа выявило широкие изменения в путях, связанных с синаптической силой (долговременная потенциация) и хорошо известными нейродегенеративными заболеваниями, с особенно сильным нарушением молекул, поддерживающих эффективную передачу сигналов и здоровый каркас нервных волокон.
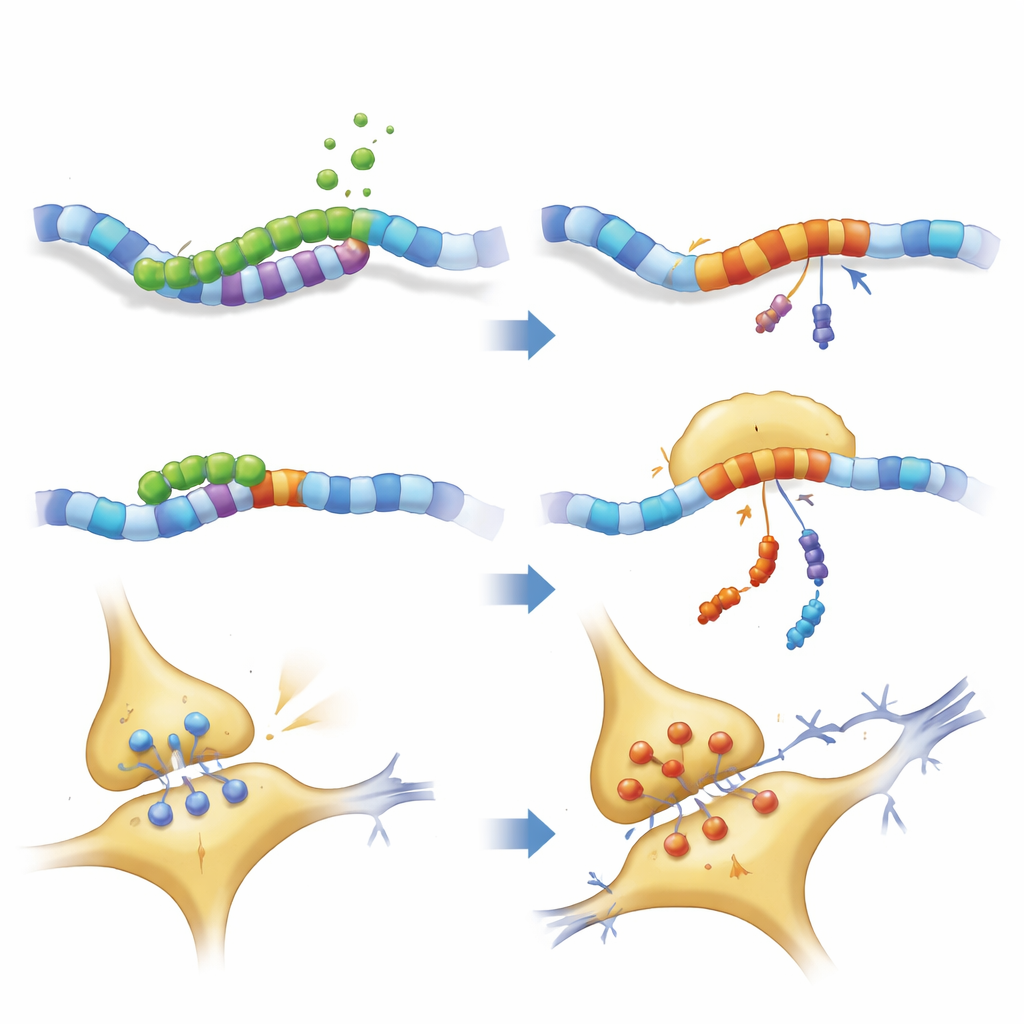
Как фрагмент нарушает схемы в мозге
Более тщательное изучение структуры нейронов показало, что и полноразмерный PKN1, и PKN207 нарушают сеть нейрофиламентов, которая придаёт аксонам форму и помогает транспортировать грузы. Ключевые моторные и каркасные белки были уменьшены, тогда как некоторые компоненты нейрофиламентов накапливались, намекая на пробки в транспортировке и возможное образование агрегатов. Электрофизиологические записи слайсов гиппокампа подтвердили, что у мышей с экспрессией PKN207 была ослаблена долговременная потенциация — процесс, при котором синапсы усиливаются после повторной активности и который считается клеточной основой обучения и памяти. Несмотря на то, что PKN207 лишен ферментативного домена PKN1, его присутствие было достаточным, чтобы имитировать и иногда превосходить нарушающие эффекты полного белка, что предполагает, что общая N‑концевая часть сама по себе может вмешиваться в гомеостаз нейронов.
Почему это открытие важно для заболеваний мозга
Эта работа добавляет новый слой к нашему пониманию расстройств, связанных с TDP-43. Вместо того чтобы просто вызывать потерю важных РНК, нарушение TDP-43 может также порождать стабильный токсичный микро‑белок, подрывающий синапсы и когнитивные функции. Криптический экзон PKN1‑5a1 и его пептидный продукт PKN207 теперь выделяются как потенциальные биомаркеры ранней дисфункции TDP-43 и как кандидатные мишени для терапии, направленной на коррекцию сплайсинга или блокирование вредного фрагмента. В более широком смысле исследование предполагает, что другие скрытые экзоны тоже могут давать начало пептидам, приводящим к болезни, что указывает исследователям на богатый — и ранее упускавшийся из виду — ландшафт молекулярных виновников нейродегенерации.
Цитирование: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Ключевые слова: TDP-43, криптический сплайсинг, PKN1, нейродегенерация, Болезнь Альцгеймера и БАС