Clear Sky Science · ru
Эпигенетическое противодействие белков FOX контролирует баланс между литическим и латентным состояниями герпесвируса
Почему скрытые герпесвирусы важны
Многие люди всю жизнь носят в себе вирусы простого герпеса и часто не знают об этом. Эти вирусы могут годами тихо находиться в нервных клетках, а затем внезапно вспыхивать, вызывая простудные высыпания, заболевания глаз или более серьёзные осложнения у людей с ослабленным иммунитетом. Что удерживает вирус в «сне» большую часть времени и что включает его обратно — оставалось давней загадкой. В этом исследовании раскрыта ключевая часть этой системы контроля: противоборство двух противоположных групп человеческих белков, которые перестраивают вирусную ДНК и определяют, остаётся ли герпес молчаливым или начинает производить новые вирусы.
Две клеточные команды, тянущие в противоположные стороны
Авторы сосредоточились на большой семье человеческих ДНК-связывающих белков, называемых белками FOX, которые обычно помогают управлять собственными генами при развитии и метаболизме. Тестируя множество членов семейства FOX в нервоподобных клетках, они обнаружили два чётких лагеря. Одна группа (включая такие белки, как FOXF1) сильно усиливала репликацию вируса простого герпеса типа 1 (HSV‑1) и нескольких родственных «альфа» герпесвирусов. Другая группа (FOXK1 и FOXK2) действовала противоположно, мощно подавляя размножение вируса. Этот баланс варьировал в зависимости от типа клетки: в не-нервных клетках и в напряжённых нейронах обычно было больше активирующих FOX-белков, тогда как в покоящихся сенсорных нейронах их было очень мало, а уровни репрессивных FOXK-белков были высокими.
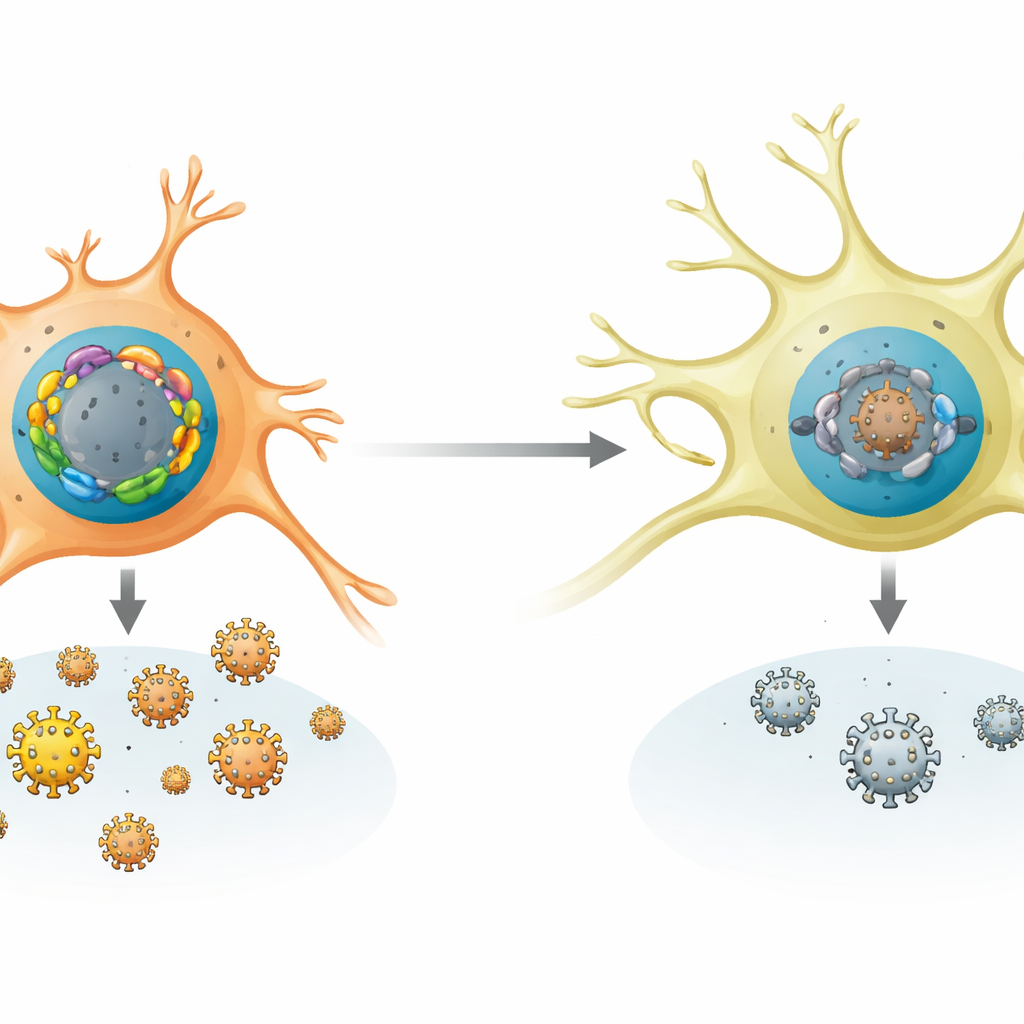
Почему нервные клетки предпочитают тихое состояние
Команда сравнила активность генов FOX в различных типах человеческих и мышиных клеток и у инфицированных животных. Сенсорные нейроны, естественная среда для латентного HSV‑1, продемонстрировали модель, благоприятную для тишины: сильная экспрессия FOXK1 и FOXK2 и слабая экспрессия большинства активирующих FOX-генов. У мышей ранняя фаза инфекции и поздние стрессовые сигналы, такие как повышение температуры или повреждение тканей, избирательно повышали уровни нескольких активирующих Fox-генов, не уменьшив при этом репрессивные. В культуре мышиных нейронов и в живых мышах удаление или снижение экспрессии FOXK-белков облегчало репликацию HSV‑1 и его возврат из латентного состояния. И наоборот, принудительная экспрессия активирующих FOX-белков в нейронах была достаточна для индукции реактивации даже без химических триггеров, что показывает, насколько чувствителен вирусный статус к этому балансу FOX.
Захват вирусной ДНК и её открытие или закрытие
Чтобы понять механизм, исследователи картировали места связывания белков FOX на вирусном геноме. Они обнаружили, что и активатор FOXF1, и репрессор FOXK1 связываются широко по всей ДНК HSV‑1, а не только в нескольких специфических последовательностях. Это связывание опирается на консервативную часть белков FOX, которая держится за остов ДНК, а не за отдельные нуклеотиды, что позволяет им прикрепляться практически в любом месте. Оказавшись на месте, две группы белков привлекают разные молекулярные партнёрские комплексы, которые перестраивают хроматин — сочетание ДНК и её упаковочных белков. Активирующие FOX-белки, особенно FOXF1, ассоциируются с CBP и P300 — ферментами, добавляющими ацетильные группы гистонам и ослабляющими хроматин. Это делает вирусную ДНК более доступной и усиливает экспрессию ранних, средних и поздних вирусных генов. В отличие от них, FOXK1 работает с факторами вроде SIN3A и MAX, связанными с деацетилированием гистонов и репрессией генов, уплотняя вирусный хроматин и удерживая гены в выключенном состоянии.
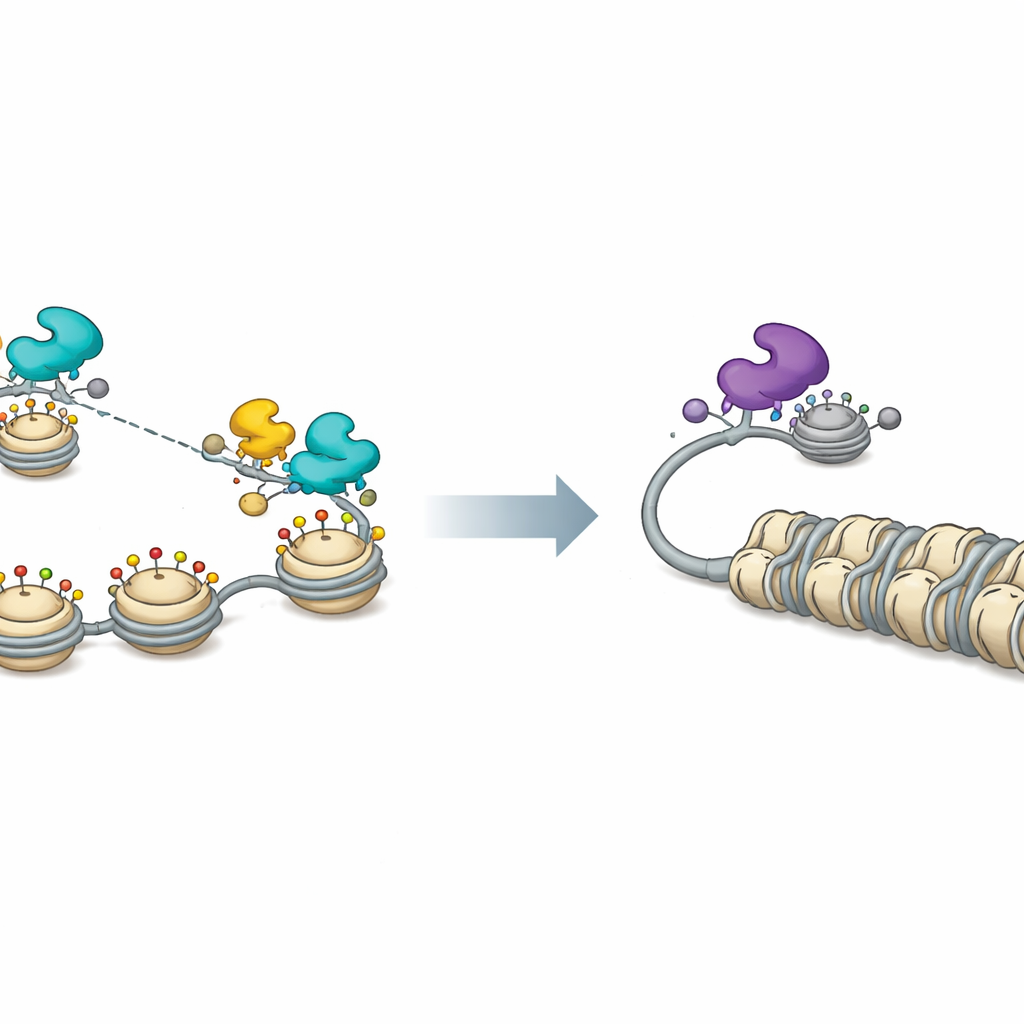
Хроматиновый переключатель для сна и пробуждения вируса
Измерения состояния вирусного хроматина подтвердили эту картину. При наличии FOXF1 гистоны на вирусной ДНК были удалены или химически помечены признаками открытого, активного хроматина, и общая доступность вирусных промоторов увеличивалась по всему геному. Экспрессия FOXF1 также нарушала небольшие ядерные структуры, называемые PML-ядерными телами, которые обычно помогают удерживать вирусную ДНК в репрессированном состоянии. Блокирование CBP и P300 устраняло многие из этих активирующих эффектов и снижало вызванную FOXF1 экспрессию вирусных генов. С репрессивной стороны исследователи показали, что партнёры FOXK1 и активность гистондеацетилаз важны для поддержания низкой репликации HSV‑1; химическая ингибиция деацетилаз как усиливала выход вируса, так и ослабляла подавление, опосредованное FOXK1.
Что это значит для контроля пожизненной инфекции
В целом работа показывает, что активность или спячка HSV‑1 во многом зависят от соотношения белков FOX в клетке‑хозяине нейроне. Покоящиеся сенсорные нейроны естественным образом склоняются к репрессивному состоянию, доминируемому FOXK, что переводит вирус в глубокую молчаливую форму с компактным хроматином. Стрессы или другие условия, повышающие уровень активирующих FOX-белков, могут сдвинуть этот баланс, открыть вирусный хроматин и снова запустить литический цикл. Раскрывая эту эпигенетическую борьбу, исследование указывает на новые подходы, с помощью которых учёные в будущем могут либо сильнее удерживать герпесвирусы в безвредной латентности, либо, наоборот, вынуждать их выйти из укрытия под контролируемыми условиями для последующего уничтожения.
Цитирование: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Ключевые слова: латентность вируса простого герпеса, факторы транскрипции FOX, вирусная хроматин, эпигенетическая регуляция, реактивация вируса