Clear Sky Science · ru
Расширение потенциала повреждения ДНК искусственными металло-нуклеазами с помощью click-химии
Создание более «умных» молекулярных ножниц
Химиотерапия часто действует за счёт повреждения ДНК раковых клеток, но современные препараты нередко оказываются грубым инструментом, повреждающим и здоровые ткани. В этом исследовании рассматривается новый класс высокопрограммируемых «молекулярных ножниц», собранных из меди и небольших органических фрагментов с использованием click-химии. Путём настройки формы и способов захвата ДНК исследователи стремятся создать агенты, которые режут генетический материал более избирательно, открывая пути для будущих противораковых и антибактериальных терапий.
Сборка трёхлучевого резца
Команда использует медь-катализируемую click-химию — метод, отмеченный Нобелевской премией и известный своей надёжностью — для сборки семейства молекул, названных Tri-Click (TC) лигандами. Каждая молекула TC представляет собой трёхлучевую «восьмёрку», которая одновременно может удерживать три иона меди, образуя компактный кластер, способный атаковать ДНК. Путём замены различных химических «донорных» групп на концах лучей — на основе азота, кислорода или серы — учёные систематически тестировали, как тонкие структурные изменения влияют на связывание меди, распознавание ДНК и биологическую активность. Среди нескольких новых конструкций особенно выделились варианты с плоскими кольцевыми азотсодержащими донорами, которые оказались многообещающими для прочного захвата ДНК.
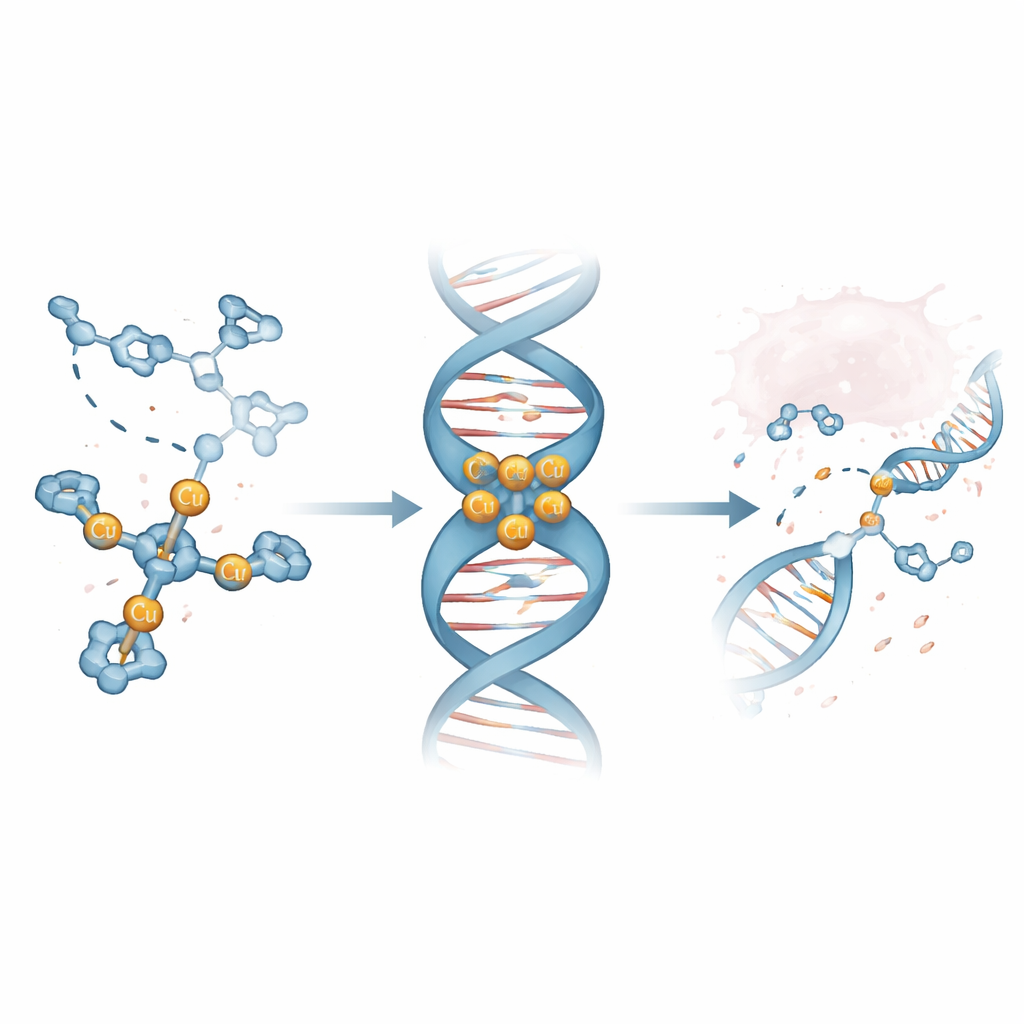
Нахождение лидирующей молекулы, «любящей» бороздки ДНК
С помощью масс-спектрометрии и оптических методов исследователи показали, что один комплекс, названный Cu3-TC-Py, стабильно формирует трёхмедный кластер в растворе. Эксперименты конкуренции с флуоресцентными красителями, связанными с телячьей тимусной ДНК, выявили, что Cu3-TC-Py вытесняет эти красители при очень низких концентрациях, что указывает на сильное связывание с ДНК. Последующие тесты на коротких «шпильковых» фрагментах ДНК показали, что этот комплекс предпочитает размещаться в малой бороздке — узкой впадине, идущей по спирали двойной цепи — и особенно благоприятствует участкам, богатым парами G и C. Высокоточные компьютерные моделирования подтвердили эту картину: трёхлучевой комплекс располагается в бороздке, его положительные заряды охватывают отрицательно заряженную ДНК и слегка уплотняют спираль.
От плотного связывания до коллапса и разрывов ДНК
На уровне одиночных молекул команда наблюдала длинные молекулы ДНК, заключённые в наноканалы, при взаимодействии с Cu3-TC-Py. При низких дозах комплекс конкурировал с растягивающим красителем, вытесняя его по мере того, как связывался в бороздках. При более высоких дозах ДНК начинала сокращаться, а затем полностью конденсироваться — что согласуется с сильным электроstatic притяжением между медным кластером и остовом ДНК. При обработке плазмидной ДНК в присутствии восстановителя молекулы переходили из родной свернутой формы в релаксированные, а затем полностью линейные формы — типичный рисунок, сигнализирующий о появлении одно- и двусцепочных разрывов. Дополнительные тесты с ловушками радикалов указывали на кратковременные кислородсодержащие виды — такие как супероксид, синглетный кислород и гидроксильные радикалы — как на истинные режущие «инструменты», генерируемые вблизи связанного комплекса.
Атака на ДНК в раковых и бактериальных клетках
Перейдя от очищенной ДНК к живым клеткам, исследователи изучили поведение Cu3-TC-Py в клеточной среде. В панелях раковых клеток свободные лиганды с азотсодержащими ароматическими группами показали существенно более сильное подавление роста по сравнению с предыдущими конструкциями, а полностью сформированный медный комплекс оказался ещё более мощным, убивая несколько раковых линий при микромолярных концентрациях. Измерения внутриклеточной меди показали, что Cu3-TC-Py эффективно переносит медь внутрь клеток и вызывает накопление повреждений ДНК, что было зафиксировано методом визуализации с участием ферментативного помечания, отмечающего повреждения вдоль растянутых геномных нитей. В бактериях микроскопия показала, что обработка быстро разрушает компактную бактериальную хромосому, распределяя ДНК по всей клетке и имитируя сильную фрагментацию, наблюдаемую при действии мощного антибиотика, повреждающего ДНК, что свидетельствует о широкомасштабном генетическом разрушении.
Почему эти дизайнерские ножницы важны
Для неспециалиста ключевая мысль заключается в том, что исследователи превратили простой модульный каркас click-химии в тонко настроенный аппарат для разрезания ДНК. Выбрав подходящие кольцевые азотные группы, они создали компактный медный кластер, который вставляется в специфическую бороздку ДНК, притягивает цепи друг к другу и локально генерирует реакционноспособные формы кислорода, разрезающие двойную спираль. Ведущее соединение Cu3-TC-Py эффективно повреждает ДНК как в раковых, так и в бактериальных клетках и демонстрирует, как рациональный дизайн может усилить действие металлических лекарств. Хотя до клинического применения ещё далеко, исследование прокладывает правила проектирования для следующего поколения молекулярных ножниц, которые однажды могут предложить более таргетированные противораковые терапии и новые антимикробные стратегии.
Цитирование: Gibney, A., Sidarta, M., Delahunt, E. et al. Expanding the DNA damaging potential of artificial metallo-nucleases with click chemistry. Nat Commun 17, 2309 (2026). https://doi.org/10.1038/s41467-026-68911-5
Ключевые слова: click-химия, повреждение ДНК, комплексы меди, противораковые препараты, искусственные нуклеазы