Clear Sky Science · ru
Эволюционное переназначение комплекса метаболической тиолазы позволяет синтез антибиотиков
Как повседневные микробы переизобретают свою химию
Многие антибиотики и лекарства, на которые мы полагаемся, тихо создаются бактериями. Эти крошечные «химики» используют ферменты — молекулярные машины — для сборки сложных защитных соединений. В этом исследовании показано, как основной метаболический ферментный комплекс, когда-то служивший для базового клеточного обслуживания, был эволюционно перепрограммирован в оральных бактериях для производства мощного антибиотика. Понимание этой трансформации не только раскрывает механизмы появления новой биохимии в природе, но и даёт подсказки для проектирования лекарств и биокатализаторов следующего поколения.
От базового метаболизма к химическому оружию
Все живые клетки зависят от набора консервативных ферментов, которые ведут их центральный метаболизм — например, расщепление жиров и синтез ключевых молекул. Одна из таких групп, называемая суперсемейством тиолаз, обычно помогает обрабатывать малые энергоёмкие молекулы вроде ацетил‑CoA и поддерживает жизненно важные пути синтеза липидов и других компонентов клетки. Авторы обнаружили, что у нескольких видов оральных Streptococcus трёхкомпонентный комплекс на основе тиолазы — состоящий из белков, родственных HMGS, ACAT и третьему вспомогательному белку — отказался от своей исконной метаболической роли. Вместо этого этот комплекс завершает биосинтез антибиотика реитерициллина A, который помогает этим бактериям конкурировать в плотной среде ротовой полости.
Новый тип ферментативной реакции на каркасе антибиотика
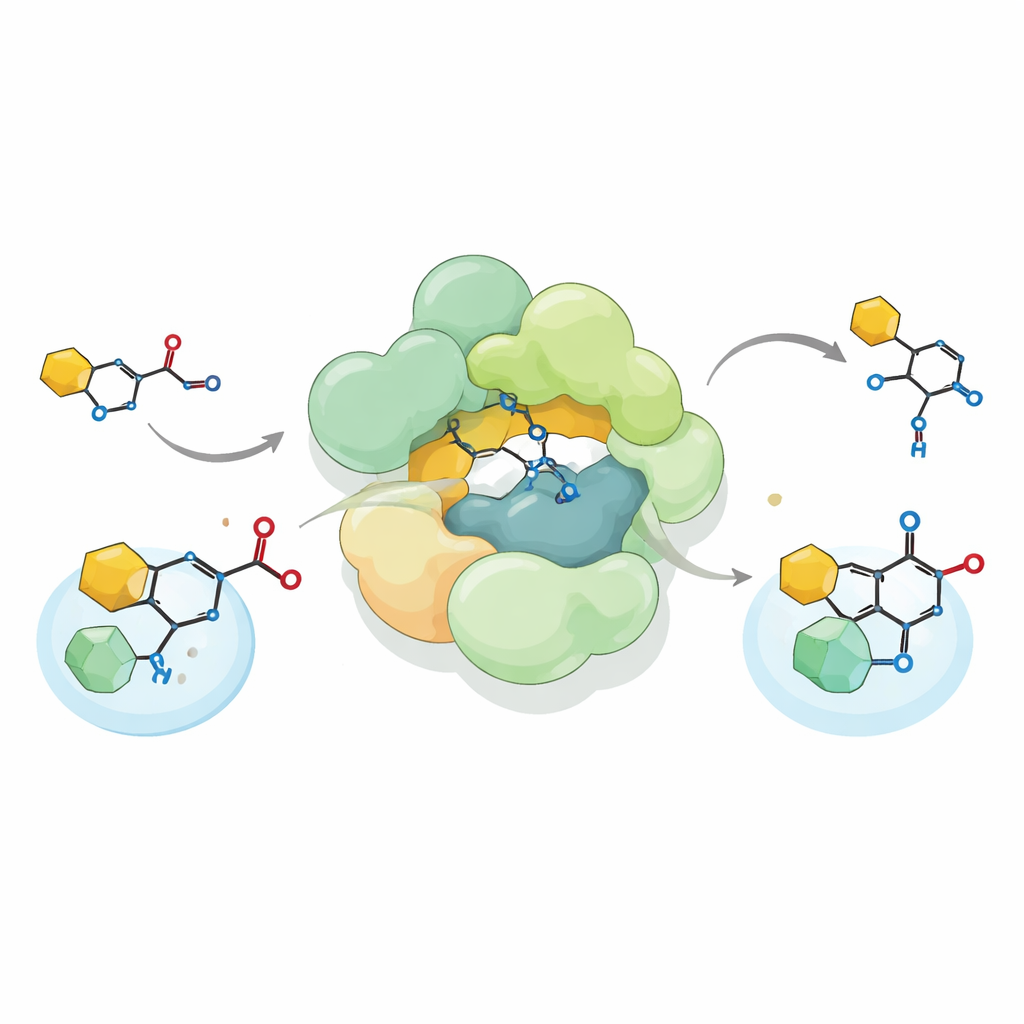
Реконституировав в лаборатории стрептококковый комплекс и подавая ему химически синтезированный предшественник реитерициллина A, исследователи показали, что комплекс выполняет нетипичную реакцию образования углерод‑углеродной связи, известную как C‑ацилирование Фриделя–Крафтса. Вместо присоединения ацетильной группы к кислороду, как это делают многие ферменты, он устанавливает эту группу прямо на атом углерода в кольце пирролидина‑2,4‑диона — важной части скелета реитерициллина. Комплекс принимает как естественные доноры ацетила, такие как ацетил‑CoA, так и несколько искусственных доноров, а затем может даже обратить реакцию в обратную сторону, разрывая созданную связь. Такая гибкость расширяет известный репертуар биологических ацилтрансфераз и указывает на пути адаптации подобных ферментов для сборки разнообразных химических продуктов.
Переназначение консервативного белкового каркаса
Используя криоэлектронную микроскопию высокого разрешения, команда решила трёхмерную структуру стрептококкового комплекса, названного SmaATase. Несмотря на новую функцию, SmaATase сохраняет поразительное архитектурное сходство с родственным комплексом у архей, участвующим в мевалонатном пути синтеза изопреноидных липидов. Оба — крупные мультимерные сборки, построенные из повторяющихся модулей, и имеют общую полость, где кофактор CoA способен связываться и перемещаться между активными центрами. Однако ключевые каталитические остатки, необходимые для исходной метаболической реакции, в бактериальной версии отсутствуют или изменены. Биохимические тесты подтверждают, что SmaATase больше не способен синтезировать предковый продукт HMG‑CoA и вместо этого использует ацетил‑CoA исключительно как донор для своих новых маломолекулярных субстратов.
Эволюционный путь от метаболизма к антибиотикам
Чтобы понять, как могло произойти такое переназначение, авторы сравнили последовательности и активности родственных комплексов у множества бактерий и архей. Они выявили более тысячи генных кластеров, содержащих ту же триаду типов ферментов. Некоторые по‑прежнему поддерживают классическую тиолазную химию; другие, например у Pseudomonas, обеспечивают синтез разных малых антибиотических молекул. Представительный комплекс от Pseudomonas fluorescens, по‑видимому, находится на полпути вдоль этого эволюционного пути: его домен, похожий на HMGS, отключён, но его блок, подобный ACAT, по‑прежнему выполняет более традиционную реакцию на CoA‑связаных субстратах. В SmaATase и его псевдомонадовском аналоге, который синтезирует защитное для растений соединение DAPG, дальнейшие изменения вокруг активного центра настроили ферменты на распознавание нестандартных акцепторов, таких как ароматические кольца или тетрамовая кислотная основа.
Почему крошечная ацетильная группа имеет большое значение
В итоге биологическая выгода этой молекулярной переделки очевидна. Когда команда протестировала ацетилированные антибиотики реитерициллин A и DAPG на панели грамположительных бактерий, эти молекулы показали сильную убивающую активность, тогда как их неацетилированные предшественники были значительно слабее или почти неактивны. Эта небольшая ацетильная группа, размещённая в точно нужной позиции репурпозированным ферментным комплексом, превращает скромный каркас в мощное оружие, позволяя Streptococcus во рту или Pseudomonas вокруг корней растений вытеснять соседей. Эта работа демонстрирует, как эволюция может переработать существующие ферментные платформы с минимальными, но стратегическими мутациями, превращая рутинную метаболическую машину в специализированный инструмент химической защиты — и даёт дорожную карту инженерам, стремящимся проектировать новые каталитические системы для формирования связей углерод–углерод в открытии лекарств и синтетической биологии.
Цитирование: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Ключевые слова: эволюция ферментов, биосинтез природных продуктов, антибиотическая химия, метаболическое переназначение, реакция Фриделя–Крафтса ацилирования