Clear Sky Science · ru
Моделирование идиопатического легочного фиброза на основе человеческих iPSC показывает, что ингибирование p300/CBP подавляет транзиторное альвеолярное состояние клеток
Почему нам всем важно понимать рубцевание лёгких
Идиопатический легочный фиброз (ИЛФ) — это прогрессирующее заболевание, при котором лёгкие постепенно заменяются рубцовой тканью, и каждый вдох даётся всё труднее. Существующие препараты лишь замедляют этот процесс и часто вызывают серьёзные побочные эффекты. В этом исследовании с помощью передовых методов работы со стволовыми клетками и геномики воссоздали рубцовые лёгкие в лаборатории и задали простой, но важный вопрос: можно ли найти переключатель, который направит повреждённые лёгочные клетки не в вредное состояние, а обратно к восстановлению?
Окно в рубцовое лёгкое — выращенное в лаборатории
Чтобы изучить ИЛФ, учёные создали миниатюрные лёгкие из индуцированных плюрипотентных стволовых клеток человека (iPSC). Эти iPSC направляли в дифференцировке в альвеолярные клетки — клетки, выстилающие крошечные воздушные мешочки, где кислород поступает в кровь — и выращивали вместе с лёгочными фибробластами, клетками соединительной ткани, образующими рубец. Вмешанные в мягкий гель, эти «альвеолярные органоиды» вели себя похоже на настоящую лёгочную ткань. При воздействии химиотерапевтического препарата блеомицин, известного как индуктор повреждения лёгких, гели сжимались по мере того, как фибробласты тянули их, имитируя сокращение ткани, наблюдаемое при фиброзе.
Используя эту систему, команда просcreenировала библиотеку из 264 малых молекул и автоматически измеряла, насколько каждая из них предотвращала сокращение геля, при этом глубокая нейросеть для анализа изображений обеспечивала объективные результаты. Многие соединения не оказывали эффекта, но одна группа явно выделялась: ингибиторы белков p300 и CBP, участвующих в контроле упаковки ДНК и активации генов. Все восемь соединений, нацеленных на p300/CBP, в библиотеке уменьшали сокращение при низких дозах, что выдвинуло этот путь как перспективную мишень для борьбы с фиброзом. 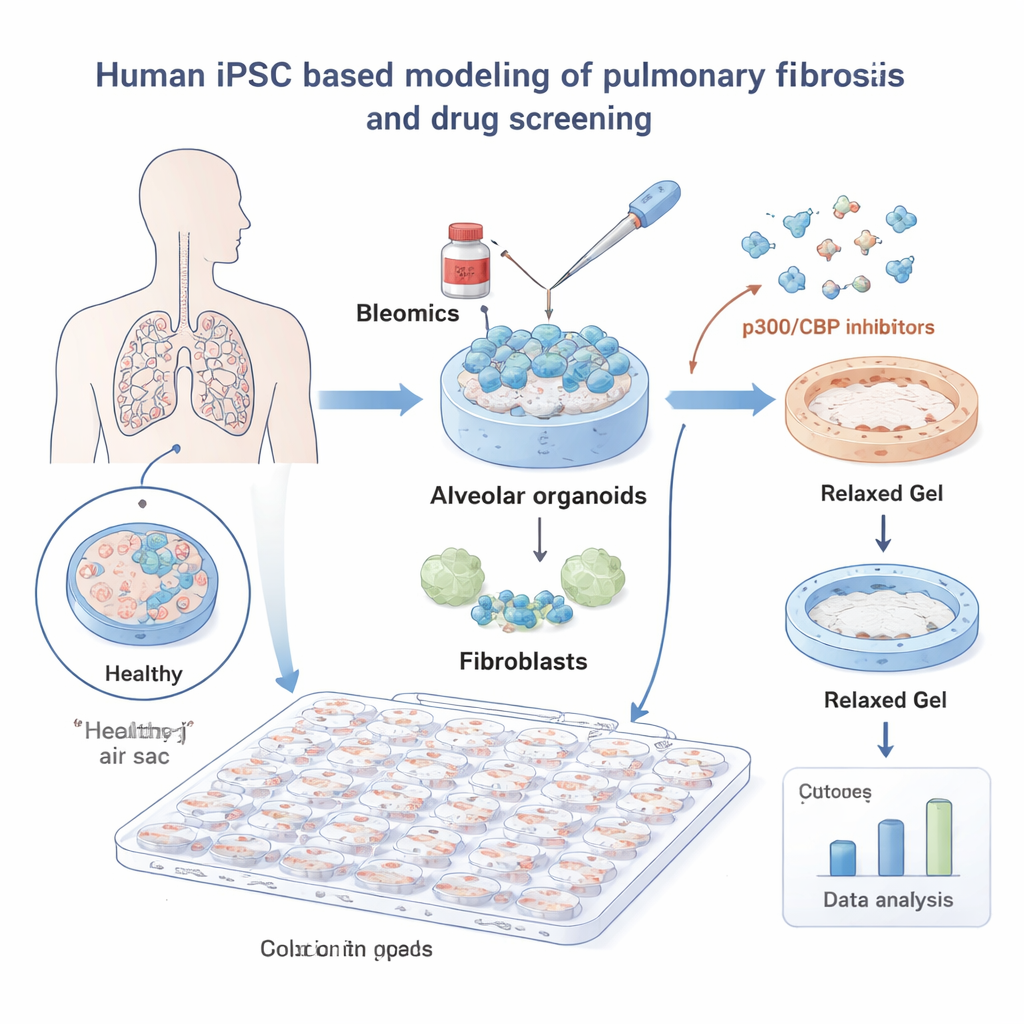
Виновники: транзиторные лёгочные клетки
Недавние исследования выявили проблемный «переходный» тип клеток в больных лёгких, называемый альвеолярным транзиторным состоянием. В норме поддерживающие клетки AT2 созревают в ультратонкие AT1-клетки, покрывающие альвеолы и обеспечивающие газообмен. При ИЛФ же AT2 часто застревают в этом переходном состоянии, экспрессируя гены стресса и ремонта и не завершая превращение в полноценные AT1. Эти транзиторные клетки сосредоточены в фиброзных областях и интенсивно взаимодействуют с фибробластами, но оставалось неясным, являются ли они просто следствием повреждения или активными драйверами рубцевания.
Секвенирование РНК и профиль открытой хроматиновой архитектуры в их органоидах показали, что транзиторные клетки, возникающие в модели, очень близки к тем, что обнаружены в лёгких пациентов с ИЛФ. Эти индуцированные транзиторные клетки демонстрировали сигнатуры генов, связанные со стрессом, воспалением и ремоделированием матрикса, и сильно активировали сопряжённые взрослыми лёгочными фибробластами. Важный момент: при блокаде p300/CBP маркеры переходного состояния снижались, сохранялась идентичность AT2, и активность фибробластов ослабевала. Иными словами, препараты не уничтожали клетки в целом; они выборочно предотвращали «застревание» AT2 в этом вредном промежуточном состоянии.
Распутывая молекулярные переключатели
Чтобы понять, как p300/CBP влияет на это решение судьбы клетки, команда изучала химические метки на гистонах — белках, которые помогают упаковывать ДНК. Особая метка, ацетилирование H3K27, обычно наносится p300/CBP на активных энхансерах и промоторах. У транзиторных клеток области рядом с генами ответа на стресс и профибротическими генами несли сильное H3K27-ацетилирование и были обогащены сайтами связывания транскрипционных факторов, таких как AP‑1 и HNF1B. При обработке клеток ингибиторами p300/CBP эти ацетильные метки ослаблялись в указанных регионах, и экспрессия многих профибротических генов снижалась. Прямое блокирование AP‑1 или снижение уровней AP‑1 и HNF1B с помощью малых интерферирующих РНК аналогично подавляло транзиторную программу и сокращение органоидов, связывая триаду — p300/CBP, AP‑1 и HNF1B — с механизмом, который подпитывает фибротическое ремоделирование.
Вне чашки Петри исследование проверило один ингибитор, CBP30, на мышах с блеомицин-индуцированным повреждением лёгких. Животные, получавшие CBP30, имели меньше транзиторных эпителиальных клеток, меньшую активацию миофибробластов, формирующих рубцы, и пониженную экспрессию маркеров фиброза. Это поперечное подтверждение между человеческими моделями на основе стволовых клеток и животной моделью укрепляет довод в пользу того, что p300/CBP — это не артефакт системы in vitro, а реальный регулятор рубцевания лёгких. 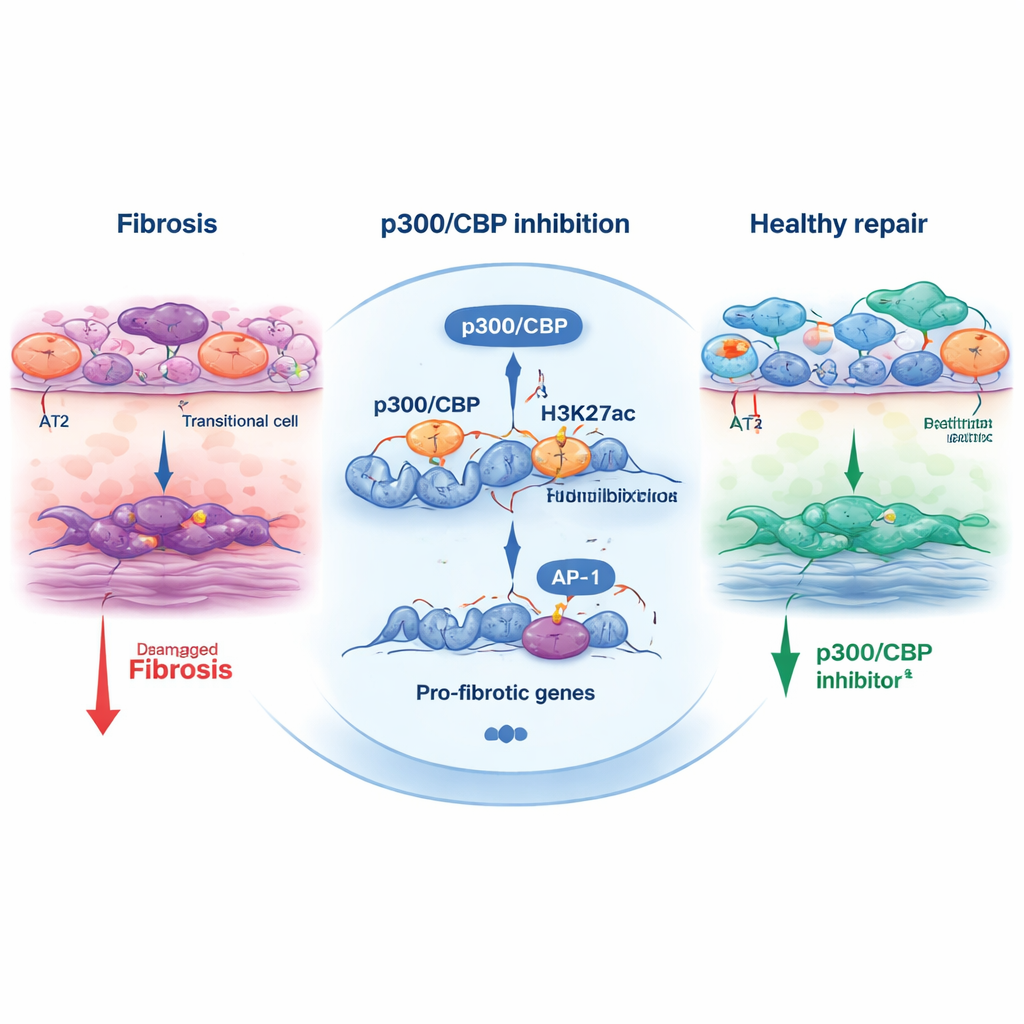
Что это значит для будущих терапий
Для неспециалистов ключевой вывод таков: авторы создали реалистичную человеческую модель фиброзных лёгких и использовали её, чтобы выявить новую лекарственную мишень. Их работа показывает, что рубцевание лёгких частично управляется обратимым, индуцированным стрессом транзиторным клеточным состоянием, которое дезориентирует окружающую ткань. Понизив активность p300/CBP, возможно, удастся «приглушить» это состояние, удержать альвеолярные клетки на здоровом пути развития и снизить сигналы, заставляющие фибробласты работать в усиленном режиме. Хотя ингибиторы p300/CBP ещё требуют оптимизации по безопасности и клинической проверки, это исследование указывает в направлении терапии, которая воздействует на корневое клеточное нарушение в ИЛФ, а не просто замедляет его последствия.
Цитирование: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
Ключевые слова: идиопатический легочный фиброз, альвеолярные органоиды, ингибиторы p300/CBP, транзиторные эпителиальные клетки, легочные стволовые клетки