Clear Sky Science · ru
Инженерия плазмид со синтетическими_origin_ами репликации
Почему важно переписывать микробную ДНК
Многие инструменты современной биотехнологии — от производства инсулина до передовых генетических схем — опираются на маленькие кольца ДНК, называемые плазмидами. Эти генетические рабочие лошадки доставляют сконструированные гены в бактерии, но их базовая конструкция почти не менялась десятилетиями. В этом исследовании показано, что самое сердце плазмид — последовательности, которые подсказывают клетке, когда и как часто копировать плазмиду — можно полностью переосмыслить. Перестроив этот «движок копирования» с нуля, авторы создали плазмиды, которые проще настраивать, комбинировать и программировать, что открывает путь к более гибким диагностическим методам, биопроизводству и синтетической биологии.
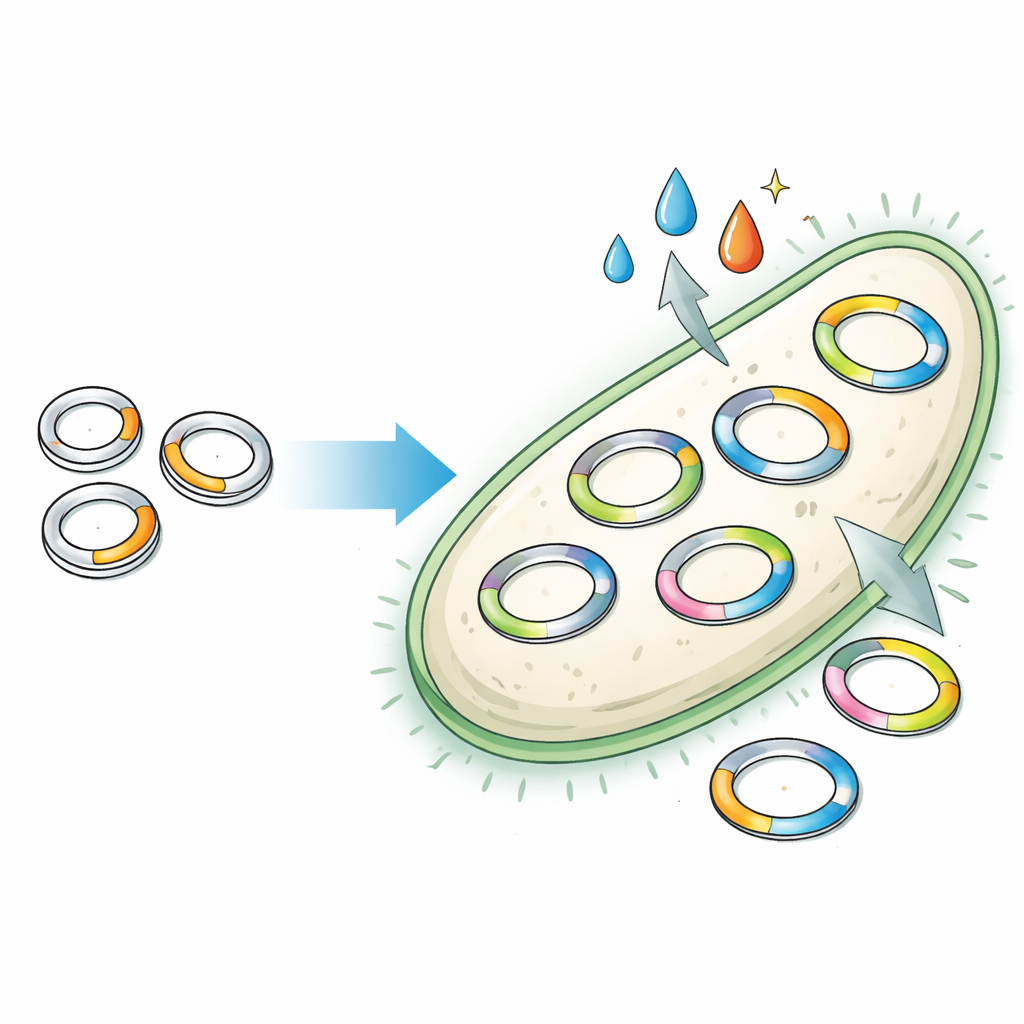
Старые инструменты с скрытыми ограничениями
Плазмиды естественно эволюционировали как мобильная ДНК, позволяя бактериям делиться признаками, такими как устойчивость к антибиотикам или новые способы усвоения питательных веществ. В лаборатории инженеры заимствуют эти плазмиды для переноса полезных генов, но большинство опираются на несколько классических конструкций, открытых в 1980-х. Те старые дизайны скрывают клубок перекрывающихся генетических частей, которые контролируют количество копий плазмиды в каждой клетке и совместимость разных плазмид друг с другом. Поскольку эти части слиты, изменение одной функции может непредсказуемо нарушить другую. В результате ученые ограничены небольшим набором плазмид с фиксированным числом копий и ограниченной совместимостью, что сдерживает сложность конструируемых систем.
Перестройка двигателя копирования с нуля
Исследователи сосредоточились на широко используемом источнике репликации из семейства плазмид pMB1. В естественной форме этот источник опирается на тонко сбалансированную «переписку» между двумя РНК — одной, запускающей копирование ДНК, и другой, его подавляющей — чтобы удерживать число плазмид под контролем. Команда сначала «рефакторила» эту систему: разделила перекрывающиеся гены, отключила скрытый промотор и разместила ключевые элементы на отдельных, чистых генетических кассетах. Это показало, что основная задача источника может быть сохранена при упрощении его структуры, превращая беспорядочную, формированную эволюцией деталь во что-то более модульное, с доступными компонентами.
Вставка синтетических регуляторов
После того как оригинальная логика управления оказалась раскрыта, авторы заменили её полностью синтетическими регуляторами. Они связали праймер репликации с разработанными РНК-переключателями, действующими как регуляторы яркости: небольшие управляющие РНК могут переключать эти схемы, разрешая или блокируя производство праймера и тем самым контролируя копирование плазмиды. Подбирая разные варианты переключателей и соединяя их с промоторами различной силы, они настроили число копий плазмид в диапазоне более чем двух порядков величины. Также исследовали разные физические компоновки управляющих кассет в ДНК, обнаружив схемы, которые повышают стабильность и позволяют сократить область репликации до компактного функционального ядра при добавлении естественных вспомогательных систем, предотвращающих проблемные взаимодействия между плазмидами.
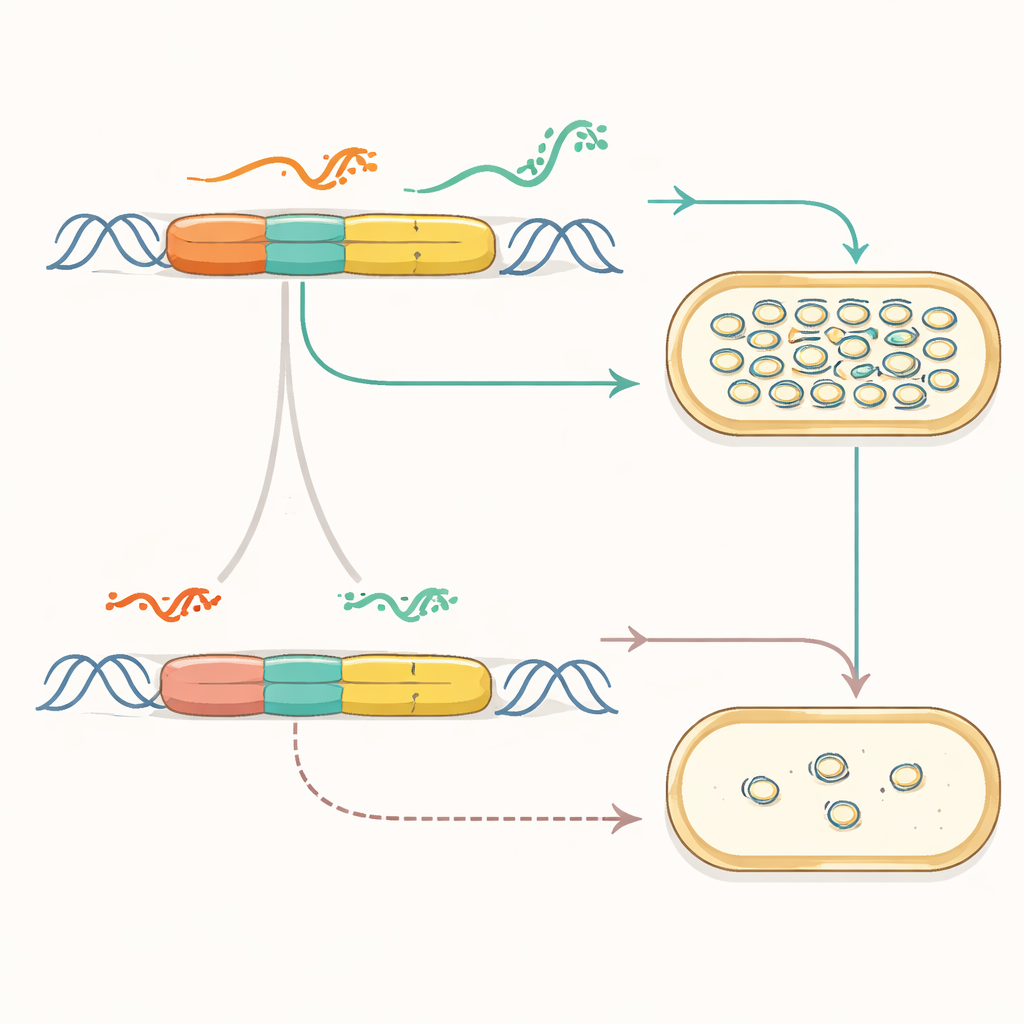
Преобразование химических сигналов в количество ДНК
Став модульным, двигатель копирования показал возможность подключения к внешним сигналам. Они соединили синтетический источник с индуцибельными промоторами и структурами РНК, называемыми рибосвитчами, которые меняют форму в ответ на малые молекулы. В этих новых плазмидах добавление химического вещества, например IPTG или cumate, вызывало рост или падение числа копий плазмид — и, следовательно, уровня репортера. Несколько сигналов можно было комбинировать так, чтобы одна молекула стимулировала копирование, а другая его ограничивала. Исследователи даже собрали пары плазмид, каждая из которых реагировала на разное химическое вещество, и отслеживали изменение их числа в одной клетке с помощью секвенирования плазмид, фактически превращая количество плазмид в штрих-код экологической истории.
Множество кастомных плазмид в одной клетке
Ключевой проверкой подхода стало то, могут ли несколько независимо управляемых плазмид мирно сосуществовать. Воспользовавшись библиотекой ортогональных РНК-регуляторов, команда собрала шесть разных плазмид, каждая со своим синтетическим источником и маркером антибиотика, и ввела все шесть одновременно в E. coli. Секвенирование полных плазмид в течение нескольких дней подтвердило, что все шесть остаются в клетках, хотя их относительные количества менялись. Попытки проделать то же самое с шестью обычными плазмидами потерпели неудачу, что подчёркивает: рефакторинг и добавленные системы стабильности делают новые плазмиды более совместимыми и устойчивыми при совместном культивировании в одной клетке.
Что это значит для будущей биотехнологии
Для неспециалиста вывод прост: авторы превратили плазмиды из жёстких, универсальных инструментов в настраиваемую платформу. Их синтетические источники репликации работают как модульные двигатели, скорость, чувствительность и входы которых можно выбирать по требованию. Это позволяет создавать бактерии, которые записывают химические воздействия в виде изменений числа копий ДНК, тестировать множество генетических путей параллельно, распределяя их по разным плазмидам, или тонко уравновешивать рост и продукцию в промышленных штаммах. Хотя частично остаются компромиссы по стабильности, работа показывает, что основные механизмы репликации плазмид больше не являются недоступными для инженерии, открывая новые возможности для инноваций в синтетической биологии.
Цитирование: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Ключевые слова: синтетические плазмиды, источник репликации, регуляторы РНК, контроль числа копий, синтетическая биология