Clear Sky Science · ru
Рецептор сукцината 1 ограничивает гемопоэз и предотвращает прогрессирование острого миелоидного лейкоза
Когда клеточное топливо выходит из-под контроля
Наша кровь постоянно обновляется небольшой популяцией стволовых клеток, скрытых в костном мозге. В этом исследовании изучается, как обычный метаболический побочный продукт — сукцинат — и его датчик на поверхности клетки действуют как тормоз для этой системы обновления. Когда этот тормоз выходит из строя, равновесие между нормальным кроветворением и раковым ростом может сместиться в сторону острого миелоидного лейкоза (ОМЛ) — агрессивного рака крови. Понимание этого скрытого переключателя контроля может привести к более точным методам лечения, которые сдерживают болезнь, восстанавливая собственные защитные механизмы организма.
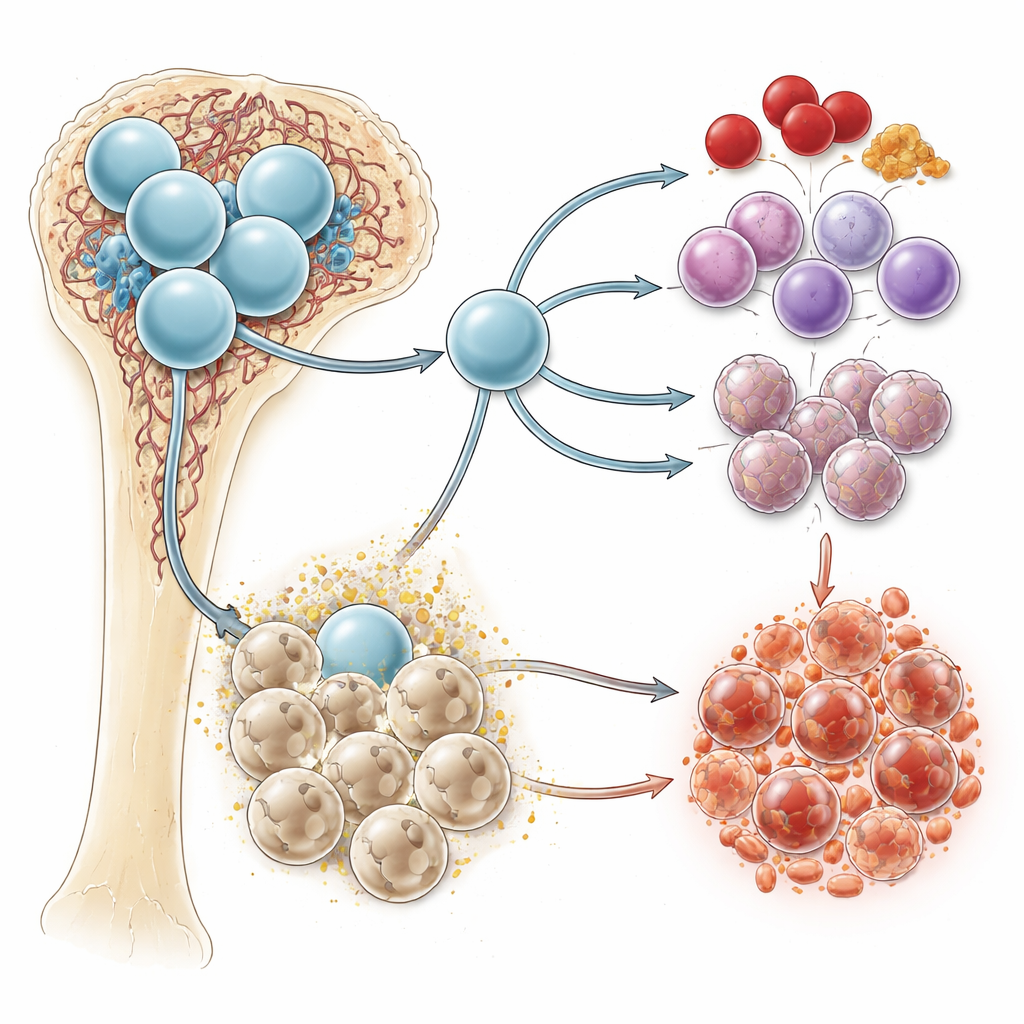
Химический сигнал с двойной ролью
Сукцинат — обычный побочный продукт того, как клетки сжигают топливо, особенно внутри митохондрий, энергетических станций клетки. В условиях пониженного содержания кислорода — как это бывает в костном мозге — сукцинат склонен накапливаться. Он может действовать внутри клеток, изменяя метаболизм и воспалительные реакции, а также выходить наружу и служить сигналом. На поверхности клетки рецептор SUCNR1 обнаруживает сукцинат и передаёт сигнал внутрь. Предыдущие работы связывали сукцинат и SUCNR1 с воспалением и создание среды, благоприятной для рака, но их прямая роль в кроветворении и лейкозе была неясна.
Предупреждающий сигнал у пациентов с лейкозом
Исследователи проанализировали данные экспрессии генов у сотен пациентов с ОМЛ и обнаружили, что уровни SUCNR1 сильно варьируют между людьми. У пациентов, чьи лейкемические клетки продуцировали мало SUCNR1, была меньшая общая и безрецидивная выживаемость, даже после учёта возраста, пола и стандартных клинических подтипов. Некоторые генетические подгруппы ОМЛ особенно часто характеризовались низким уровнем SUCNR1. Когда команда трансплантировала человеческие клетки ОМЛ без SUCNR1 в иммунодефицитные мыши и затем вводила животным щавелевую кислоту (которая в организме превращается в сукцинат), нагрузка лейкоза в костном мозге увеличивалась. Это указывает на то, что при раке с низким уровнем SUCNR1 дополнительный сукцинат может фактически подпитывать прогрессирование болезни, а не сдерживать его.
Скрытый тормоз для стволовых клеток крови
Чтобы понять, как SUCNR1 действует при нормальном кроветворении, учёные обратились к генетически модифицированным мышам. При удалении SUCNR1 либо во всём организме, либо только в кроветворных клетках костный мозг становился гиперактивным. Количество стволовых и прогениторных клеток увеличивалось, а также в крови и селезёнке возрастало число миелоидных клеток (например, моноцитов и гранулоцитов) и В-клеток. Эти стволоподобные клетки лучше выживали и образовывали больше колоний в чашке Петри, хотя они были немного менее способны восстанавливать кроветворение при трансплантации в конкуренции с нормальными клетками. Особая репортерная линия мышей показала, что только подпопуляция стволовых и прогениторных клеток действительно экспрессирует SUCNR1; эти SUCNR1-положительные клетки имели особенно ограниченный потенциал при приживлении. В целом рецептор действовал как сдерживающий фактор по отношению к размеру и активности пула стволовых клеток.
От сбалансированной защиты к воспалительному перегрузу
Детальное профилирование экспрессии генов в стволовых и прогениторных клетках, лишённых SUCNR1, выявило поразительный сдвиг. Отпечатки, характерные для спокойных, примитивных стволовых клеток, были приглушены, тогда как гены, связанные с воспалением, реактивными формами кислорода и зрелыми кровяными клетками, были увеличены. Две молекулы особенно выделялись: S100A8 и S100A9 — пара «тревожных» белков, усиливающих воспалительную сигнализацию. Эти факторы были повышены как внутри стволового компартмента, так и в окружающей жидкости костного мозга. Когда командa лечила мышей без SUCNR1 тасхинимодом — препаратом, блокирующим сигнализацию S100A9 — чрезмерное разрастание стволовых и прогениторных клеток, а также перепроизводство миелоидных и В-клеток в значительной мере обращалось вспять. Иными словами, большая часть ущерба от потери SUCNR1 могла быть устранена путем прерывания петли тревоги S100A8/S100A9.
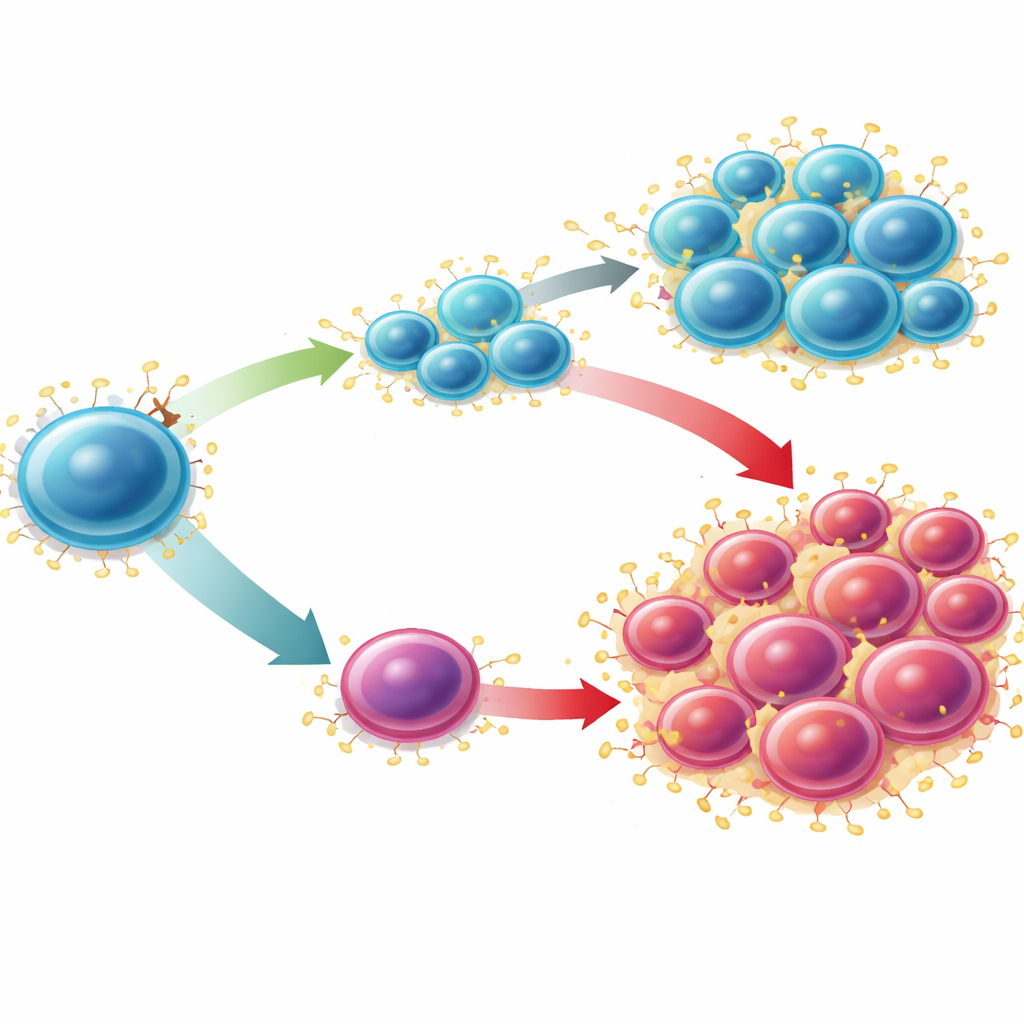
Преобразование уязвимости в терапевтическую стратегию
Учёные затем спросили, можно ли эту цепочку использовать в терапевтических целях при ОМЛ. В агрессивной мышиной форме лейкоза, вызванной мутацией MLL-AF9 — где уровни Sucnr1 очень низки — блокада S100A9 тасхинимодом, особенно в сочетании с мощным соединением, активирующим SUCNR1, уменьшала количество лейкемических стволоподобных клеток и снижала нагрузку болезни в костном мозге и селезёнке. Анализ данных одно-клеточной РНК от человеческих моделей ОМЛ, леченных цитарабином, показал, что устойчивые к лечению кластеры клеток были богаты на S100A8 и S100A9, тогда как SUCNR1 был редок и ассоциировался с другой, метаболически активной субпопуляцией, которая сократилась после лечения. В человеческих линиях лейкозных клеток активация SUCNR1 усиливала клеточную гибель, индуцируемую химиотерапией, и могла вызывать апоптоз сама по себе при сверхэкспрессии SUCNR1. Вместе эти результаты указывают на то, что низкий уровень SUCNR1 не только служит маркером плохого прогноза, но и представляет слабое место: лейкемические клетки, утратившие этот тормоз, могут сильно зависеть от оси S100A8/S100A9 и особенно чувствительны к стратегиям, восстанавливающим сигнализацию SUCNR1 или блокирующим последующую тревогу.
Новый рычаг для приручения лейкоза
Для непрофессионального читателя основная мысль такова: на первый взгляд банальный метаболический побочный продукт — сукцинат — и его рецептор SUCNR1 формируют неожиданную систему безопасности в кроветворении. Когда SUCNR1 присутствует и активен, он сдерживает стволовые клетки и предотвращает неконтролируемый рост. Когда SUCNR1 теряется или его уровень низок — как часто бывает у некоторых пациентов с ОМЛ — сукцинат и воспалительные тревожные белки, такие как S100A8 и S100A9, могут сдвинуть стволовые и прогениторные клетки в сторону чрезмерного разрастания и лейкоза. Комбинируя препараты, ослабляющие этот воспалительный сигнал, с агентами, восстанавливающими или имитирующими сигнализацию SUCNR1, возможно направить систему обратно к сбалансированному кроветворению и повысить эффективность существующей химиотерапии.
Цитирование: Cuminetti, V., Boet, E., Heugel, M. et al. Succinate receptor 1 restricts hematopoiesis and prevents acute myeloid leukemia progression. Nat Commun 17, 2403 (2026). https://doi.org/10.1038/s41467-026-68906-2
Ключевые слова: острый миелоидный лейкоз, рецептор сукцината, гемопоэтические стволовые клетки, метаболизм и рак, воспалительная сигнализация