Clear Sky Science · ru
Инженерные алкогольные оксидазы катализируют трансэстерификацию в водной среде без конкурирующей гидролизной реакции
Почему эта история про фермент важна
Многие повседневные продукты — от лекарств и пищевых ароматизаторов до биодизеля — зависят от простого типа химической связи, называемой эфирной. Эффективное, экономичное и экологичное создание и модификация таких эфиров — одна из ключевых задач «зелёной химии». Проблема в том, что вода, идеальный растворитель с точки зрения безопасности и устойчивости, обычно разрушает эти реакции, распадая эфиры так же быстро, как их получают. В этом исследовании показано, что инженерный фермент может собирать эфиры в воде, почти полностью игнорируя окружающую воду, что открывает путь к более чистым промышленным процессам.
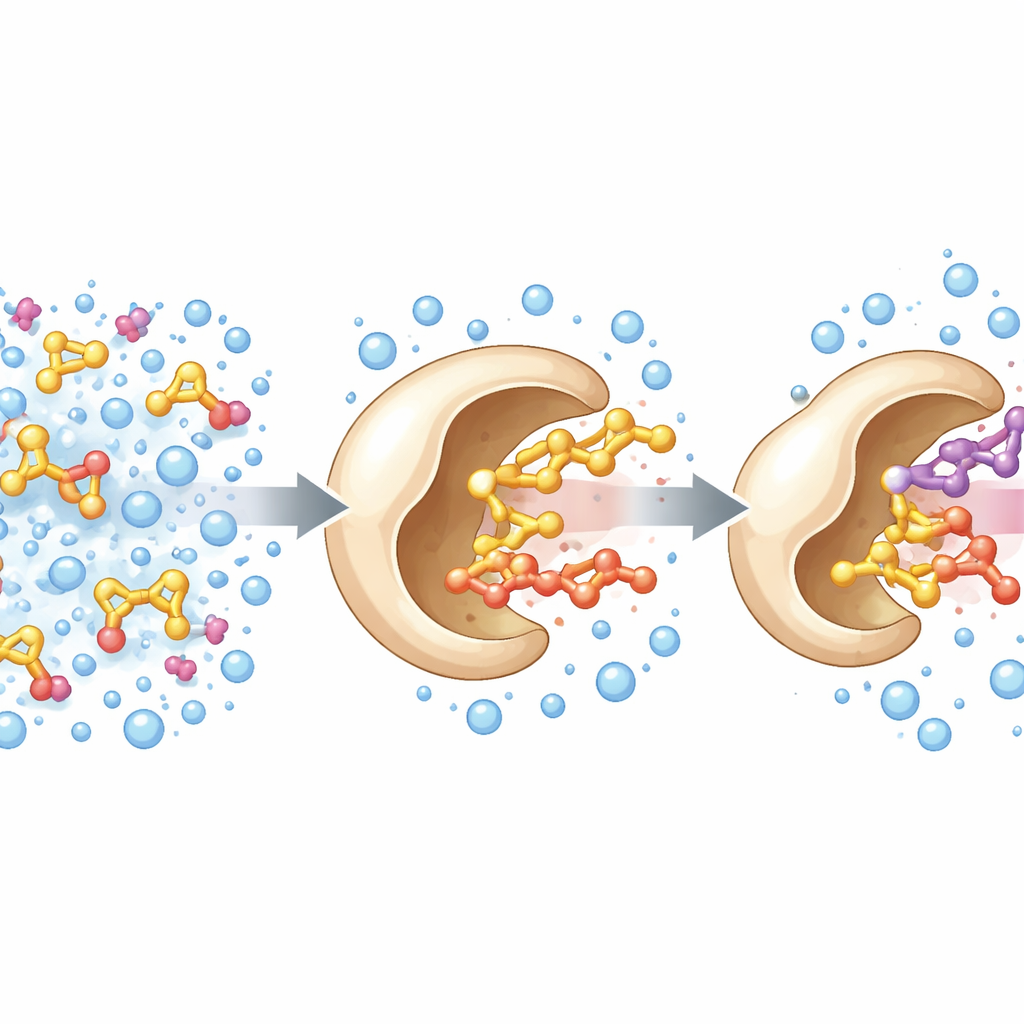
Переквалификация известного фермента
Исследователи начали с известного фермента — алкогольной оксидазы из древесноразрушающего гриба. В природе этот фермент использует флавиновый кофактор для забирания электронов у мелких спиртов, таких как метанол. Команда поставила цель расширить его способность работать с более объёмными спиртами, которые более актуальны для тонких химикатов и ароматов. Используя трёхмерную структуру фермента как дорожную карту, они сфокусировались на трёх аминокислотах, образующих своего рода вход в активный сайт. Случайно изменив эти позиции и отскринив полученные варианты, они обнаружили тройной мутант — названный PcAOx‑VPN — который эффективно превращал более крупные спирты, например бензиловый спирт, при значительной утрате исходной активности по отношению к мелким спиртам вроде метанола.
Неожиданный талант: сборка эфиров в воде
Во время тестов PcAOx‑VPN в смесях, предназначенных для растворения жирных субстратов, команда заметила дополнительные пики в аналитических данных. Эти пики оказались ацетилированными продуктами: фермент переносил ацильную группу от активированного эфирного донора на спирты — реакция, известная как трансэстерификация. Поразительно, что это происходило в водном буфере, где обычно доминирует конкурирующий гидролиз, при котором вода атакует и разрушает эфир. Здесь PcAOx‑VPN эффективно соединял спирты и ацильные доносы, такие как винилацетат, образуя новые эфиры, часто с выходами выше 80% и лишь незначительными побочными реакциями. Тот же фермент действовал на широкий спектр спиртов — предельных, ароматических, хиральных и содержащих сера — и в ряде случаев демонстрировал явное предпочтение одной энантиомерной формы над другой.
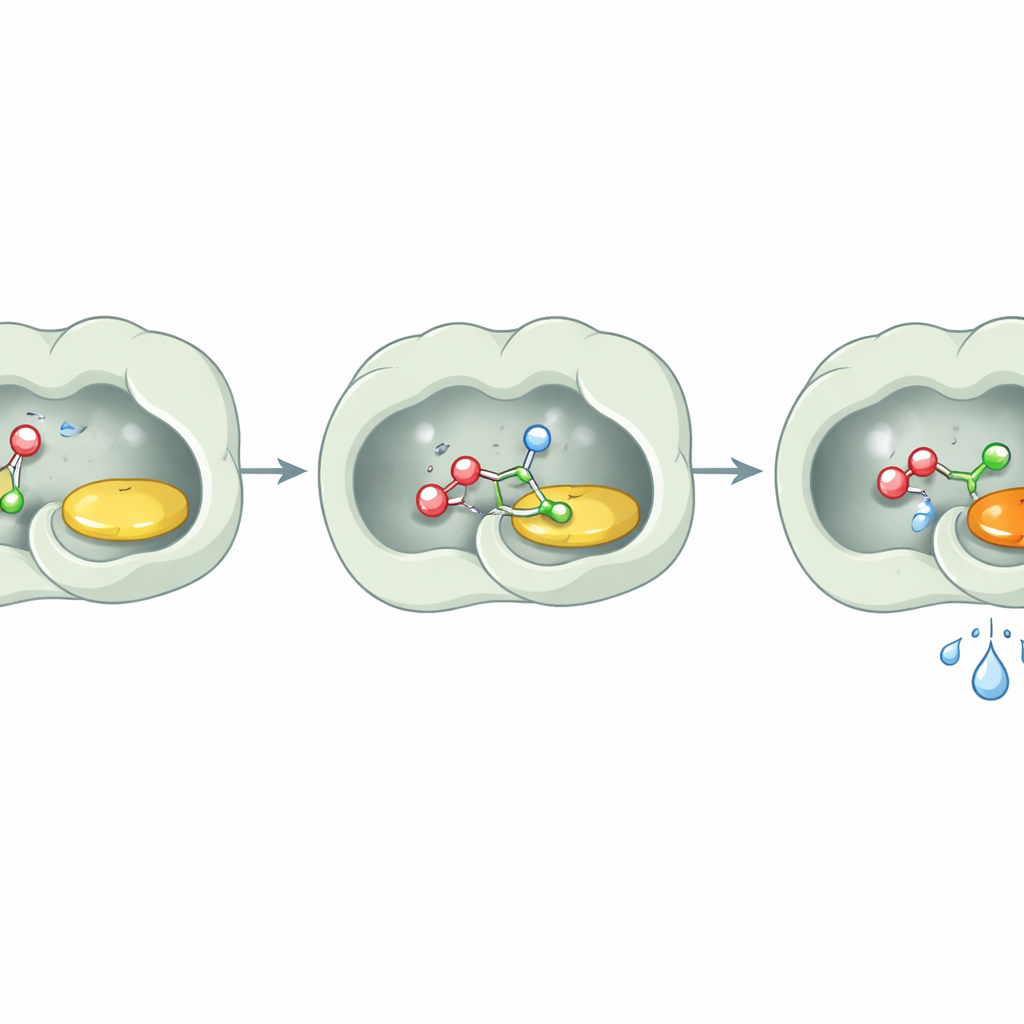
Как фермент не даёт воде помешать
Ключевым сюрпризом было то, чего фермент не делал: он практически не гидролизовал эфиры. Даже после длительного инкубирования с эфирными субстратами и водой PcAOx‑VPN оставлял их по существу нетронутыми, если только не добавлялся дополнительный ацильный донор. Структурные исследования дают простое объяснение. Активный сайт облицован в основном неполярными ароматическими аминокислотами, формирующими сильно гидрофобный карман. Детальный анализ не выявил молекул воды рядом с флавиновым кофактором, а вычислительные инструменты подтвердили, что канал, ведущий в активный сайт, также неблагоприятен для воды. По сути, фермент строит крошечную сухую «комнату» внутри водного мира: спирты и активированные эфиры могут войти и прореагировать, а молекулы воды остаются в стороне и не успевают разрушить продукт.
Как, вероятно, протекает реакция внутри
Механистические эксперименты и анализ мутантов показали, что две аминокислоты — гистидин и аспарагин — играют центральную роль как в естественной окислительной функции фермента, так и в его новой способности к трансэстерификации. Гистидин действует как основа, помогая отнять протон у входящего спирта и сделать его более нуклеофильным, тогда как аспарагин стабилизирует возникшее заряженное состояние. Вместе они способствуют атаке спирта на ацильный донор и образованию кратковременного интермедиата, который затем распадается с образованием желаемого эфира. Также необходим окисленный состояние флавинового кофактора: в бескислородных условиях, когда флавин восстановлен, трансэстерификация останавливается и возобновляется только при возвращении воздуха. Примечательно, что при внесении той же тройки мутаций в родственные оксидазы из других грибов эти ферменты также приобрели выраженную трансэстерификационную активность, что указывает на возможность обобщения этого поведения.
Что это означает для более экологичной химии
Для неспециалистов главный вывод таков: авторы научили известный фермент новому трюку — синтезировать полезные эфиры прямо в воде, эффективно игнорируя склонность воды разрушать продукт. Выделив внутри белка сухой, благоприятный для неполярных молекул карман и настроив несколько ключевых аминокислот, они создали катализатор, который предпочитает спирты вместо воды в качестве реакционных партнёров. Поскольку тот же принцип проектирования работает в родственных ферментах, этот подход может быть распространён на семейство катализаторов для производства ароматов, отдушек, тонких химикатов и, возможно, биотоплива в более безопасных и устойчивых процессах, где меньше применяются жёсткие органические растворители, а больше — вода.
Цитирование: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Ключевые слова: инженерия ферментов, биотрансформация, зелёная химия, синтез эфиров, флавопротеины