Clear Sky Science · ru
Ингибирование сигнальной передачи TGF-β в микроглии стимулирует взрослую нейрогенез в гиппокампе и снижает поведение, похожее на тревогу, у взрослых мышей
Почему иммунные клетки мозга важны для настроения и памяти
Большинство из нас думают об иммунных клетках как о патрулях по телу, а не как о факторах, формирующих наши мысли и чувства. Это исследование оспаривает такое мнение, показывая, что микроглия — иммунные клетки, обитающие в мозге — может значительно влиять на рождение новых нейронов в гиппокампе, области, важной для памяти и эмоций. Отключив в микроглии взрослой мыши конкретный сигнальный путь, исследователи усилили образование и выживаемость новых нейронов и зафиксировали изменения в поведении, связанного с тревогой.
Тихий питомник мозга для новых нейронов
У взрослых млекопитающих новые нейроны продолжают рождаться в нескольких специализированных «питомниках». Один из важнейших — субгранулярная зона гиппокампа, которая помогает различать похожие воспоминания, поддерживает обучение и участвует в регулировании настроения. В норме многие из этих новорожденных клеток гибнут, не достигнув зрелости. Их число может увеличиваться или уменьшаться в ответ на физическую активность, обогащённую среду, стресс, инсульт или эпилепсию. Микроглия постоянно обследует эту среду, но до сих пор оставалось неясным, способствует ли её реактивное, «воспалённое» состояние взрослой нейрогенезе или, наоборот, вредит ей.
Выключение ключевого «тормоза» в микроглии
Группа сосредоточилась на сигнальном молекуле TGF‑β, которая обычно удерживает микроглию в спокойном, гомеостатическом состоянии. Используя генетически модифицированных мышей, они избирательно нарушили передачу сигнала TGF‑β в микроглии у взрослых животных — либо удаляя сам лиганд TGF‑β, либо рецепторы (ALK5 или TβRII), которые его распознают. Это перевело микроглию в реактивный, провоспалительный профиль без массовой гибели нейронов. В таком состоянии число микроглиальных клеток увеличивалось и менялась их форма, что указывало на активацию, тогда как соседние вспомогательные клетки — астроциты — в основном оставались без изменений.
Больше новых нейронов, лучшее выживание и изменённая тревожность
При отключении сигнальной передачи TGF‑β в микроглии гиппокамп выдал волну незрелых нейронов, отмеченных белком DCX. Этот всплеск появлялся примерно через три недели после генетического переключения и приводил к длительному увеличению числа полностью зрелых нейронов через несколько недель. Точное отслеживание делящихся клеток показало, что основной эффект заключался в улучшении выживания новорожденных нейронов, а не просто в ускорении деления. Полное удаление микроглии с помощью препарата не воспроизводило этого эффекта, что указывает на то, что важно не отсутствие микроглии, а конкретный реактивный профиль, возникающий при подавлении TGF‑β. В поведении мыши с дефицитом TGF‑β в микроглии проводили больше времени в открытых ветвях возвышенных лабиринтов — обычный признак снижения тревожного поведения или разряжения поведения. Эти изменения исчезали, когда в некоторых моделях микроглия возвращалась к более нормальному состоянию, но сохранялись в других моделях, где микроглия оставалась реактивной.
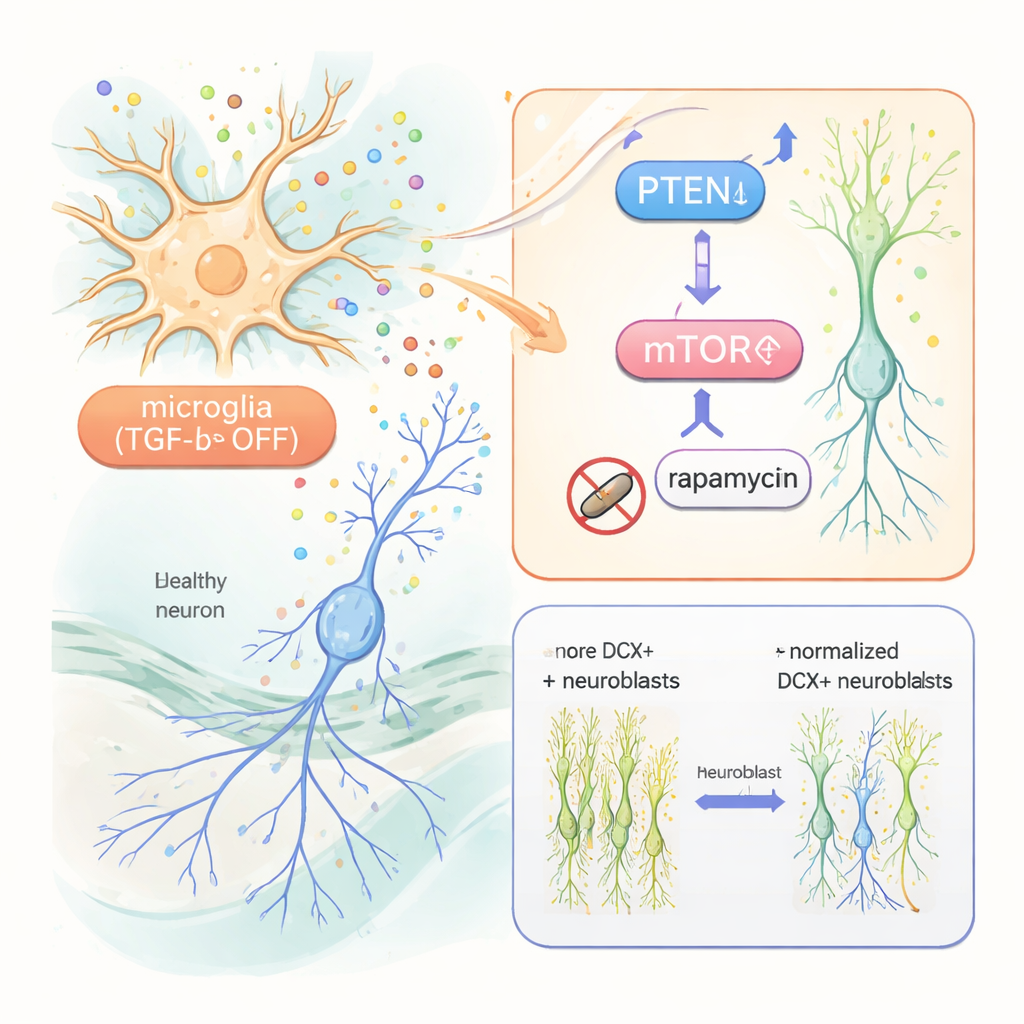
Выявление пути внутри новорожденных нейронов
Чтобы понять, как изменённая микроглия общается с новорожденными нейронами, исследователи использовали одноклеточный РНК‑секвенирование клеток гиппокампа. Они обнаружили широкие изменения активности генов не только в микроглии, но и в незрелых нейронах. Среди ключевых изменений — снижение уровня PTEN, белка, который обычно сдерживает рост клеток, и признаки повышенной активности пути mTOR, который способствует выживанию и росту клеток. Интересно, что хорошо известные факторы роста, такие как IGF‑1 и TNF‑α, хотя и были повышены в реактивной микроглии, оказались не обязательными: даже при их генетическом удалении усиление нейрогенеза сохранялось. Напротив, когда мышей лечили рапамицином, препаратом, блокирующим mTOR, избыток незрелых нейронов и их чрезмерная ветвистость возвращались к норме. Новорождённые нейроны также демонстрировали повышенные уровни маркера mTOR‑сигнализации ниже по цепочке, который снижался под действием рапамицина.
Что это может значить для здоровья мозга
В совокупности результаты указывают на то, что при отключении сигнальной передачи TGF‑β в микроглии эти клетки переходят в реактивное состояние, которое через путь PTEN–mTOR внутри новорожденных нейронов способствует их выживанию и интеграции в гиппокамп. Это, в свою очередь, связано со снижением тревожного поведения у мышей, хотя может сопровождаться изменениями в обучении и памяти. Для неспециалиста ключевое сообщение таково: собственные иммунные клетки мозга способны точно регулировать, сколько новых нейронов присоединяется к цепям памяти — и аккуратная модуляция этой системы в будущем может помочь усиливать полезный нейрогенез или сдерживать вредное чрезмерное разрастание нейронов при состояниях вроде эпилепсии или после травмы мозга.
Цитирование: Ware, K., Peter, J., Yazell, J. et al. Inhibition of TGF-β signaling in microglia stimulates hippocampal adult neurogenesis and reduces anxiety-like behavior in adult mice. Nat Commun 17, 1440 (2026). https://doi.org/10.1038/s41467-026-68885-4
Ключевые слова: взрослая нейрогенез, микроглия, гиппокамп, тревожное поведение, сигнальная передача TGF-бета