Clear Sky Science · ru
Посттрансляционная адаптация к голоданию, опосредованная PRMT3, регулирует метаболическую гибкость
Почему важно время приёма пищи и источник топлива в организме
Многие люди пробуют голодание или питание с ограниченным окном приёма пищи, чтобы похудеть или улучшить уровень сахара в крови, но результаты часто бывают непредсказуемыми. В этом исследовании заглядывают внутрь нашей метаболической «кухни», чтобы понять почему. Фокусируясь на брюшном жире у мышей и на образцах человека, учёные обнаружили молекулярный переключатель, который помогает жировой ткани решать, сжигать ли топливо или запасать его, и показали, как и время приёма пищи, и препарат могут переключать этот механизм в сторону улучшения здоровья.
Гибкий двигатель внутри нашего жира
Наш организм лучше всего функционирует, когда умеет плавно переключаться между сжиганием жира в период голода и сжиганием сахара после приёма пищи. Эта «метаболическая гибкость» часто теряется при ожирении, что затрудняет адаптацию к колебаниям энергетического предложения и спроса. Команда изучала висцеральный белый жир — глубоко расположенный брюшной жир, сильно связанный с диабетом и сердечными заболеваниями — и обнаружила, что специфические химические метки на белках, называемые метильными группами, меняются в зависимости от приёма пищи и голодания. У мышей и у людей две такие метки, MMA и ADMA, накапливаются в висцеральном жире с ростом массы тела и индекса массы тела, что указывает на их связь с вялым, менее приспособляемым обменом веществ.
Сигнал кормления, который «жёстко» фиксирует метаболизм
Исследователи сосредоточились на ферменте в жировых клетках под названием PRMT3, который добавляет эти метильные метки. У мышей уровень PRMT3 в висцеральном жире повышается ночью, когда животные питаются, и падает днём во время голодания, тесно повторяя динамику MMA и ADMA. Этот ритм зависит от инсулина и ключевого сигнального белка AKT: когда пища или введённый инсулин активируют AKT, PRMT3 включается и становится более модифицированным, что в свою очередь увеличивает количество метилированных белков. Блокирование AKT или прямое ингибирование PRMT3 быстро сглаживает этот сигнал метилирования, имитируя эффект более длительного голодания.
Перенастройка жировых клеток от запасания к сжиганию
Что делает эта химическая маркировка на практике? В исследовании показано, что PRMT3 стабилизирует транспортерный белок SLC25A1 в митохондриях — энергетических станциях клетки. SLC25A1 выводит цитрат, ключевой метаболический промежуточный продукт, из митохондрий в цитоплазму, где он участвует в синтезе нового жира. PRMT3 метилирует два специфических аргининовых участка на SLC25A1, делая транспортер более стабильным и способствуя выносу цитрата и образованию жира. При блокировке PRMT3 уровень SLC25A1 падает, вынос цитрата снижается, и жировые клетки переключаются на расщепление сахара вместо синтеза жира. У мышей на высокожировой диете препарат, блокирующий PRMT3, уменьшает жировую массу, улучшает контроль глюкозы и повышает показатель респираторного коэффициента, что показывает более лёгкое переключение животных на сжигание углеводов.
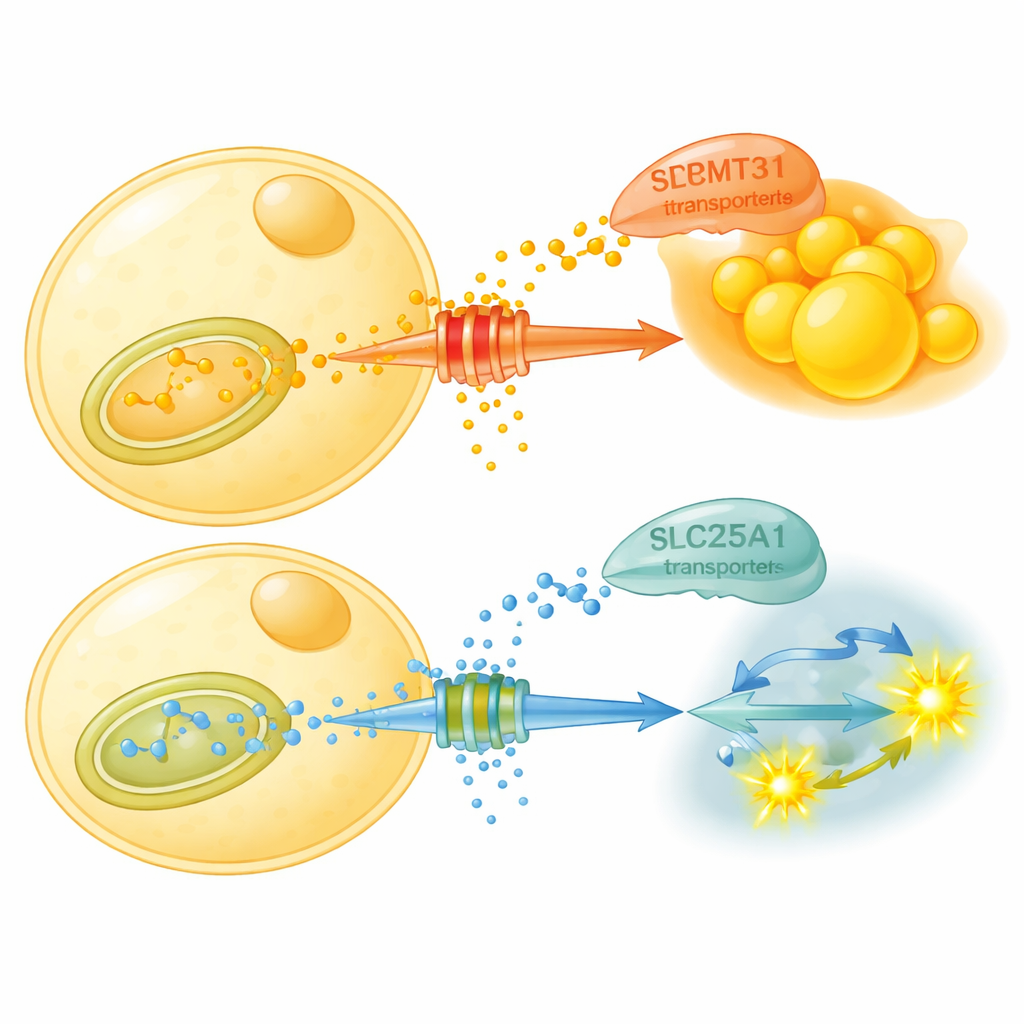
Графики голодания и генетические модификации указывают на один путь
Далее учёные задали вопрос, используют ли обычные схемы голодания тот же самый переключатель. При режиме 16:8 — 16 часов голодания и 8 часов приёма пищи — мыши теряли вес и лучше справлялись с глюкозой, не сокращая общий объём потребляемой еды. В их висцеральном жире снижались уровни PRMT3, SLC25A1 и метилированных белков, а использование топлива становилось более гибким, особенно ночью, когда они обычно едят. Парадоксально, что введение препарата, блокирующего PRMT3, в определённое время суток давало многие из тех же преимуществ, что и режим 16:8. Генетическое удаление SLC25A1 только в жировых клетках также защищало мышей от диет-индуцированной гипергликемии и стеатоза печени, опять же за счёт усиления расщепления сахара и энергетического расхода в жире, даже без заметного уменьшения жировой массы.
Что это значит для будущих терапий
В целом полученные данные свидетельствуют о том, что глубокий брюшной жир содержит чувствительный ко времени переключатель, контролируемый инсулином, AKT, PRMT3 и SLC25A1, который определяет, останется ли наш метаболизм подвижным или застрянет в режиме накопления. Ограничение времени приёма пищи, по-видимому, смещает этот переключатель в сторону гибкости, снижая активность PRMT3 и его эффекты по каскаду. Препарат, ингибирующий PRMT3, способен воспроизвести многие из этих преимуществ у ожиревших мышей, что намекает на возможное будущее средство, делающего метаболические выгоды голодания более доступными. Для обычных читателей основной вывод таков: важно не только что мы едим, но и когда мы едим — это способ изменить то, как жировая ткань обращается с топливом, с важными последствиями для веса, уровня сахара в крови и долгосрочного здоровья.
Цитирование: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
Ключевые слова: метаболическая гибкость, ограниченное по времени питание, висцеральный жир, метилирование белков, метаболизм глюкозы