Clear Sky Science · ru
Наноустройство на основе ДНК распознаёт пуринергическую сигнализацию и переключает иммунитет для разрешения воспаления
Уменьшение «сигнализации тревоги» в организме
Когда тканям причиняют повреждение, клетки выбрасывают вспышку химических «сигналов тревоги», которые привлекают иммунные клетки для борьбы с инфекцией и удаления мусора. Эта реакция жизненно важна, но если сигнал тревоги звучит слишком громко или слишком долго, это может приводить к разрушительному воспалению в лёгких, почках и других органах. В этом исследовании описано крошечное программируемое наноустройство на основе ДНК, которое распознаёт, когда сигнал тревоги чрезмерен, и тихо его ослабляет, помогая иммунной системе переключиться с атакующего режима на режим заживления.
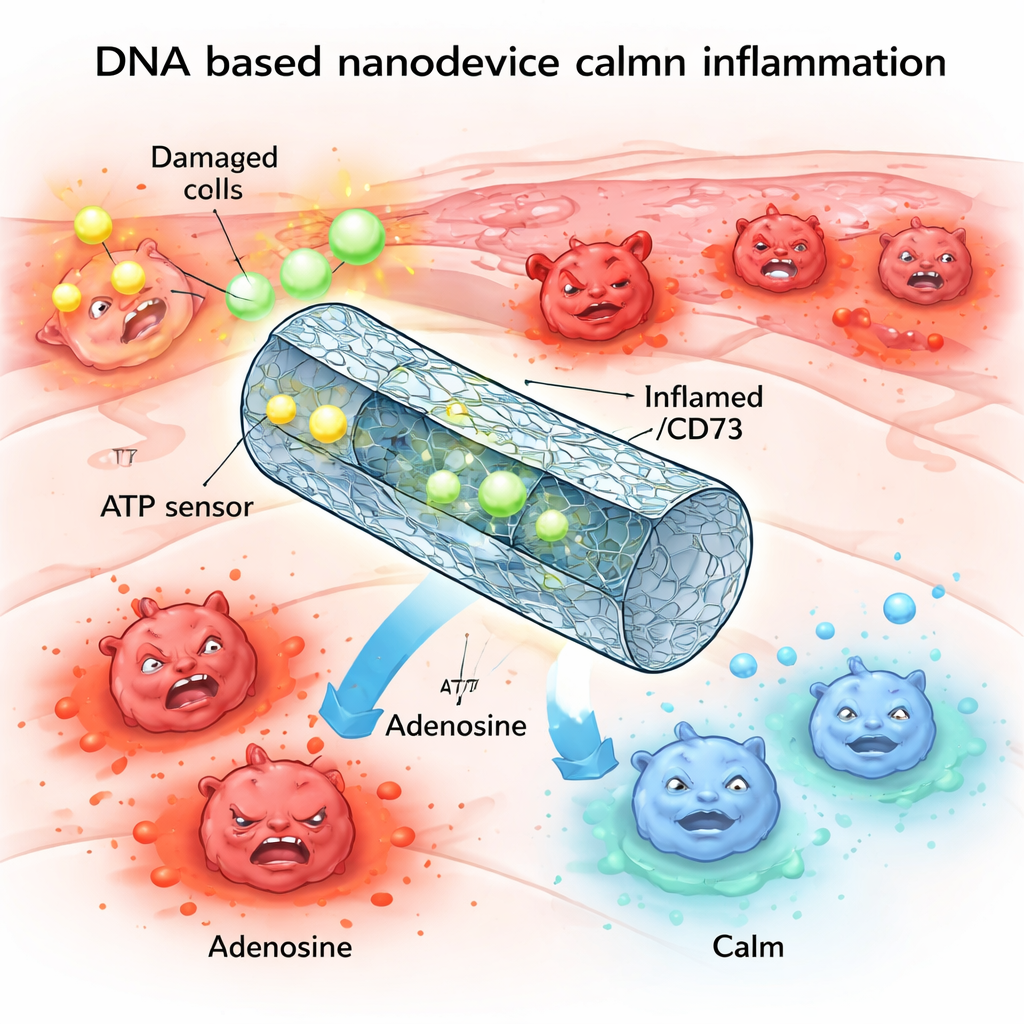
Химическая тревога, которая может выйти из-под контроля
Одна из ключевых молекул‑тревог в организме — АТФ, лучше известная как «валюта энергии» внутри клеток. При повреждении или стрессе большое количество АТФ просачивается из повреждённых клеток в окружающее пространство. Там внеклеточный АТФ действует как сигнал бедствия, связываясь с рецепторами на иммунных клетках и стимулируя их к выраженному воспалительному состоянию. В нормальных условиях ферменты на поверхности клеток быстро расщепляют избыток АТФ до аденозина — родственной молекулы с успокаивающим, противовоспалительным эффектом. Но при многих хронических или тяжёлых воспалительных заболеваниях этот механизм расщепления нарушается: уровень АТФ остаётся высоким, аденозина мало, и ткани застревают в порочном круге повреждения.
Создание «умной» ДНК‑трубки
Исследователи поставили цель имитировать и исправить эту природную систему контроля с помощью ДНК‑нанотехнологий. Они собрали полую трубку из ДНК, сложенную наподобие оригами, и оснастили её двумя основными компонентами: «сенсорами», распознающими АТФ, и ферментами, превращающими АТФ в аденозин. В состоянии покоя трубка заперта короткими ДНК‑фрагментами, которые одновременно служат датчиками АТФ. Когда уровень АТФ поднимается выше определённого порога, характерного для повреждённых тканей, АТФ связывается с этими фрагментами, заставляя трубку открыться и обнажая внутри ферменты ENPP1 и CD73. Те затем расщепляют избыток АТФ и производят аденозин, мягко смещая местный химический баланс от опасности к разрешению воспаления.
Доказательство работоспособности переключателя
В контролируемых лабораторных тестах команда подтвердила, что их ДНК‑трубка остаётся закрытой при низких уровнях АТФ, но надёжно открывается при избытке АТФ, подобно аварийному клапану. После разблокировки устройство последовательно преобразует АТФ в промежуточные продукты и в конечном счёте в аденозин, не нарушая заметно активности ферментов. В иммунных клетках, подвергнутых действию высокого АТФ, это наноустройство снижало токсичные побочные продукты в митохондриях, уменьшало активацию воспалительных путей, таких как NF-κB и инфламмасома NLRP3, и усиливало сигналы, связанные с успокаивающими действиями аденозина. Иными словами, устройство делало больше, чем просто удаляло АТФ: оно активно перенастраивало поведение клеток с воспалительного на регуляторное.
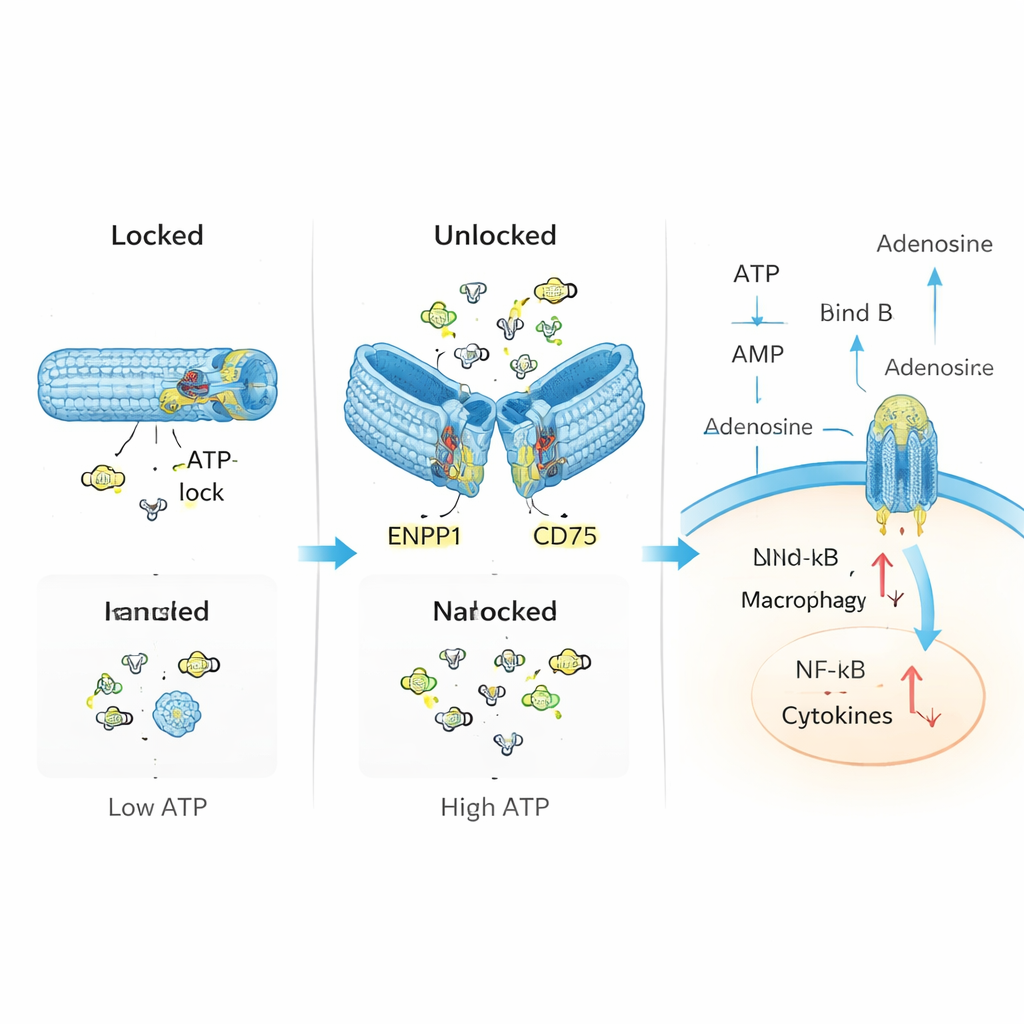
Доставка к местам повреждения
Разработать умный переключатель — одно, доставить его в нужное место в организме — другое. Для решения этой задачи исследователи прикрепили свои ДНК‑трубки к поверхности циркулирующих моноцитов, типа лейкоцита, который естественно направляется в воспалённые ткани. С помощью холестерин‑связанного ДНК‑якоря они «припарковали» большое количество наноустройств на мембране каждой клетки, где устройства в основном оставались на поверхности, а не поглощались клеткой. В мышиных моделях острой травмы лёгких и почек эти украшенные моноциты накапливались в повреждённых органах намного эффективнее, чем свободные устройства, при этом наноустройства сохраняли способность специфически реагировать на высокий АТФ в поражённых тканях.
Содействие заживлению тканей
У мышей с химически вызванными повреждениями лёгких или почек лечение ДНК‑устройством уменьшало повреждение тканей, скопление иммунных клеток и уровень провоспалительных медиаторов. Версия, переносимая моноцитами, работала лучше всего, обеспечивая более надежную защиту, чем свободное устройство или одни только ферменты. Более глубокие генетические и метаболические анализы лёгочной ткани показали, что этот подход не только подавляет воспалительные гены, но и помогает восстановить нарушенный энергетический метаболизм в клетках. Важно, что устройства продемонстрировали низкую токсичность и не вызывали вредных иммунных реакций у здоровых животных.
Почему это важно для будущих терапий
Для неспециалиста ключевая мысль такова: эта работа демонстрирует программируемый молекулярный «термостат» для воспаления. Построенное из ДНК и природных ферментов наноустройство распознаёт, когда сигнал опасности избыточен, и автоматически превращает его в успокаивающий сигнал, помогая иммунным клеткам отступить и тканям восстановиться. Хотя метод всё ещё находится на ранней экспериментальной стадии, эта стратегия предлагает новый класс терапий, которые не просто повсеместно блокируют иммунные пути, а локально восстанавливают баланс химических сигналов в местах повреждения, потенциально обеспечивая точный контроль над вредным воспалением при многих заболеваниях.
Цитирование: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
Ключевые слова: ДНК-наноустройство, внеклеточный АТФ, воспаление, аденозиновая сигнализация, наномедицина