Clear Sky Science · ru
Анти-TLR2 иммунотерапия модулирует перенос α-синуклеина от нейронов к олигодендроцитам в моделях мыши и человека
Почему это исследование важно
Множественная системная атрофия (МСА) — редкое, но быстро прогрессирующее заболевание мозга, сочетающее паркинсонизм с нарушениями равновесия и вегетативной функции, например падениями артериального давления. Врачи могут облегчать симптомы, но пока не умеют замедлять само заболевание. В этом исследовании показано, как неправильно свернутая белковая молекула распространяется между клетками мозга и повреждает «изоляцию проводки» мозга, а также продемонстрировано, что таргетная антителозависимая терапия может прервать этот процесс в животных и клеточных моделях. Работа указывает на реальную, фармакологически реализуемую стратегию, которая со временем может изменить течение МСА, а не только лечить ее симптомы.
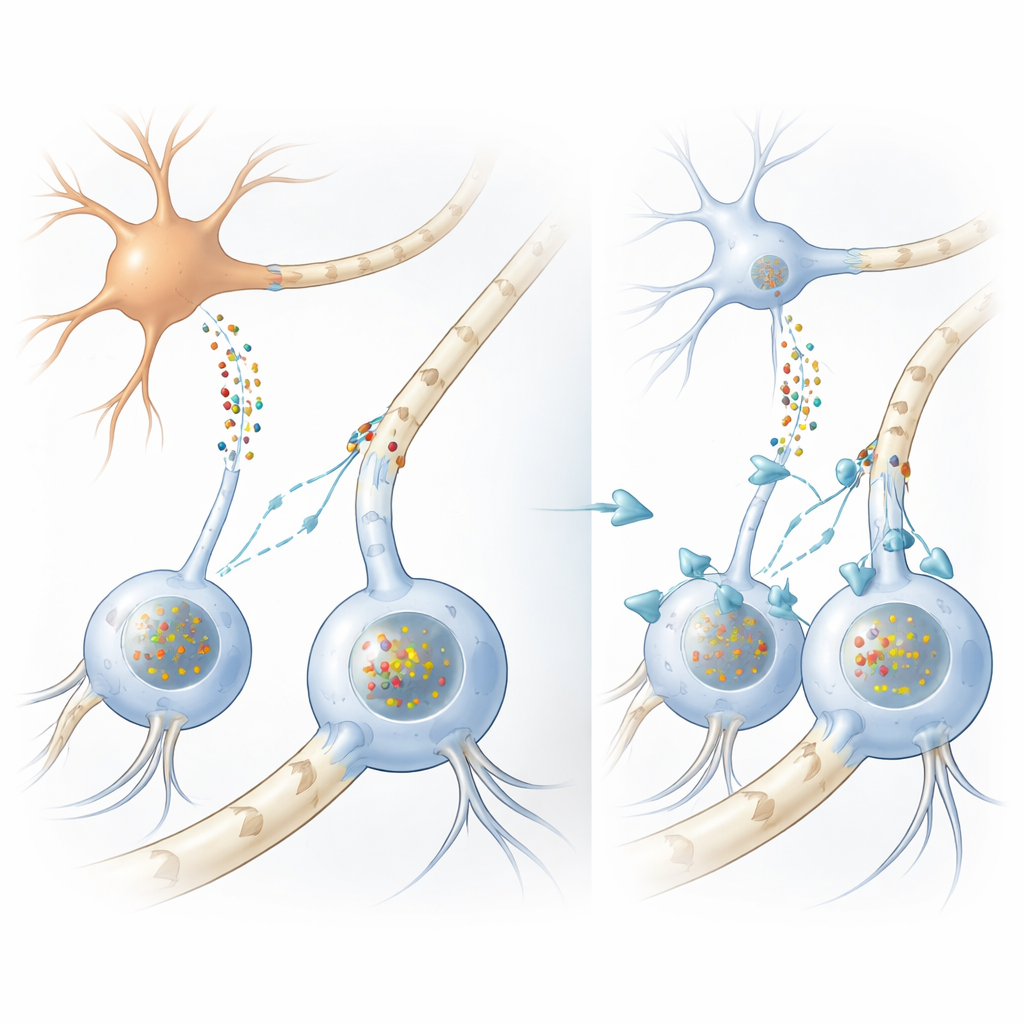
Как нарушается проводимость мозга
При многих двигательных расстройствах, включая болезнь Паркинсона, в нейронах накапливаются скопления белка под названием альфа-синуклеин. Однако при МСА наиболее впечатляющие скопления образуются в вспомогательных клетках — олигодендроцитах, которые обычно оборачивают нервные волокна жировыми миелиновыми оболочками, ускоряющими передачу электрических сигналов. Странно, что сами олигодендроциты почти не синтезируют альфа-синуклеин, что долгое время оставляло загадку: откуда в этих клетках берутся массивные белковые отложения? Авторы сначала подтвердили на образцах человеческого мозга и при масштабных анализах РНК, что олигодендроциты действительно производят гораздо меньше альфа-синуклеина, чем нейроны, что усиливает идею о внешнем происхождении вредного белка.
Белок передаётся от нейрона к вспомогательной клетке
Чтобы проверить это, команда создала несколько дополняющих друг друга моделей. В культурах они вырастили подобные человеческим олигодендроциты из нейральных стволовых клеток и выдерживали их в среде, собранной из клеток-нейроноподобных линий, генетически запрограммированных выделять большое количество альфа-синуклеина. Вспомогательные клетки поглощали этот белок и формировали включения, очень похожие на глиальные включения, обнаруживаемые в мозге пациентов с МСА, включая те же химические метки и шаперонные белки. Когда исследователи изучали мышиную линию, продуцирующую человеческий мутантный альфа-синуклеин только в нейронах, они вновь находили человеческие белковые скопления внутри олигодендроцитов в белом веществе, несмотря на то что эти клетки не экспрессировали человеческий ген. В совокупности эти эксперименты показывают, что альфа-синуклеин может переходить из нейронов в олигодендроциты и образовывать там патологические включения.
«Ворота» на поверхности клетки
Далее учёные задали вопрос, как белку удаётся проникать в олигодендроциты. Предыдущие работы выявили иммунный сенсор Toll-подобный рецептор 2 (TLR2) на поверхности клеток как точку прикрепления альфа-синуклеина в нейронах и микроглии. Анализируя наборы данных экспрессии генов из мозгов пациентов с МСА, команда обнаружила, что олигодендроциты у больных несут необычно высокий уровень TLR2 по сравнению с контролем, а повышенный TLR2 был связан с пониженной экспрессией генов, связанных с миелином, таких как белок миелина (MBP). Эта зависимость не проявлялась в нескольких независимых наборах данных по болезни Паркинсона, что даёт основание полагать: чувствительность олигодендроцитов к альфа-синуклеину через TLR2 — отличительная черта МСА, а не универсальное свойство всех синуклеинопатий.
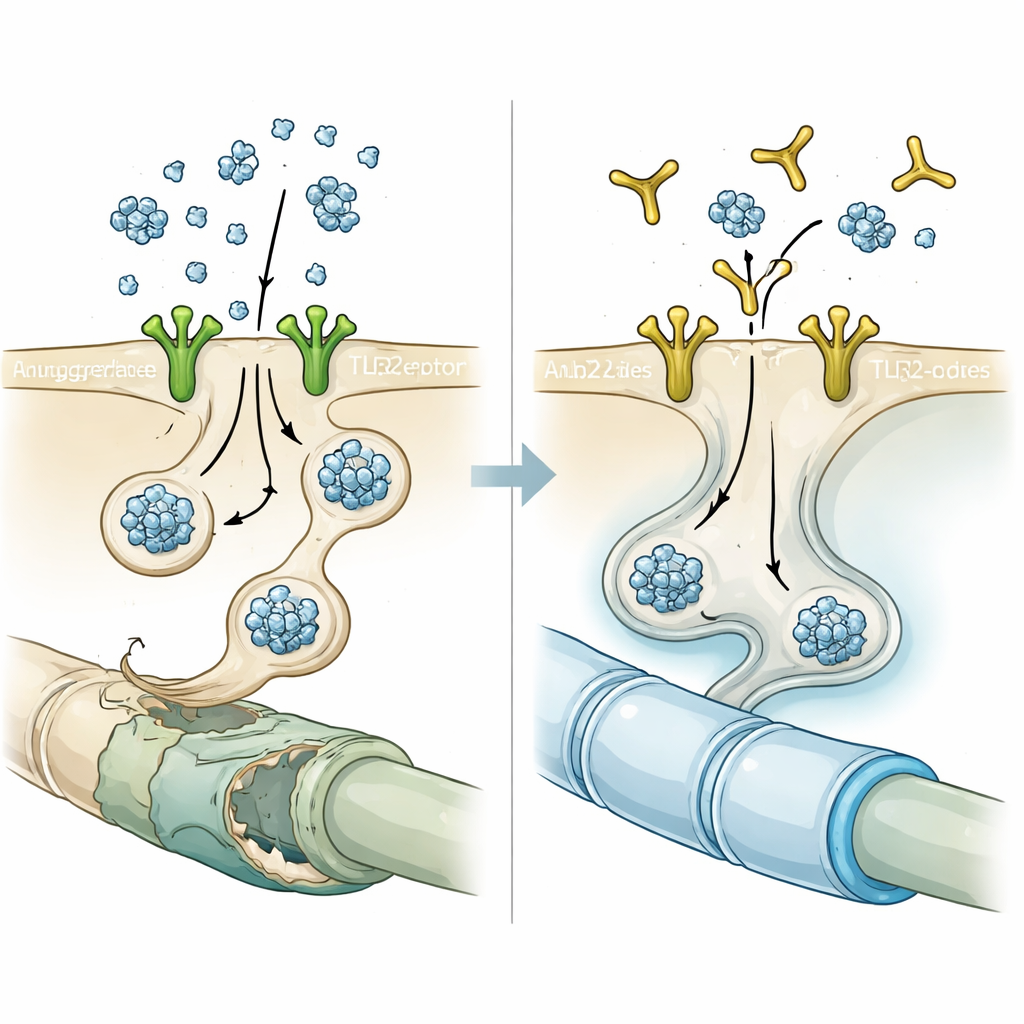
Блокирование «ворот» антителом
Опираясь на эту подсказку, исследователи испытали NM-101 — антитело, созданное для связывания с TLR2 и предотвращения его активации. В клеточных культурах краткая предобработка олигодендроцитов NM-101 перед добавлением нейронопроизводного альфа-синуклеина резко уменьшала количество и интенсивность включений. У мышей, либо сверхэкспрессирующих нейрональный альфа-синуклеин, либо получавших инъекции предварительно сформированных фибрилл альфа-синуклеина, еженедельные инфузии NM-101 снижали агрегированный белок в белом веществе, ослабляли воспалительную реакцию микроглии и астроцитов и уменьшали активацию воспалительного фермента каспазы-1 внутри олигодендроцитов. Лечёные животные жили дольше и показывали лучшие результаты в моторных тестах, что говорит о функциональной значимости защитного эффекта антитела, а не о его чисто микроскопическом проявлении.
Восстановление повреждённой изоляции
Поскольку олигодендроциты отвечают за образование миелина, команда проверила, повреждает ли перенос альфа-синуклеина миелин и может ли блокада TLR2 помочь. Секвенирование РНК по отдельным клеткам олигодендроцитов, полученных от человека и подвергнутых воздействию нейронно обусловленного альфа-синуклеина, выявило широкие сдвиги: снижение зрелого, миелинпродуцирующего состояния и смещение в сторону более незрелого, прогениторного профиля с пониженной активностью многих ключевых генов миелина. Параллельные исследования экспрессии генов в лазерно-захваченных олигодендроцитах от пациентов с МСА и от мышиной модели показали общую подпись — снижение экспрессии генов, участвующих в образовании и поддержании миелина. Под электронным микроскопом белое вещество у мышей с альфа-синуклеином демонстрировало более тонкие и дезорганизованные миелиновые оболочки. Лечение NM-101 обратило многие из этих изменений: миелин утолщался, восстанавливались уровни миелиновых белков и нормализовалась экспрессия генов, необходимых для созревания олигодендроцитов.
Что это значит для будущих терапий
Исследование подтверждает ясный сценарий: при МСА альфа-синуклеин, производимый нейронами, может распространяться в олигодендроциты через TLR2 на их поверхности, где он накапливается, запускает воспаление, нарушает программу развития клеток и разъедает миелиновое покрытие «проводки» мозга. Блокируя TLR2 с помощью таргетного антитела, исследователи смогли разорвать эту цепочку событий в мышиных и человеческих клеточных моделях, сократив токсические включения, подавив воспаление, восстановив миелин и улучшив выживаемость и моторную функцию. Хотя сам NM-101 ещё требует тщательной проверки в клинических исследованиях, работа выделяет TLR2-зависимый перенос белка как центральный драйвер патологии, сходной с МСА, и подчёркивает анти-TLR2 иммунотерапию как перспективную стратегию для замедления или предотвращения этого разрушительного заболевания.
Цитирование: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Ключевые слова: множественная системная атрофия, альфа-синуклеин, олигодендроциты, повреждение миелина, иммунотерапия