Clear Sky Science · ru
Подготовка против распространения: различные иммунные эффекты радиофармацевтических препаратов, испускающих альфа‑ и бета‑частицы, в сочетании с ингибированием контрольных точек иммунитета у мышей
Превращая радиацию в союзника иммунитета
Онкологи всё чаще пытаются привлечь иммунную систему к борьбе с опухолями, но многие виды рака по‑прежнему игнорируют или противостоят этим препаратам. В этом исследовании поставлен своевременный вопрос: можно ли разные виды таргетной радиации использовать не только для прямого уменьшения опухоли, но и чтобы «обучить» иммунную систему работать лучше — и влияет ли выбор радиоактивного препарата на характер такого обучения?
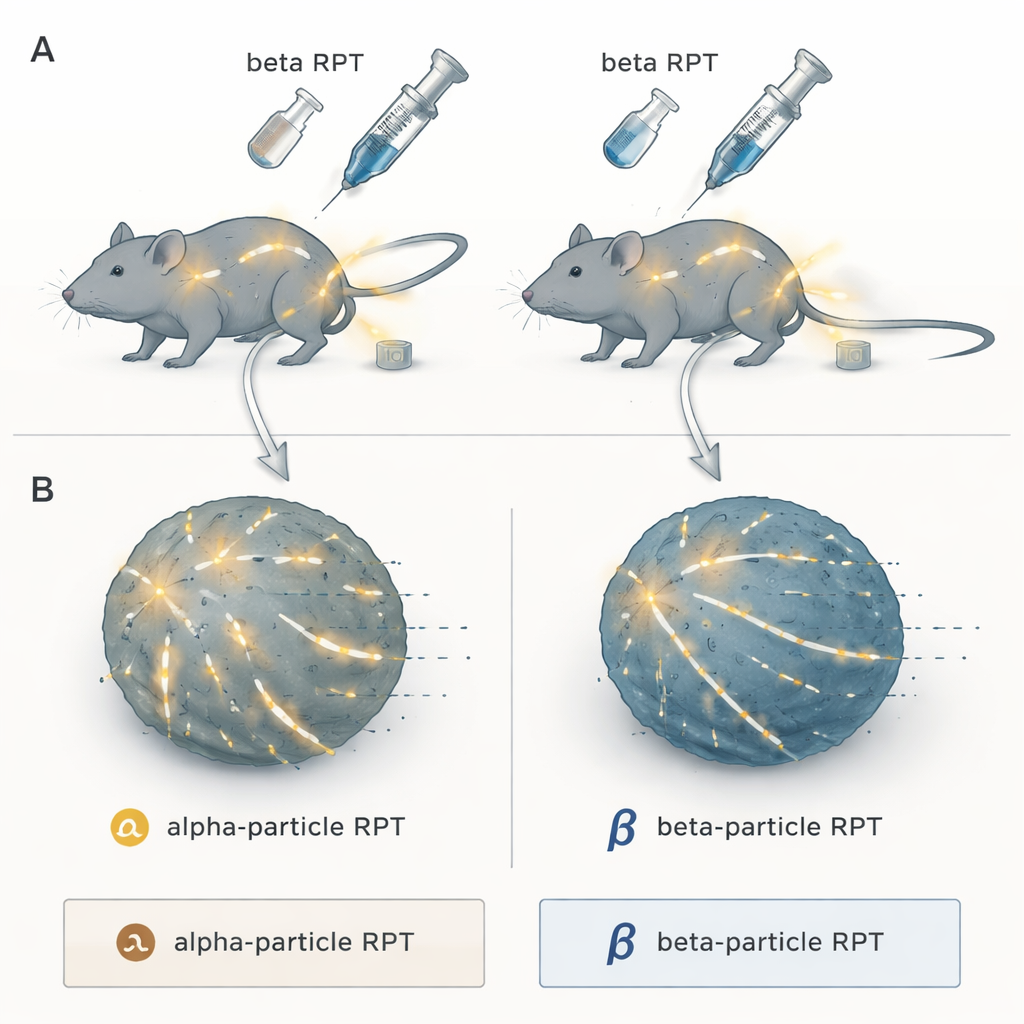
Два подхода к прицельной радиации
Исследователи сосредоточились на радиофармацевтической терапии — подходе «поиск‑и‑уничтожение», при котором радиоактивный груз прикреплён к молекуле, которая естественным образом нацеливается на опухоль. После введения она циркулирует по организму и доставляет радиацию к очагам рака в тех местах, где внешняя лучевая терапия справляется с трудом при распространённом заболевании. Команда сравнила две основные категории: испускатели альфа‑частиц, которые высвобождают чрезвычайно плотные всплески энергии на очень коротком расстоянии, и испускатели бета‑частиц, которые дают менее плотное излучение, простирающееся дальше в ткани. Во всех случаях радионуклиды были связаны с тем же опухоле‑ориентированным соединением NM600, так что различался только тип излучения, а не таргетирование.
Сочетание радиации с блокаторами контрольных точек
Сами по себе ингибиторы контрольных точек, такие как анти‑PD‑L1 и анти‑CTLA4, могут снять «тормоза» с иммунных клеток, но они наиболее эффективны, когда опухоль уже распознаётся иммунной системой. В мышиных моделях меланомы, рака простаты и колоректального рака учёные применяли тщательно подобранную низкую дозу радиации от NM600 либо на альфа‑, либо на бета‑основе, с комбинацией или без комбинации с ингибиторами контрольных точек. Они также варьировали время введения иммунных препаратов — до, вскоре после или значительно позже радиационной терапии — чтобы увидеть, как тайминг влияет на такие исходы, как рост опухоли, выживание и долговременная иммунная память.
Когда бета‑излучение эффективно: усиление существующего ответа
В «иммунно‑горячей» модели колоректального рака, которая изначально реагирует на иммунотерапию, лучшие результаты показало NM600 с бета‑излучателем, особенно при раннем или промежуточном начале терапии ингибиторами. Опухоли уменьшались сильнее, мыши жили дольше, а вылеченные животные часто отвергали ту же опухоль при её повторном введении через несколько месяцев. Детальное иммунное профилирование показало, что бета‑терапия в сочетании с блокадой контрольных точек не столько создаёт новый ответ, сколько усиливает уже существующий: расширяется популяция опухоле‑специфичных киллерных Т‑клеток, они становятся более активными и вырабатывают больше сигнальной молекулярной активности. Кратко: бета‑излучатели отлично подходят для распространения и усиления текущего иммунного ответа.
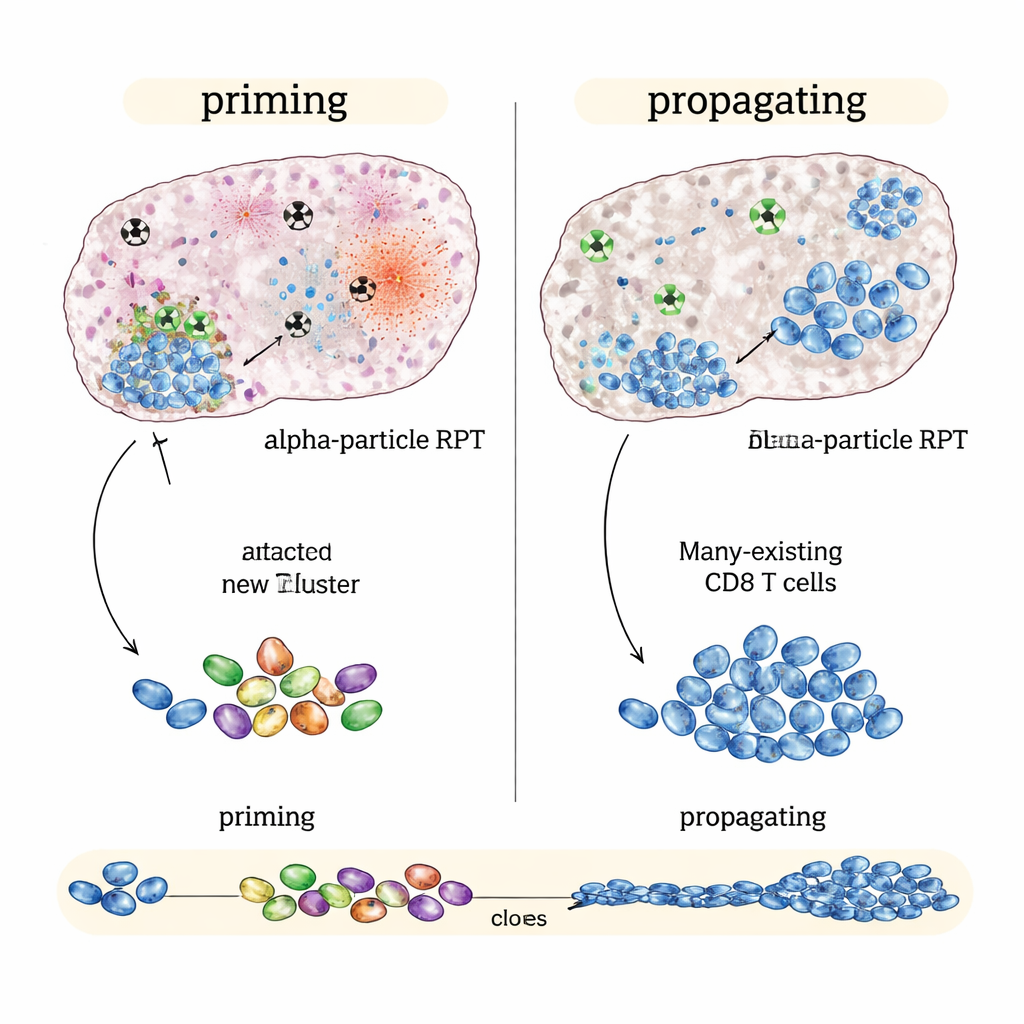
Когда альфа‑излучение эффективно: разжигание нового иммунного ответа
Напротив, в «иммунно‑холодных» опухолях, таких как модель меланомы и модель рака простаты, которые слабо реагируют на одни только ингибиторы контрольных точек, альфа‑вариант показал лучшую эффективность при той же средней дозе в опухоли, чем бета‑излучатели. Альфа‑терапия в сочетании с иммунными препаратами сильнее замедляла рост опухоли и ещё больше увеличивала выживаемость. Анализы на уровне отдельных клеток подсказали причину: альфа‑излучение вызывало интенсивное локализованное повреждение, которое, по‑видимому, генерировало сильные сигналы тревоги внутри опухоли, при этом в меньшей степени повреждая соседние иммунные структуры. Такая картина связывалась с более широкими, разнообразными ответами Т‑клеток и признаками того, что формируются новые киллерные Т‑клетки, распознающие опухоль, которые затем связаны с долговременными клетками памяти — свидетельство «прайминга» иммунитета, а не лишь его усиления.
Почему важны тип и время радиации
Во всех моделях ранний или промежуточный тайминг введения ингибиторов контрольных точек — приблизительно совпадающий с пиком радиационно‑индуцированных сигналов опасности — последовательно давал лучшие результаты по сравнению с отложенной терапией. Работа предлагает практическое правило: при опухолях, уже видимых иммунной системой, низкодозные радиофармацевтические препараты на бета‑основе могут быть идеальными партнёрами для ингибиторов контрольных точек, поскольку они распространяют и укрепляют существующий иммунитет. В более иммунно‑устойчивых опухолях высокоэнергетичные альфа‑излучатели лучше подходят для «подготовки» новых Т‑клеточных ответов и превращения «холодной» опухоли в «горячую». Для пациентов это означает, что не все радиоактивные препараты взаимозаменяемы; согласование изотопа и расписания с иммунной «личностью» опухоли может сделать комбинированную радио‑иммунотерапию более эффективной и долговечной.
Цитирование: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Ключевые слова: терапия радиофармацевтическими средствами, альфа против бета излучения, ингибиторы контрольных точек иммунитета, иммунотерапия рака, микроокружение опухоли