Clear Sky Science · ru
Безопасность и биологическая активность биспецифического T‑клеточного рецептора, нацеленного на Gag ВИЧ, у мужчин, живущих с ВИЧ: первое исследование на людях
Почему это новое исследование ВИЧ важно
Люди, живущие с ВИЧ сегодня, могут рассчитывать на почти нормальную продолжительность жизни благодаря современным комбинированным препаратам. Но эти лекарства, называемые антиретровирусной терапией (АРТ), не удаляют вирус; они лишь держат его под контролем. В теле остаются скрытые очаги ВИЧ, которые могут возобновить инфекцию, если лечение прекратить. Это исследование проверяет новый вид точечной иммунной терапии — созданный на основе лабораторного T‑клеточного рецептора — который призван научить иммунную систему безопасно находить и уничтожать эти укрытия у людей, у которых инфекция уже хорошо контролируется АРТ.
Скрытый вирус, который не уходит
Даже когда анализы крови показывают «неопределяемый» уровень вируса, ВИЧ сохраняется в виде генетического материала, укрытого в долгоживущих клетках, в основном в типе белых кровяных клеток, называемых CD4‑T‑клетками. Эти резервуарные клетки несут молчащий, но целый вирус, который может вновь пробудиться, заставив людей принимать таблетки ежедневно всю жизнь. Полное уничтожение каждой инфицированной клетки чрезвычайно сложно и было достигнуто лишь у немногих людей, перенесших рискованные пересадки костного мозга при лечении рака. Многие исследователи вместо этого стремятся к «функциональному излечению»: уменьшению резервуара до уровня, при котором собственные защитные силы организма смогут сдерживать ВИЧ без постоянных лекарств.
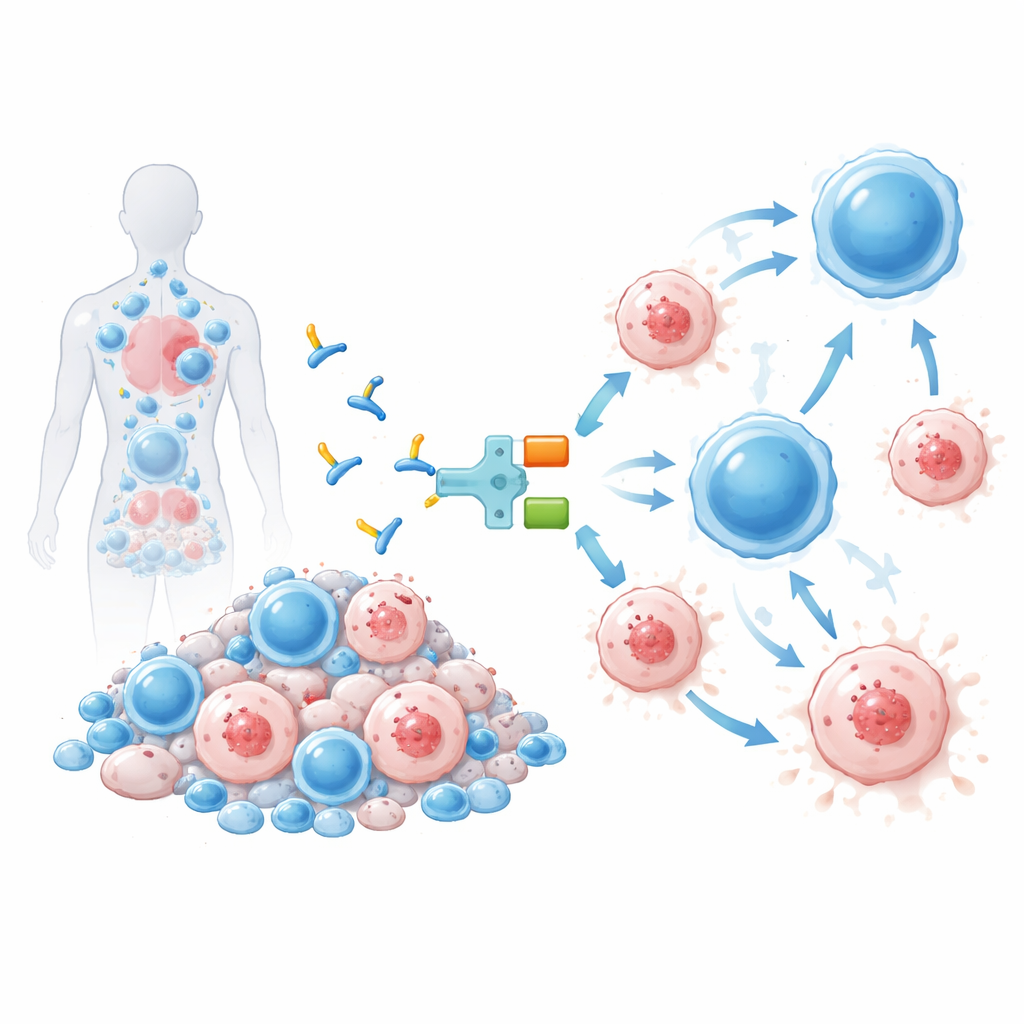
Синтетическая молекула для перенаправления Т‑клеток
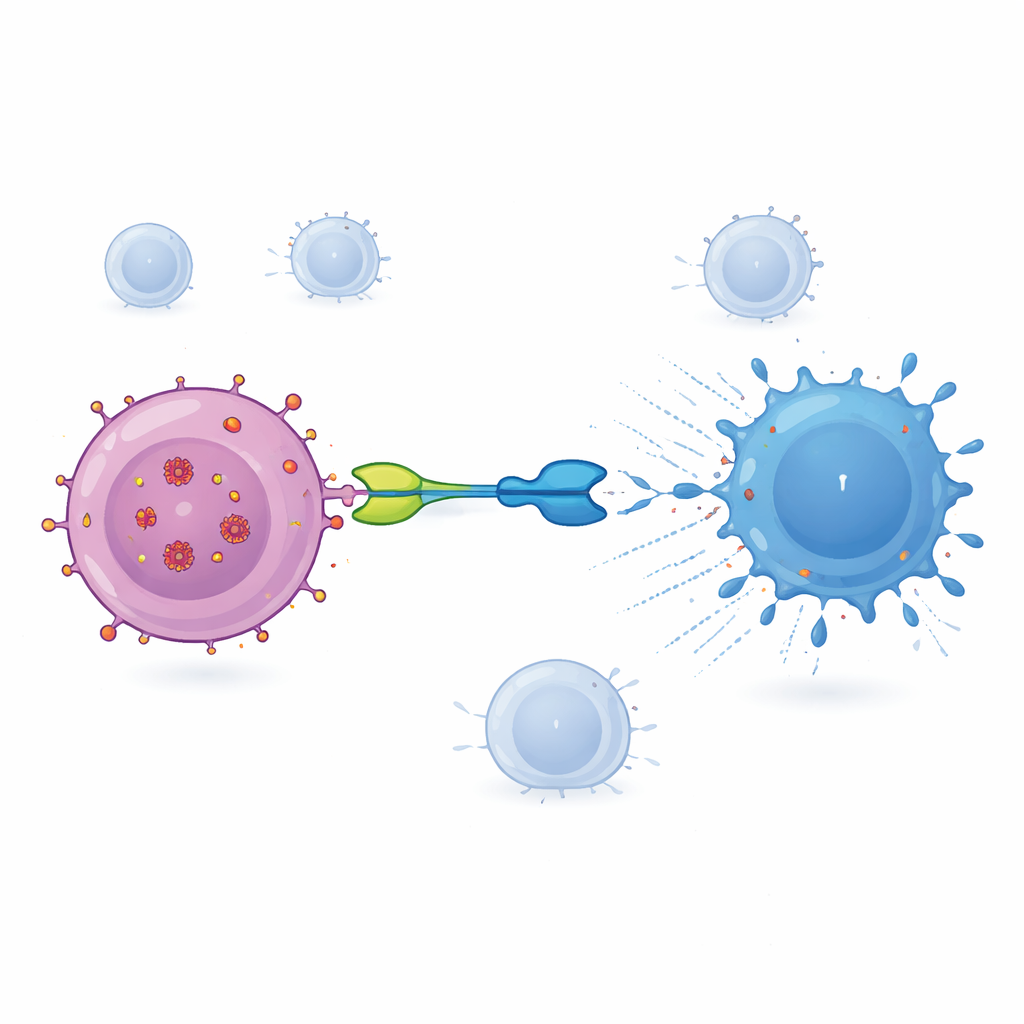
Терапия, протестированная здесь и названная IMC‑M113V, представляет собой небольшой белок, который действует как молекулярный адаптер между инфицированными клетками и иммунной системой. Одна часть IMC‑M113V — это сконструированный T‑клеточный рецептор, который распознаёт небольшой фрагмент ВИЧ из белка Gag, отображаемый на поверхности инфицированных клеток в контексте общего иммунного маркера (HLA‑A*02:01). Другая часть цепляется за CD3 — структуру, присутствующую на всех T‑клетках. Когда IMC‑M113V одновременно связывает обе стороны, он сближает обычные T‑клетки с инфицированной клеткой и запускает их цитотоксическую активность. В лабораторных тестах эта молекула оказалась чрезвычайно чувствительной: она обнаруживала всего несколько копий вирусного фрагмента на поверхности клетки и эффективно устраняла клетки, инфицированные несколькими распространёнными вариантами ВИЧ, при этом не вызывая значимой активации в отношении панели здоровых человеческих клеток.
Первое испытание у людей, живущих с ВИЧ
Чтобы проверить безопасность подхода у людей, исследователи провели раннюю фазу испытания с участием двенадцати взрослых мужчин, живущих с ВИЧ, в Великобритании, Бельгии и Испании. Все участники имели хорошо контролируемую инфекцию на АРТ, высокий уровень CD4 и имели необходимый тип HLA. Каждому человеку однократно вводили внутривенно IMC‑M113V в одной из трёх низких доз, после чего в течение месяца тщательно наблюдали. На этом этапе основной акцент делался на безопасности: поиск побочных эффектов, таких как лихорадка, тяжёлое воспаление или неврологические проблемы, которые могут возникать при других мощных препаратах, вовлекающих T‑клетки, применяемых в онкологии.
Что наблюдали исследователи в клинике
Во всех дозах IMC‑M113V в целом хорошо переносился. У половины участников отмечались некоторые побочные эффекты, в основном лёгкие — утомляемость или раздражение кожи, и ни у кого не развились серьёзные осложнения, такие как синдром высвобождения цитокинов или нейротоксичность. Анализы крови показали, что уровни препарата повышались и снижались в течение примерно суток, с периодом полувыведения около 15–22 часов. При наивысшей дозе (15 микрограммов) у нескольких участников наблюдались временные повышения воспалительных молекул, особенно интерлейкина‑6, и признаки активации их T‑клеток с повышенной способностью продуцировать цитотоксические белки. Эти изменения иммунного ответа были наиболее выражены у добровольцев, вирусы которых несли варианты Gag, к которым IMC‑M113V связывался особенно прочно, что свидетельствует о том, что препарат контактировал с предполагаемыми мишенями в организме. Однако после однократной дозы не было зафиксировано измеримого уменьшения размера вирусного резервуара в крови, судя по уровням вирусной РНК и интактной вирусной ДНК внутри CD4‑клеток.
Что это значит для будущего лечения ВИЧ
Для неспециалиста главный вывод таков: это исследование даёт важное первое доказательство концепции — высокоточная иммунная «мостовая» молекула может быть безопасно введена людям с хорошо контролируемым ВИЧ и способна пробудить их T‑клетки для распознавания клеток, содержащих вирус. Оно не избавило от ВИЧ и не позволило прекратить приём АРТ, но целью этого первого исследования на людях такого уровня не было. Полученные данные обосновывают дальнейшее изучение более высоких и повторных доз, возможные сочетания с препаратами, вынуждающими больше инфицированных клеток проявить вирус, а также расширение подхода на другие типы иммунного ответа помимо HLA‑A*02:01. Если последующие исследования подтвердят, что эта стратегия может надежно уменьшать вирусные резервуары без опасных побочных эффектов, она может стать ключевой частью комбинированных схем, направленных на долговременный контроль ВИЧ без постоянных лекарств.
Цитирование: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Ключевые слова: Лечение ВИЧ, Т‑клеточная терапия, вирусный резервуар, биспецифический рецептор, клиническое исследование