Clear Sky Science · ru
Механистические сведения о раскручивании выбранной i‑мотивной ДНК под управлением PCBP1 на контрольной точке G1/S
Свертки ДНК, работающие как светофоры
Внутри наших клеток генетический код — это не просто прямая лестница ДНК. Его участки могут складываться в необычные формы, которые действуют как крошечные переключатели и помогают контролировать, когда клетки копируют свою ДНК и делятся. В этом исследовании внимание сосредоточено на одной из таких форм, называемой i‑мотивом, и на белке PCBP1, который распознаёт и раскручивает эти структуры именно в тот момент, когда клетка готовится к репликации ДНК. Понимание этого взаимодействия проливает свет на то, как клетки поддерживают стабильность генома и что может пойти не так при раке.
Странные узлы ДНК в зонах, связанных с раком
Большинство людей знают, что ДНК образует знаменитую двойную спираль, но определённые участки, обогащённые буквой C (цитозин), могут складываться в четырёхцепочечный узел, известный как i‑мотив. Эти структуры склонны появляться в регионах регуляции генов, управляющих ростом клетки, таких как cMYC и BCL2. Годы шли споры о том, формируются ли i‑мотивы в живых клетках, поскольку их легче обнаружить в кислых условиях пробирки, чем при близком к нейтральному pH в организме. С помощью специализированных антител, распознающих i‑мотивы, недавние работы, включая настоящее исследование, подтвердили, что они действительно появляются в ядрах клеток — и часто локализуются рядом с ключевыми генами роста и онкогенами.
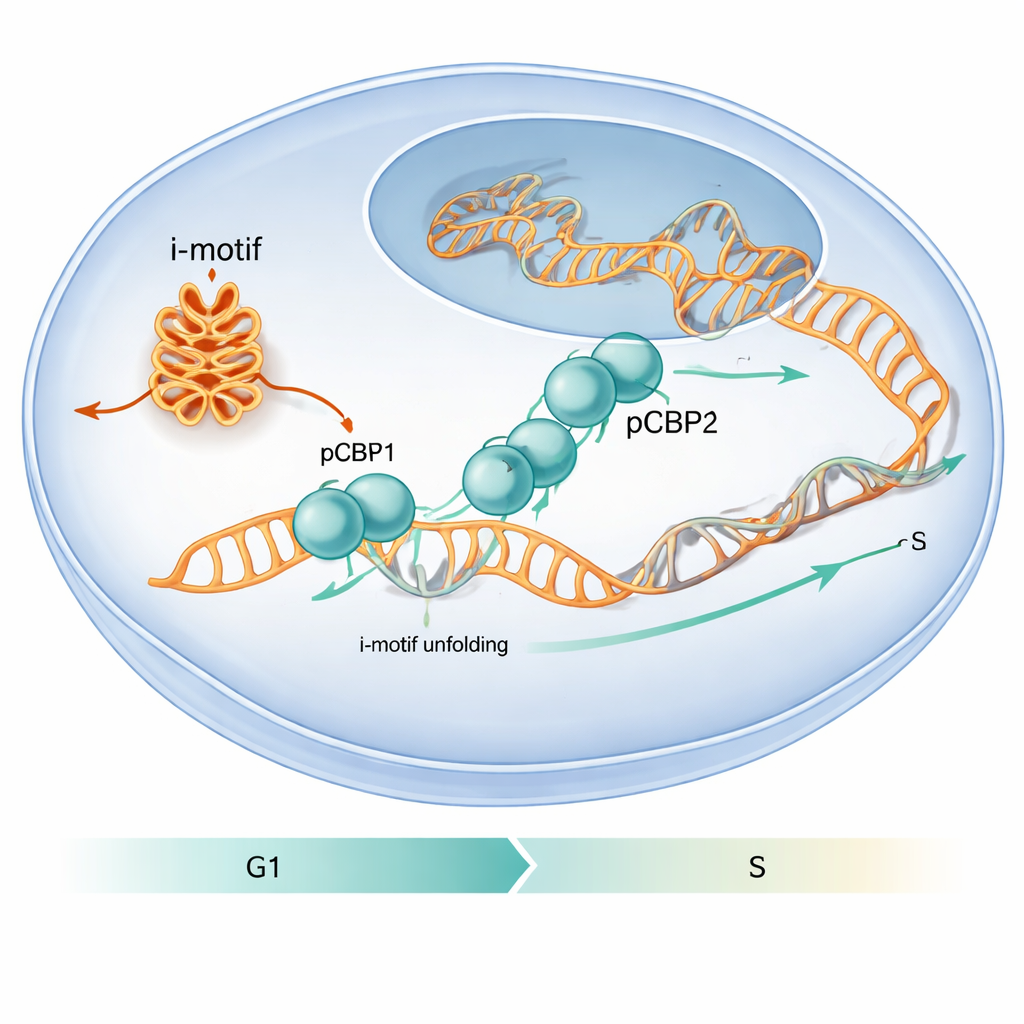
Белок, который выявляет особые свёртки ДНК
Авторы поставили цель выяснить, как белки в клетке обращаются с этими необычными свёртками ДНК. Они сосредоточились на PCBP1 — белке, уже известном своей способностью связываться с C‑обогащёнными участками ДНК и РНК и влиять на клеточный цикл. Анализируя имеющиеся геномные карты связывания и проводя целевые эксперименты, они обнаружили, что PCBP1 часто локализуется на C‑богатых регионах, способных формировать i‑мотивы, особенно возле стартовых сайтов генов. В клеточных экспериментах на линиях человеческих раковых клеток участки промоторов cMYC, BCL2 и последовательность ILPR, связанная с инсулином, показали как сильные сигналы i‑мотивов, так и существенную занятость PCBP1, что говорит о том, что PCBP1 выступает в роли специализированного хранителя этих структур.
Как PCBP1 захватывает и развязывает узел
В пробирочных тестах исследователи сравнивали, насколько хорошо PCBP1 связывается со свёрнутыми i‑мотивами и с теми же последовательностями в распущенной форме. Они настраивали кислотность так, чтобы ДНК либо оставалась сложенной, либо распадалась, при этом сохраняя стабильность белка. PCBP1 постоянно предпочитал свёрнутый i‑мотив, связываясь с ним примерно вдвое сильнее, чем с той же последовательностью в распущенном виде, и лишь слабо связывался с несвязанными формами ДНК. После связывания PCBP1 мог активно способствовать разворачиванию, позволяя цепи i‑мотивa спариться с комплементарной нитью. Однако не все i‑мотивы вели себя одинаково: некоторые, например структура в промоторе cMYC, разворачивались быстро, в то время как другие, как в BCL2, сопротивлялись и раскрывались лишь медленно. Дополнительные особенности, такие как шпилечные петли в ДНК и степень протонирования цитозинов (наличие дополнительного положительного заряда), могли как помогать, так и мешать разгибанию, осуществляемому PCBP1.
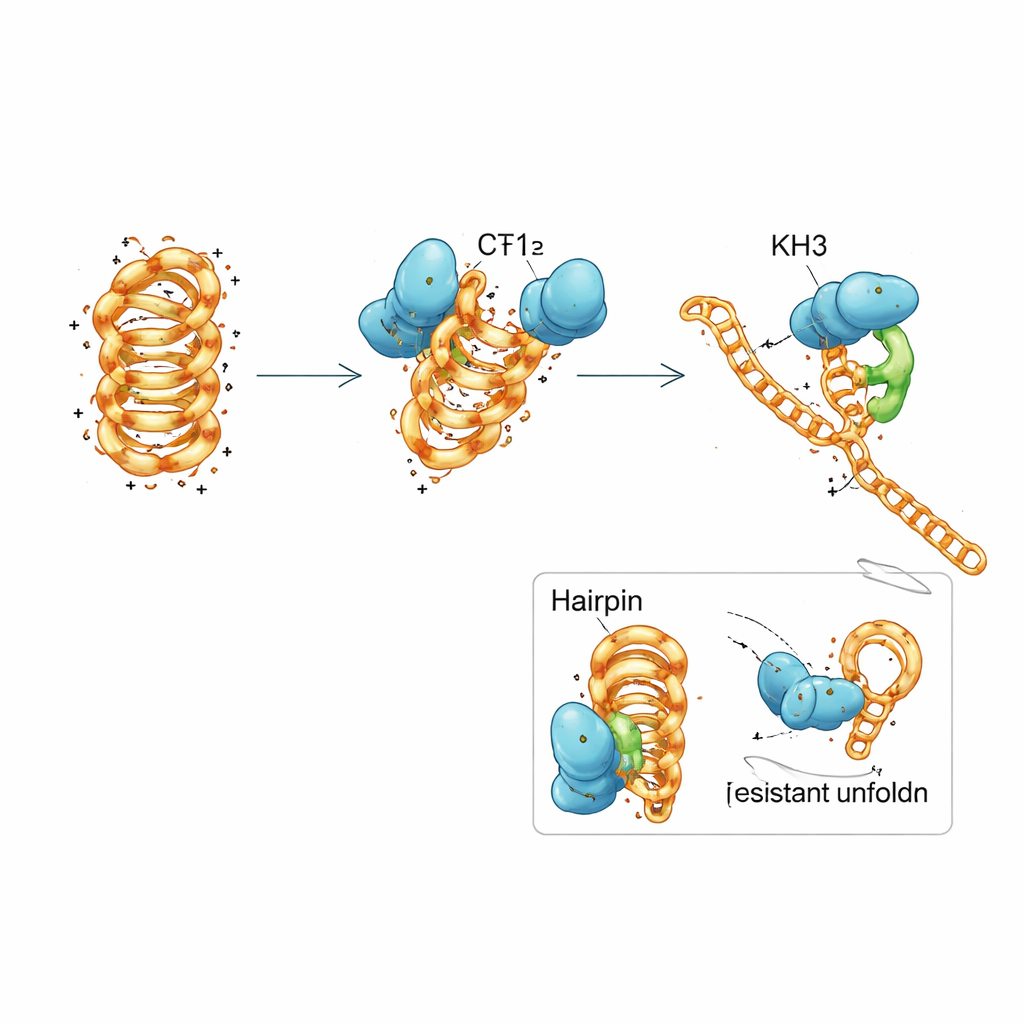
Командная работа внутри одного белка
PCBP1 состоит из трёх повторяющихся модулей, называемых KH‑доменами — распространённых мотивов, которые захватывают короткие отрезки нуклеиновых кислот. Команда разрезала PCBP1 на фрагменты и обнаружила, что ни один отдельный KH‑домен не мог в полной мере воспроизвести поведение целого белка. Первые два домена вместе могли прикрепляться как к свёрнутой, так и к распущенной ДНК и сдвигать i‑мотив в менее стабильную форму, но они лишь медленно способствовали полному разворачиванию. Третий домен по отдельности практически не связывался. Когда все три домена были вместе и могли взаимодействовать, белок вновь приобретал сильное предпочтение к свёрнутым i‑мотивам и эффективную способность их разворачивать. Подробные биофизические измерения и компьютерные моделирования предложили поэтапный механизм: KH1 и KH2 сначала садятся на гибкие петли i‑мотивa и частично разрушают выбранные спаривания оснований, что затем позволяет KH3 вовлечься и привести структуру в открытое, готовое к репликации состояние.
Поддержание расписания клеточного цикла
Работа также показывает, что этот молекулярный танец важен для поведения клетки. При снижении уровня PCBP1 в человеческих клетках на определённых промоторах появлялось больше i‑мотивов, увеличивались маркеры повреждения ДНК, и клетки останавливались на критической контрольной точке G1/S — моменте непосредственно перед началом репликации ДНК. При нормальных условиях присутствие PCBP1 в регионах, формирующих i‑мотивы, достигает пика вокруг этой контрольной точки, а затем падает по мере вступления в фазу S и разрешения i‑мотивов. Такое временное согласование указывает на то, что PCBP1 действует как смотритель: он связывается и разворачивает конкретные i‑мотивы в нужный момент, чтобы репликация ДНК проходила гладко и геном оставался целым. Для непрофессионального читателя основной посыл таков: необычные свёртки ДНК могут выступать как временные препятствия, а PCBP1 — один из специализированных инструментов клетки для их устранения, что помогает предотвратить ошибки, способные способствовать возникновению рака.
Цитирование: Sengupta, P., Gillet, N., Obi, I. et al. Mechanistic insights into PCBP1-driven unfolding of selected i-motif DNA at G1/S checkpoint. Nat Commun 17, 1149 (2026). https://doi.org/10.1038/s41467-026-68822-5
Ключевые слова: i‑мотивная ДНК, белок PCBP1, контрольная точка клеточного цикла, стабильность генома, вторичная структура ДНК