Clear Sky Science · ru
Функциональный ландшафт альтернативного сплайсинга при выборе гемопоэтических линий
Как крошечные правки в генах формируют нашу кровь
Каждую секунду в вашем организме образуются миллионы новых кровяных клеток. За этим тихим чудом стоит молекулярная система редактирования, которая способна вырезать и вставлять фрагменты генетических сообщений по-разному, создавая слегка отличающиеся варианты одного и того же белка. В этом исследовании изучают, как этот процесс редактирования, называемый альтернативным сплайсингом, помогает направлять незрелые стволовые клетки в сторону превращения в эритроциты, лейкоциты или другие типы кровяных клеток — и что происходит, когда отсутствует один отредактированный фрагмент.
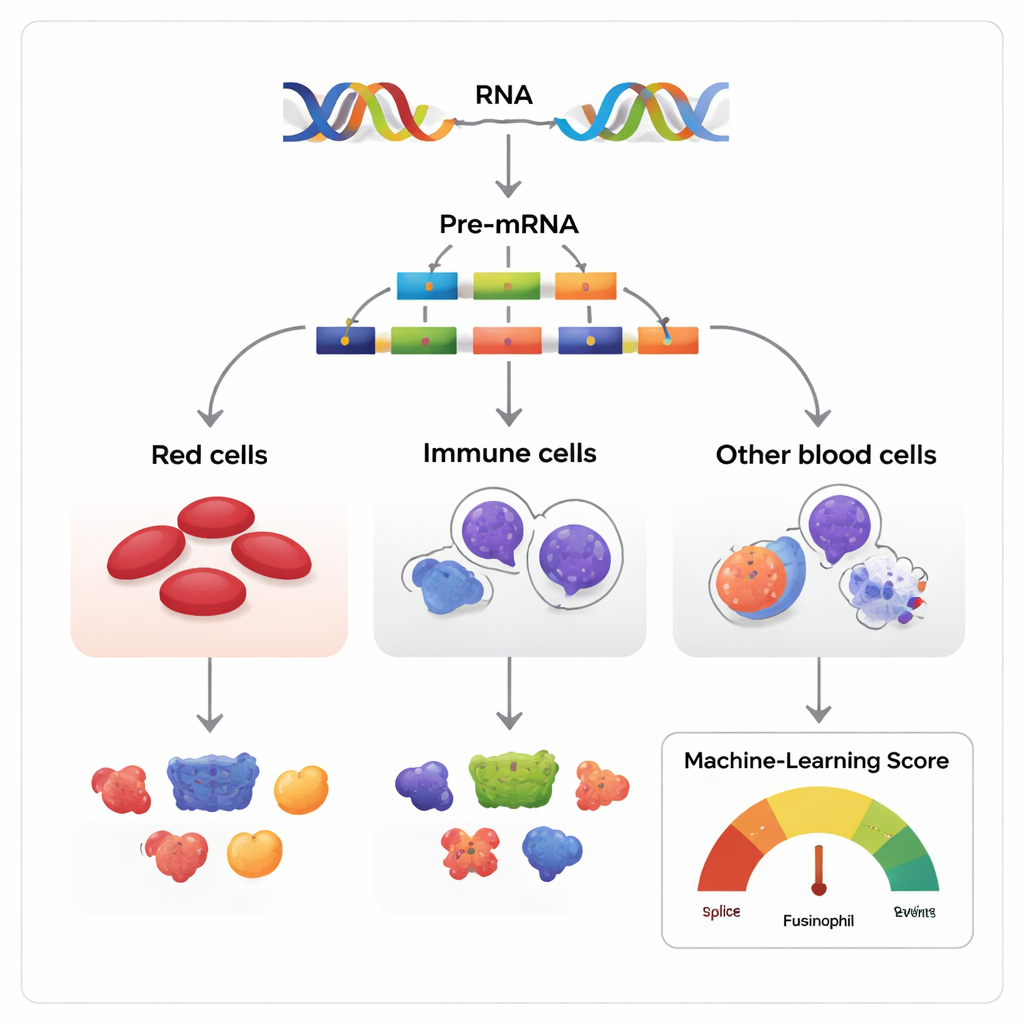
Много версий из одного генетического сценария
Гены часто сравнивают с чертежами, но на самом деле они ближе к сценарию, который можно переставлять. Когда ген считывается, первоначальная копия РНК содержит сегменты, называемые экзонами, которые перед превращением сообщения в белок можно либо сохранить, либо пропустить. Авторы изучали этот процесс, известный как пропускание экзонов, в тканях, образующих кровь у людей, мышей и нескольких других позвоночных. Они собрали более 270 наборов данных РНК, которые вместе прослеживают, как стволовые и прогениторные клетки крови созревают в три главные семьи: эритроидную (производящую эритроциты), миелоидную (борющуюся с инфекциями) и лимфоидную (вырабатывающую антитела).
Ранжирование сплайс-изменений по значимости
Поскольку большинство генов с несколькими экзонами может подвергаться множеству вариантов сплайсинга, основная задача — отличить безвредные варианты от тех, которые действительно влияют на судьбу клетки. Исследователи построили модель машинного обучения, названную Functional AS Score (FAScore), чтобы решить эту проблему. Для каждого события пропускания экзона модель учитывает 19 характеристик, таких как насколько сильно меняется его использование в ходе развития клетки, насколько хорошо соседняя ДНК сохраняется между видами, изменяет ли это известные белковые домены и содержит ли экзон сайты для химических модификаций белка. Алгоритм, обученный по стратегии positive–unlabeled и с использованием классификатора случайного леса, выдает оценку от 0 до 1, показывающую, насколько вероятно функциональное влияние данного сплайс-события.
Поиск консервативных, специфичных для линии переключателей
Применив FAScore к десяткам тысяч событий пропускания экзонов, команда классифицировала их как вероятно функциональные, нефункциональные или неуверенные. События, предсказанные как функциональные, чаще встречались в белковых областях, важных для взаимодействий, в эволюционно консервативных последовательностях и в сегментах, содержащих химические метки, такие как фосфорилирование или SUMOилция. Многие из этих событий также были активны только в определённых кровяных линиях или во время фетального (плодного) гемопоэза, что указывает на их роль как тонко настроенных переключателей в конкретные окна развития. Исследование также показало, что некоторые из самых древних событий сплайсинга — те, что сохранялись у позвоночных на протяжении сотен миллионов лет — особенно часто оказываются функциональными, отражая то, что более старые гены часто несут ключевые биологические роли.
Экспериментальное подтверждение: настройка результатов кроветворения
Чтобы проверить предсказания модели, авторы выбрали несколько экзонов с высокими баллами в генах, активных в разных кровяных линиях, и удалили эти экзоны в стволовых и прогениторных клетках крови мышей с помощью CRISPR. Результаты подтвердили ожидания модели: удаление определённых экзонов в генах KLF6 и SSBP3 нарушало образование миелоидных колоний, не повреждая при этом продукцию эритроцитов, тогда как удаление экзонов в EPB41L1 и TBC1D23 меняло образование эритроидных колоний. В частности, пропускание 15-го экзона TBC1D23 снижало производство предшественников эритроцитов у мышей и зебрафишей, приводя к уменьшению числа циркулирующих эритроцитов и снижению уровня гемоглобина, при этом в значительной степени не затрагивая белые кровяные клетки.
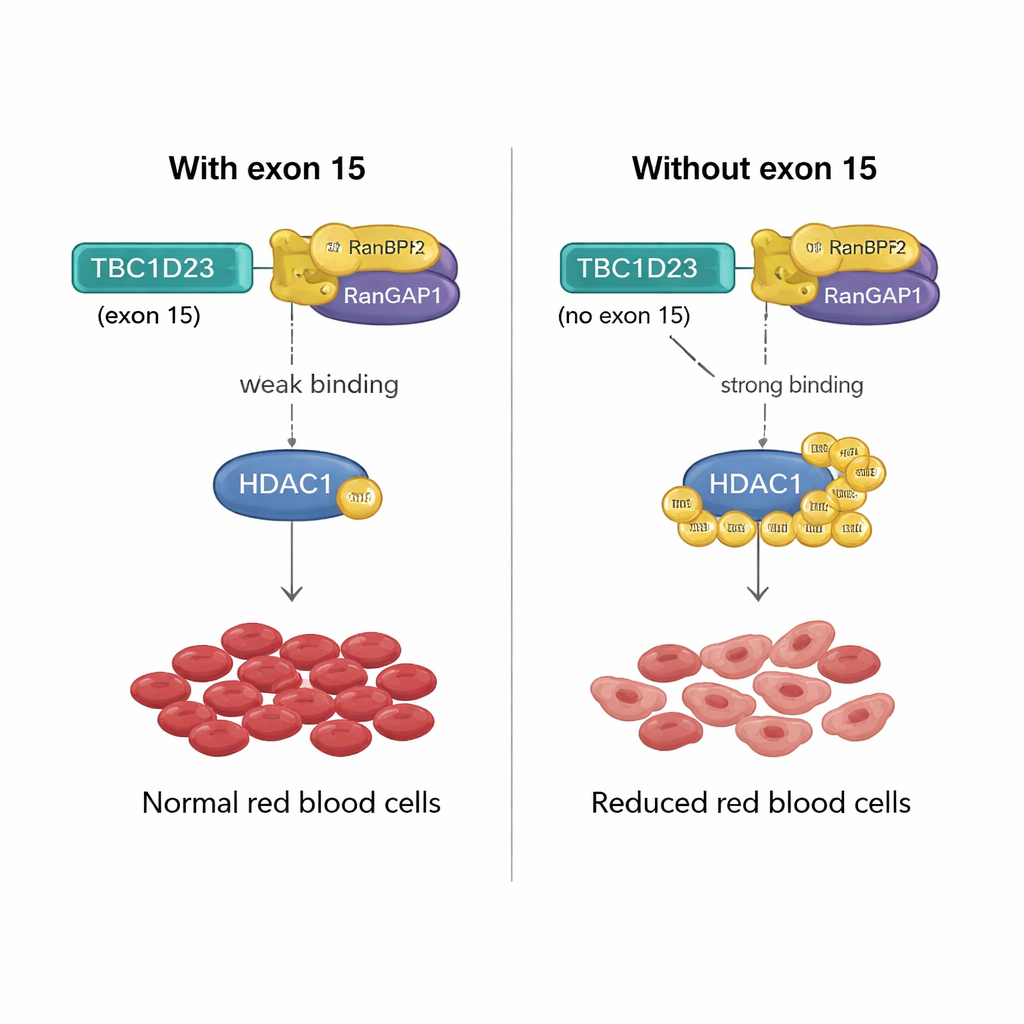
Молекулярный рычаг для производства эритроцитов
Как же участок из 15 аминокислот, кодируемый 15-м экзоном TBC1D23, может так влиять? Команда обнаружила, что включение этого экзона ослабляет связывание TBC1D23 с парой белков RANBP2/RANGAP1, которая сотрудничает при прикреплении SUMO-меток к другим белкам. Без 15-го экзона TBC1D23 связывается с этой парой сильнее, усиливая SUMOилцию ключевого фермента HDAC1. Усиленное помечание изменяет активность множества факторов транскрипции — главных регуляторов экспрессии генов — нарушая программы генов, необходимые для правильного созревания эритроцитов. Когда исследователи создали версию HDAC1, лишённую возможности SUMO-модификации в двух критических позициях, это восстановило образование эритроцитов в клетках, лишённых 15-го экзона TBC1D23, подтверждая, что именно это химическое помечание является ключевым звеном.
Почему это важно для здоровья и будущих терапий
Для неспециалиста основная мысль работы в том, что не все генетические изменения равнозначны: порой разница между здоровой кровью и анемией заключается в том, сохраняется ли крошечный сегмент гена или пропускается при формировании окончательного сообщения. Сочетая крупномасштабные РНК-данные со сложной системой оценивания, исследование предлагает дорожную карту для выявления вариаций сплайсинга, которые наиболее вероятно влияют на то, как стволовые клетки выбирают свою судьбу. Этот подход не только углубляет понимание формирования кровяных клеток в норме и при заболеваниях, но и предлагает общий метод для выявления важных сплайс-событий в других органах, что потенциально может направлять будущие генетические и персонализированные терапии.
Цитирование: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
Ключевые слова: альтернативный сплайсинг, гемопоэз, машинное обучение, красные кровяные клетки, регуляция генов