Clear Sky Science · ru
Клеточные и транскрипционные траектории спецификации нейронной судьбы у актинии выявляют два режима взрословой нейрогенезы
Как простое морское существо продолжает производить новые клетки мозга
Большинство животных, включая людей, создают основную часть своих нейронов в ранней жизни, а затем в значительной степени прекращают этот процесс. Тем не менее некоторые, на первый взгляд простые существа, такие как актинии, продолжают наращивать новые нервные клетки на протяжении всей взрослой жизни. В этом исследовании изучается, как звёздчатая актиния (Nematostella vectensis) постоянно обновляет и перестраивает свою диффузную нервную систему, раскрывая стратегии, которые могут отражать древние решения задачи роста и восстановления мозговой ткани.
Растущему телу нужна растущая сеть нервов
Актинии не имеют мозга; вместо этого у них есть сетчатая нервная система, распределённая по телу. По мере того как эти животные растут или уменьшаются в зависимости от доступности пищи, их нервная сеть должна соответственно расширяться или сжиматься. Используя светочувствительный флуоресцентный белок как временную отметку, авторы промаркировали существующие нейроны у ювенильных взрослых особей и затем наблюдали за появлением новорожденных клеток в течение следующей недели. Они обнаружили множество новых нейронов, разбросанных вдоль оси тела и не ограниченных особой зоной роста. Эти свежие клетки появлялись как на стороне, обращённой к рту, так и на противоположном конце животного, что показывает широкую пространственную распространённость и постоянный характер взрослового нейрогенеза.
Отслеживание происхождения новых нервных клеток
Чтобы выяснить, откуда берутся эти новые нейроны, исследователи сочетали живое визуальное наблюдение с секвенированием РНК одиночных клеток, техникой, позволяющей прочитать, какие гены активны в тысячах индивидуальных клеток. Они сосредоточились на клетках с флуоресцентными «репортёрами», контролируемыми тремя ключевыми генами: FoxL2, SoxC и Elav. FoxL2 отмечает широкий пул делящихся многопотентных прогениторов; SoxC включается кратковременно по мере начала специализации клеток; а Elav сильно активен в пептидергических нейронах, которые в основном общаются с помощью малых сигнальных пептидов. Команда показала, что популяция прогениторов FoxL2-позитивных и Piwi1-позитивных ведёт себя как стволовые клетки: они самоподдерживаются, одновременно постоянно порождая разнообразных потомков, включая нейроны, стрекательные клетки — книдоциты, и секреторные клетки. SoxC и Elav, напротив, загораются только когда клетки покидают этот пул прогениторов и обязуются на конкретные нейральные судьбы.
Два разных пути к взрослым нейронам
Сопоставив временные метки репортёров с транскрипционными подписью каждой клетки, исследование выявило два различных маршрута к зрелым нейронным клеткам. Пептидергические нейроны идут по прямому пути: они возникают из прогениторов, которые уже несут молекулярный профиль, «нацеленный» на пептидергическую судьбу, и затем быстро дифференцируются в разнообразные подтипы нейронов. Новые представители каждого подтипа появляются пропорционально тому, насколько распространён этот подтип уже существует, что свидетельствует о том, что система поддерживает сбалансированную смесь типов нейронов, а не предпочитает какие‑то конкретные. В этой линии нет ясной последовательности промежуточных стадий; вместо этого близкие по признакам нейронные подтипы возникают параллельно из сходно подготовленных прогениторов. 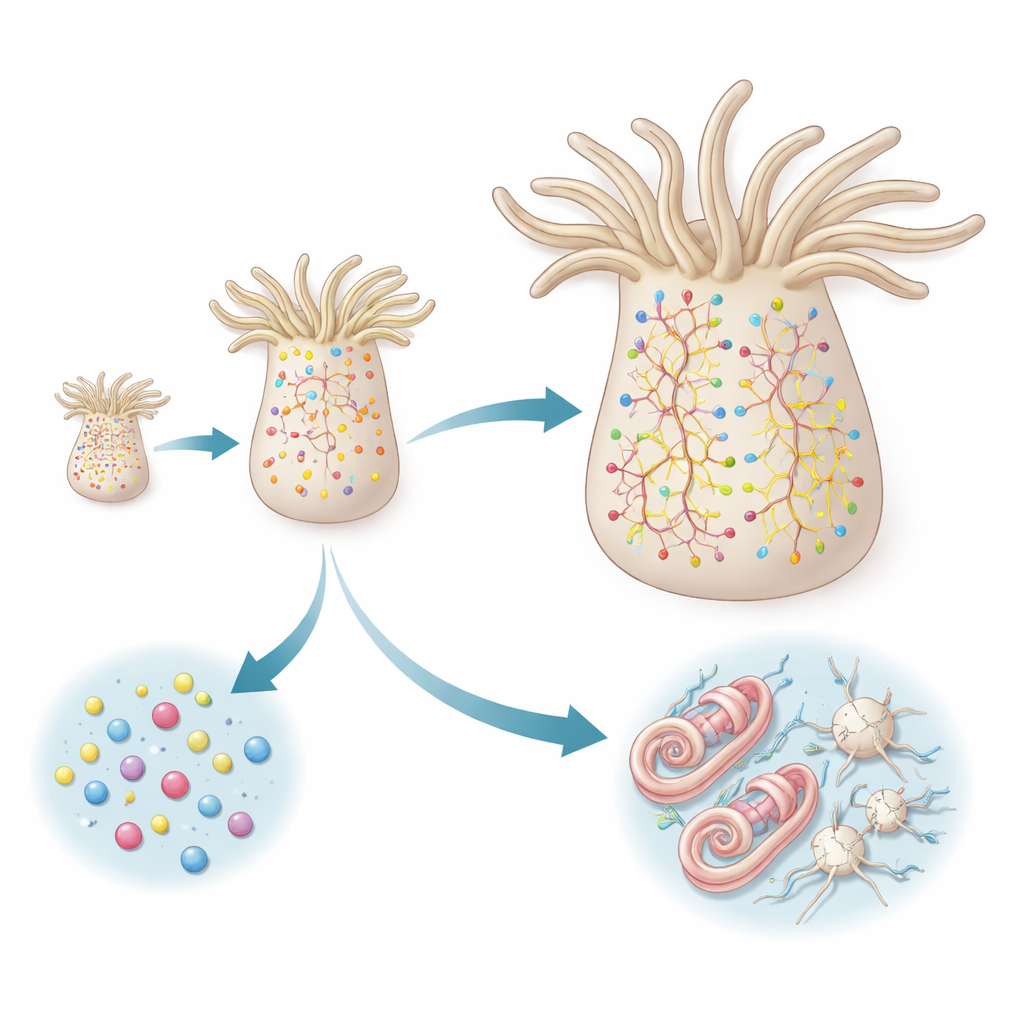
Особый случай стрекательных клеток
Книдоциты, стрекательные клетки, уникальные для книдарий, проходят более поэтапный путь. Сначала они проходят фазу «построения капсулы», в ходе которой формируют характерные для себя прессурированные органеллы, способные выстреливать микроскопическим гарпуном. Эта стадия опирается на специфический набор регуляторных генов и структурных белков, которые в основном отсутствуют в других типах клеток. Только после завершения этой промежуточной программы книдоциты переключаются на вторую, более обычную нейронную программу, добавляя ионные каналы и другие компоненты, необходимые для электрической передачи сигналов. Генетические данные от мутантов, задерживающихся на ранней стадии, укрепляют эту двухфазную модель: блокирование перехода препятствует появлению поздних нейронных признаков. 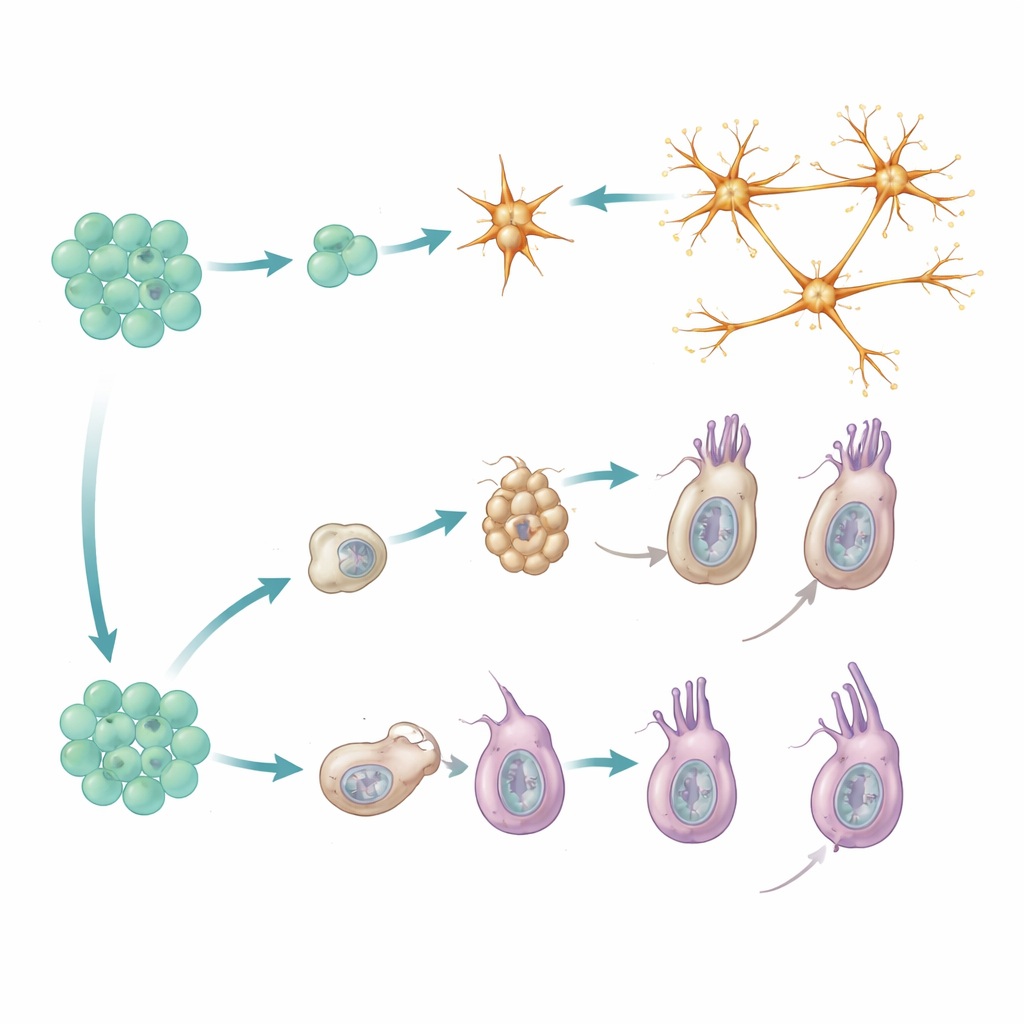
Общие правила и древние корни
Несмотря на разные маршруты, пептидергические нейроны и книдоциты опираются на пересекающиеся семьи регуляторных генов для закрепления своей идентичности. Широкие нейральные признаки связаны с факторами транскрипции семейств bHLH и bZIP, тогда как тонкая спецификация каждого нейронного подтипа задаётся уникальными комбинациями генов с домашодоменами и цинковыми пальцами — «кодом», напоминающим то, как типы нейронов определяются у более сложных животных, включая нематод и позвоночных. Авторы утверждают, что эти модульные стратегии — стволоподобные прогениторы, транзиторная активность SoxC в момент обязательства и подтипоопределяющие коды домашних доменов — могут представлять глубоко сохраняющиеся принципы нейрогенеза. У актиний они обеспечивают пожизненное обновление и масштабирование нервной сети; у других животных родственные механизмы могут лежать в основе как ограниченного взрослового нейрогенеза, так и поразительных регенеративных способностей, наблюдаемых в некоторых линиях.
Цитирование: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
Ключевые слова: взрословой нейрогенез, актиния, нейральные прогениторные клетки, книдоциты, транскриптомика одиночных клеток