Clear Sky Science · ru
Доставка коацерватов пептидов для формирования стабильных центров взаимодействия в клетках
Создание новых «рабочих станций» внутри клеток
Наши клетки заполнены крошечными рабочими зонами, где выполняются важные задачи — например, производство энергии или ответ на стресс. Со временем или при заболеваниях эти естественные «рабочие станции» могут давать сбой. В этой работе исследуется способ добавления полностью новых «центров взаимодействия» в живые клетки с помощью простых лабораторных капель, собранных из коротких пептидов. Эти синтетические центры способны захватывать определённые белки, концентрировать их и даже способствовать их уничтожению, что открывает новые возможности для будущих терапий и клеточного инжиниринга.
Почему клеткам нужны настраиваемые рабочие пространства
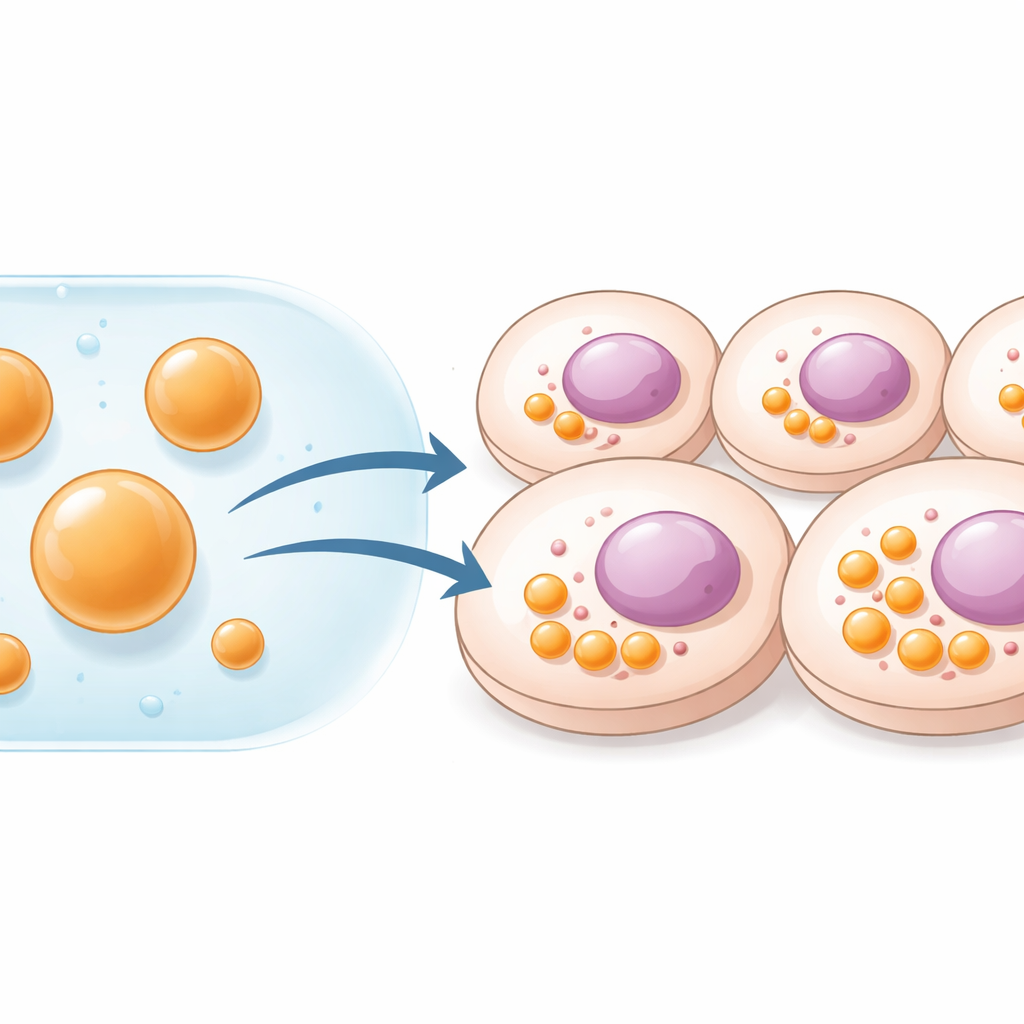
Клетки поддерживают порядок, разделяя разные задачи по отдельным компартментам. Некоторые окружены мембранами, как митохондрии; другие — более мягкие, каплеобразные структуры, которые образуются при кластеризации определённых белков и РНК. Эти жидкие капли, или конденсаты, служат центрами реакций, ускоряя или подавляя конкретные биохимические пути. Ранее учёные создавали такие компартменты, заставляя клетки синтезировать специальные каркасные белки с помощью введённых генов. Хотя этот подход эффективен, он требует доставки ДНК и ограничивает количество материала, которое клетка может произвести. Авторы работы решили обойтись без генетических вмешательств и вместо этого собирать готовые компартменты вне клетки, а затем доставлять их напрямую в виде стабильных капель микронного размера.
Пептидные капли, образующие стабильные центры
Команда работала с короткими, неупорядоченными пептидами, известными как HBpep, и их редокс‑чувствительным вариантом HBpep‑SA. При слегка кислых условиях эти пептиды остаются растворёнными, но при сдвиге pH в сторону физиологических значений — или при понижении температуры — они фазово расслаиваются в мягкие, желатиноподобные капли диаметром примерно 1–5 микрометров. Подбирая концентрацию пептидов, исследователи могли контролировать как размер, так и число капель. С помощью флуоресцентных методов они показали, что молекулы пептидов внутри капель перемещаются медленно, что указывает на гелеобразное состояние, достаточно прочное, чтобы выдерживать разведение и манипуляции. При добавлении в культуры человеческих раковых клеток, клеток меланомы мыши и первичных человеческих иммунных клеток капли эффективно поглощались и накапливались в цитоплазме. Особенно крупные капли сохранялись как минимум пять дней, действуя как долговременные синтетические органеллы внутри живых клеток.
Загрузка и наведение центров
Чтобы эти центры были полезны, они должны удерживать и организовывать белковый груз. Сначала исследователи улучшили загрузку, прикрепив короткий тэг, производный от HBpep, к модельному белку GFP. Этот тэг способствовал сильному распределению GFP в каплях и, что интересно, концентрации белка возле их поверхности, создавая организацию «ядро‑оболочка». Затем они встроили в капли нанотела — компактные белки, подобные антителам, которые прочно связываются с выбранными мишенями. Нанотело, связывающее GFP, позволило центрам селективно захватывать GFP как в пробирке, так и внутри клеток. Поскольку пептидный гель относительно плотен, поначалу большая часть захваченного GFP накапливалась на поверхности капли. Но когда внутренняя структура частично разрыхлялась, либо за счёт изменения редокс‑условий, либо при помощи механизмов, облегчающих выход капель из эндосомных мембран, GFP начинал проникать и в их внутреннюю часть. В клетках химические агенты, способствующие выходу из эндосом, значительно увеличивали долю центров, успешно рекрутировавших свои мишени.
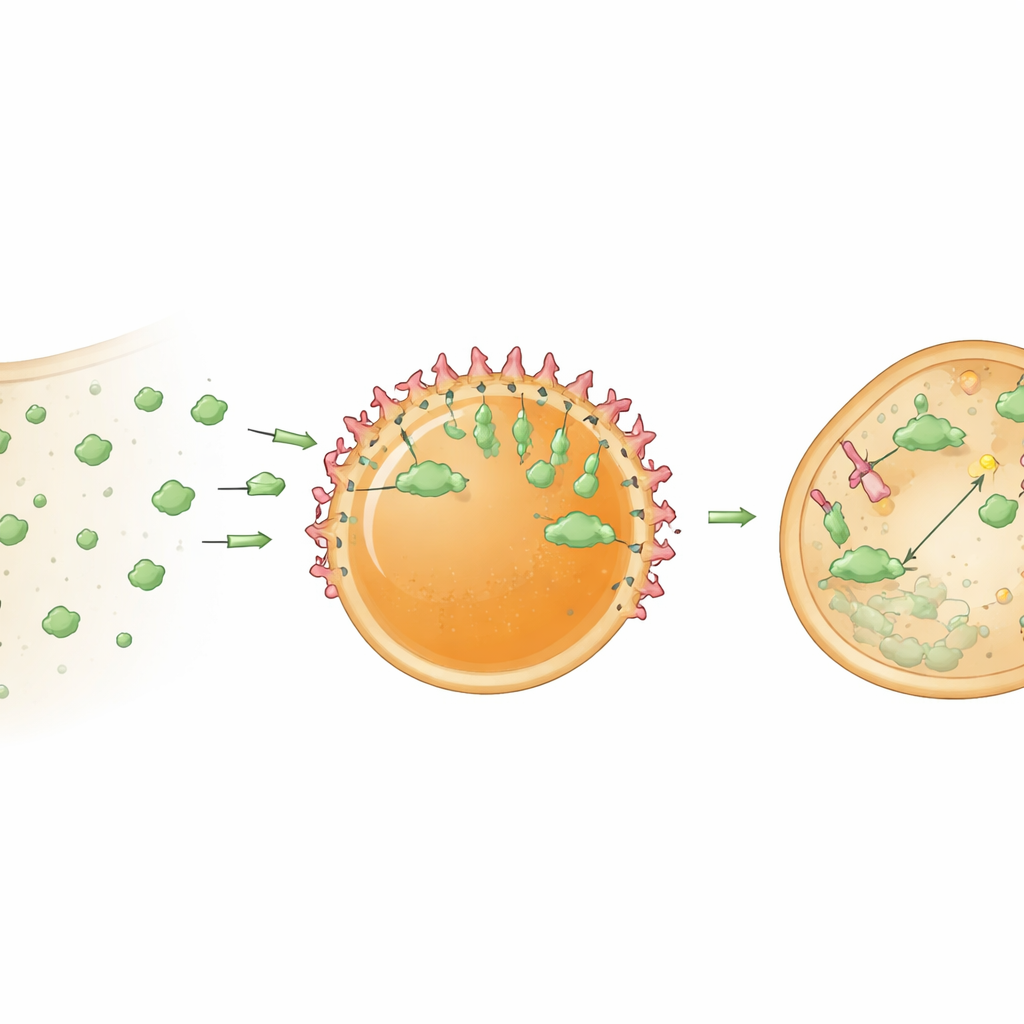
Преобразование центров в «измельчители» белков
Далее авторы превратили эти центры из пассивных ловушек в активные перерабатывающие узлы. Они загрузили капли биоPROTAC — белковый гибрид, который сочетает в себе нанотело, связывающее мишень, и часть адаптора фермента, маркирующего белки для разрушения клеточной системой утилизации. Когда такие «деградосомные» капли доставляли в клетки, стабильно экспрессирующие GFP, уровень цитозольного GFP упал примерно на 78 процентов в течение суток. Контрольные центры, содержащие только нанотело, захватывали GFP, но существенно не снижали его общего уровня, что подтверждает: сильное уменьшение обусловлено целенаправленной деградацией, а не простым захватом. Результаты указывают, что конденсация биоPROTAC внутри концентрированного микроокружения делает их значительно более эффективными, чем при свободном распределении в цитоплазме.
Что это может значить для будущих терапий
Проще говоря, работа показывает, что учёные могут собирать в пробирке пептидные капли, загружать их настраиваемыми белковыми инструментами и доставлять эти капли в живые клетки, где они функционируют как новые, долгоживущие органеллы. Эти синтетические центры способны выборочно притягивать естественные белки и, будучи оснащены механизмами деградации, активно удалять выбранные мишени из клетки. Поскольку платформа обходится без изменения генома клетки и модульна в отношении переносимого груза, она открывает путь к терапиям, восстанавливающим или переписывающим поведение клетки — например, очищение вредных белков или перенастройка нарушённых сигнальных путей — путём простого внедрения новых, программируемых «рабочих станций» в наши клетки.
Цитирование: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Ключевые слова: синтетические органеллы, коацерваты пептидов, внутриклеточная доставка, деградация белков, инжиниринг клеток