Clear Sky Science · ru
Адгезин, связывающий коллаген, сдерживает кожную инфекцию Staphylococcus aureus
Почему «липучка» кожного микроба важна
Staphylococcus aureus — основная причина болезненных кожных фурункулов и абсцессов, и штаммы, устойчивые к препаратам, такие как MRSA, затрудняют лечение этих инфекций. В этом исследовании рассматривается неожиданный поворот: бактериальный поверхностный белок Cna, действующий как «липучка» для коллагена, основного структурного белка кожи и ран. Вместо того чтобы усугублять инфекции, авторы обнаружили, что этот белок, хватающий коллаген, фактически смягчает течение кожного заболевания у мышей, формируя то, как иммунные клетки атакуют бактерии.
Липкий белок с неожиданной ролью
Коллаген — самый распространённый белок в нашем организме, необходимый для удержания кожи и заживления ран. У некоторых штаммов S. aureus есть Cna — белок, прикреплённый к клеточной стенке бактерии, который прочно связывается с коллагеном и с коллагеноподобным хвостом кровяного белка C1q. C1q обычно помогает пометить микробы для разрушения иммунной системой. Ранее Cna связывали с тяжёлыми инфекциями суставов и глаз, но его роль в кожных поражениях была неясна. Исследователи использовали модель кожного абсцесса у мышей и генетически модифицированные бактерии, которые либо экспрессировали Cna, либо не имели его, либо восстанавливали его с плазмиды, чтобы выяснить, как этот одиночный адгезин изменяет ход инфекции.
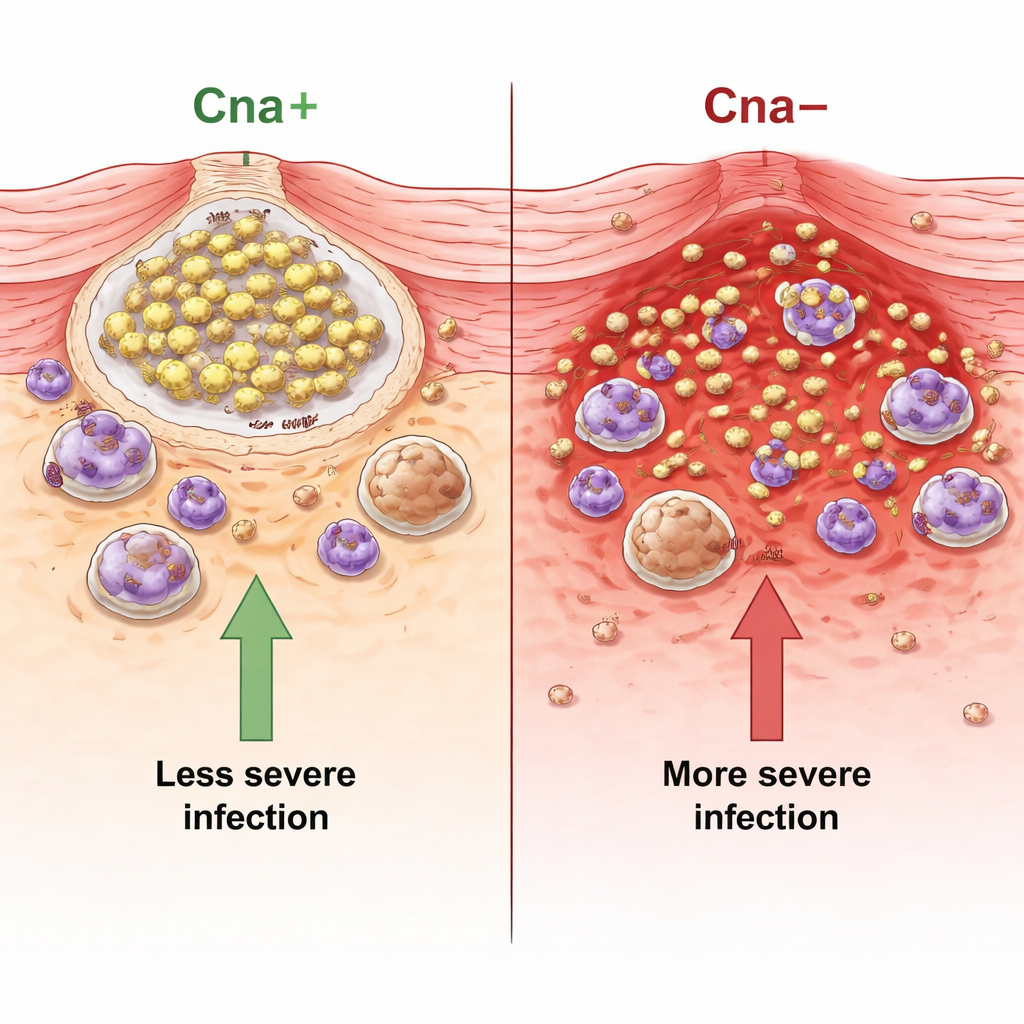
Когда бактерии не хватают коллаген, инфекции становятся хуже
У мышей, заражённых Cna‑положительным S. aureus, кожные поражения оставались меньше, животные теряли меньше веса, и значительно меньше бактерий было выделено из абсцессов, чем у мышей, инфицированных Cna‑отрицательными мутантами. Восстановление Cna устраняло эти эффекты, показывая, что причина кроется в самом белке. Команда также протестировала штамм USA300, распространённый MRSA, который естественно лишён Cna и известен своими кожными инфекциями у людей. Для этого штамма добавление Cna тоже уменьшало размер поражений и количество бактерий. Обзоры изолятов пациентов с кожными инфекциями, из носителей и при пневмонии показали, что большинство циркулирующих штаммов S. aureus вообще не несут ген cna, что указывает на то, что потеря этого белка может на самом деле способствовать более агрессивному и распространяющемуся заболеванию.
Как коллаген защищает бактерии и успокаивает воспаление
Исследование срезов тканей из мышиных абсцессов дало ясную картину. При инфекциях Cna‑положительными бактериями наблюдались компактные бактериальные кластеры, обёрнутые коллагеном, а иммунные клетки, такие как нейтрофилы и макрофаги, собирались по краям. Напротив, при Cna‑отрицательных инфекциях очаги были разорванными и инфильтрированными, наполненными мёртвыми иммунными клетками и выраженным воспалением. Химический анализ тканей показал, что при Cna‑отрицательных инфекциях повышались уровни провоспалительных сигнальных молекул, таких как IL‑6, TNF‑α и IL‑1β, а также ферментов матриксных металлопротеаз (MMP‑9 и MMP‑12) и липидного медиатора лейкотриена B4 — все они усиливают приток иммунных клеток и повреждение тканей. Поточная цитометрия и визуализация подтвердили, что нейтрофилы в Cna‑отрицательных абсцессах значительно чаще были мёртвыми или умирающими, тогда как живых иммунных клеток было относительно мало.
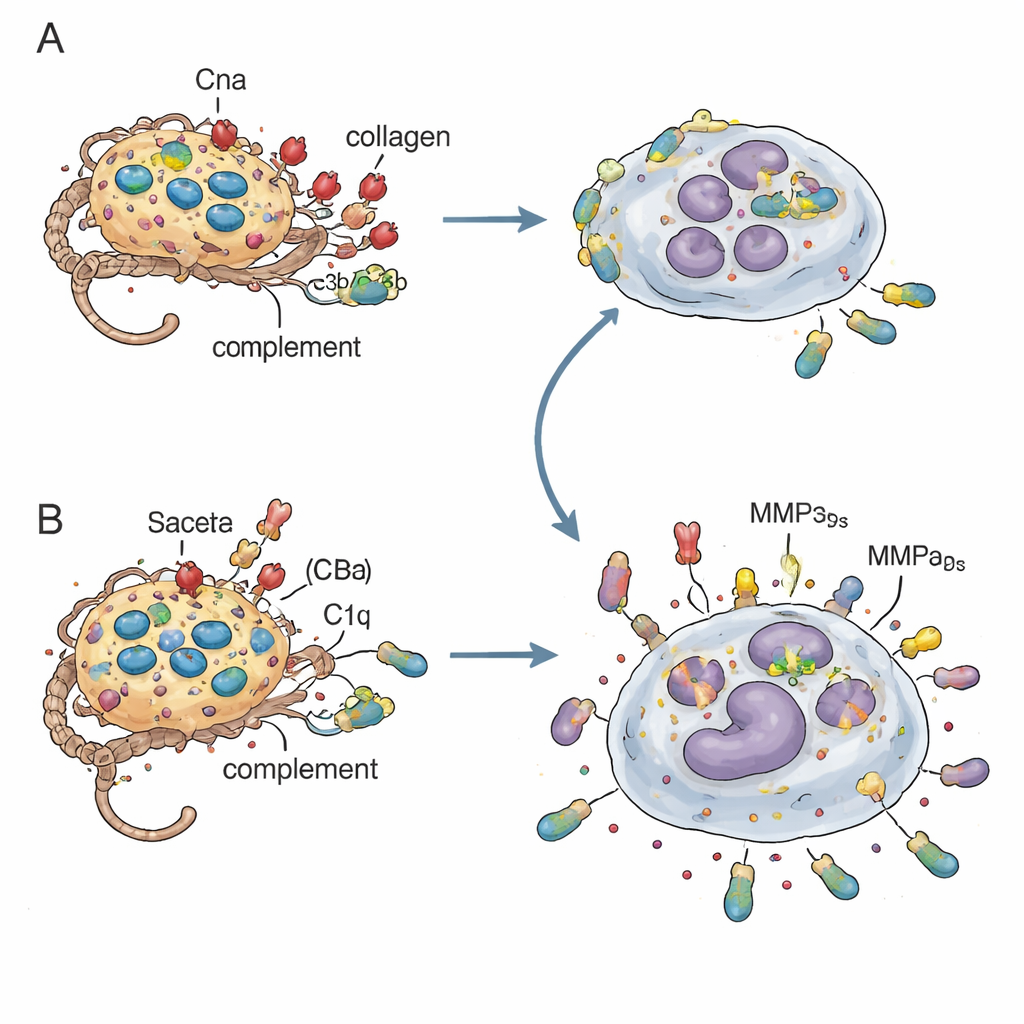
Перехват комплемента, чтобы избежать смертельного захвата
Ключевой механистической связью оказался C1q — молекула запускающей фазы системы комплемента, которая опаковывает бактерии, чтобы нейтрофилы могли их фагоцитировать. В пробирочных экспериментах на поверхностях бактерий, лишённых Cna, накапливалось больше компонентов комплемента (C4b и C3b), и они активнее захватывались человеческими нейтрофилами. Но такая чрезмерная фагоцитозная активность оборачивалась против хозяина: нейтрофилы, переполненные Cna‑отрицательными бактериями, склонны лизироваться, выпуская живые бактерии и провоспалительные молекулы обратно в ткань. Когда исследователи использовали сыворотку, лишённую C1q, или мышей с генетическим дефицитом C1q, различия между Cna‑положительными и Cna‑отрицательными инфекциями сокращались, показывая, что связывание Cna с коллагеноподобным хвостом C1q ослабляет пометку комплементом и смягчает чрезмерную реакцию нейтрофилов. Одновременно коллаген, обвивающий Cna‑положительные бактерии, по‑видимому, создаёт физический барьер, замедляющий прямой контакт с нейтрофилами и позволяющий более контролируемому уничтожению.
Баланс между защитой и повреждением при кожных инфекциях
Для неспециалиста главный вывод в том, что не всякая бактериальная «прилипчивость» ухудшает инфекцию. В этом случае штаммы S. aureus, способные цепляться за коллаген и C1q, вызывают более взвешенную иммунную реакцию: меньше нейтрофилов гибнет взрывным образом, воспаление ниже, и повреждение кожи уменьшается, хотя бактерии по‑прежнему присутствуют. Штаммы, лишённые Cna, включая многие значимые клоны MRSA, легче помечаются комплементом, запускают бурную нейтрофильную активность и в итоге вызывают более крупные, разрушительные абсцессы. Понимание этого тонкого равновесия между сокрытием бактерий и чрезмерной реакцией иммунитета может помочь разработать новые стратегии лечения кожных инфекций — либо направленные на то, как бактерии взаимодействуют с коллагеном и C1q, либо на модуляцию воспалительных ферментов и липидов, которые превращают локальный абсцесс в разрушительное поражение.
Цитирование: Bhattacharya, M., Spencer, B.L., Kwiecinski, J.M. et al. Collagen binding adhesin restricts Staphylococcus aureus skin infection. Nat Commun 17, 1980 (2026). https://doi.org/10.1038/s41467-026-68788-4
Ключевые слова: Staphylococcus aureus, кожный абсцесс, коллаген, нейтрофилы, система комплемента