Clear Sky Science · ru
NatA участвует в многофакторных комплексах у выхода рибосомного туннеля для полипептидов
Как клетки точно настраивают вновь синтезируемые белки
Каждую секунду ваши клетки производят тысячи новых белков на крошечных машинах, называемых рибосомами. Когда каждая белковая цепь выходит наружу, её нужно обрезать, пометить и свернуть правильно — в противном случае белок может неправильно функционировать и способствовать развитию заболеваний. В этом исследовании рассматривается одна из ключевых систем пометки — модификация, называемая N-концевым ацетилированием, — и показано, как центральный ферментный комплекс NatA взаимодействует с несколькими партнёрами прямо в месте выхода новых белков из рибосомы. Понимание этой хореографии помогает объяснить, как клетки поддерживают бесперебойную работу своих белковых фабрик.
Малая химическая метка, которая имеет значение
Большинство белков начинается с одного и того же первого компонента — аминокислоты метионина. Часто этот начальный метионин удаляют и заменяют маленькой химической меткой — ацетильной группой. Эта метка, добавляемая к самому концу белка (его N-концу), может влиять на продолжительность жизни белка, его локализацию в клетке и функцию. Два основных типа ферментов находятся у выхода рибосомного туннеля, чтобы управлять этой первой «перевоплощением»: метионин-аминопептидазы (MAPs), которые отрезают начальный метионин, и N-концевые ацетилтрансферазы (NATs), которые добавляют ацетильную метку. Среди NAT комплекс NatA является «трудягой» в человеческих клетках, потенциально модифицируя почти 40% всех белков. Поскольку многие белки синтезируются одновременно, клетке нужно организовать эти ферменты так, чтобы обрезка и пометка происходили быстро и в правильном порядке.
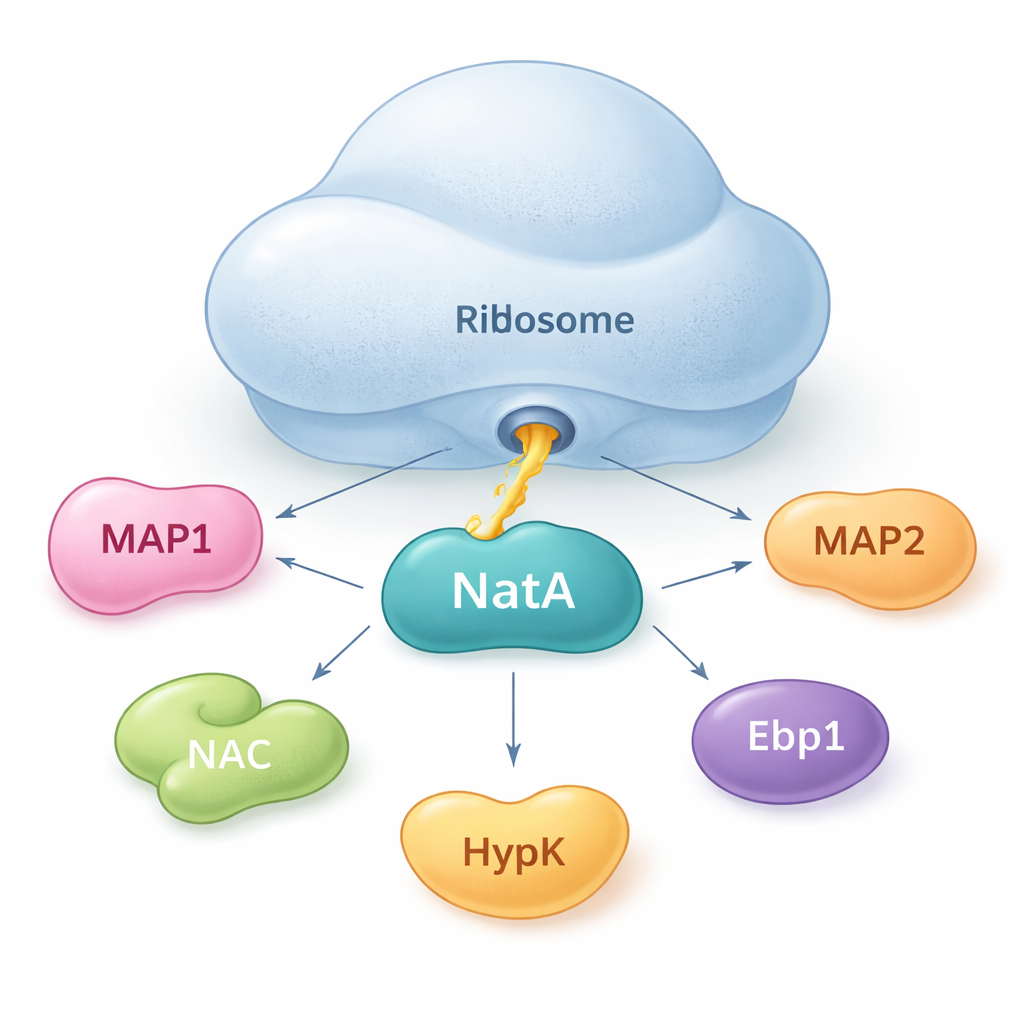
NatA как узел для помощников белка
Авторы показывают, что NatA не действует в одиночку. Скорее, он ведёт себя как центр, собирающий несколько вспомогательных белков как на рибосоме, так и вне её. С помощью чувствительных измерений связывания в растворе они обнаружили, что NatA может образовывать прочные комплексы с MAP1, ассоциированным с нарастающей полипептидной цепью комплексом (NAC), регуляторным белком HypK и другим ферментом Naa50, даже без присутствия рибосомы. NAC может мостить NatA к MAP1, позволяя связать шаги обрезки и пометки в одной сборке. Однако HypK, который обычно подавляет активность NatA, может блокировать связывание NAC. Это наводит на мысль, что клетки могут переключать NatA между более активным состоянием, связанным с NAC, и сдержанным, связанным с HypK, в зависимости от своих потребностей.
Вторая точка докинга прямо у выхода туннеля
Используя крио-электронную микроскопию — метод, который визуализирует большие молекулы с почти атомарной детализацией — исследователи обнаружили, что NatA может связываться с рибосомой в двух различных положениях. Одно место, известное ранее, располагается немного отдалённо от выхода туннеля. Новооткрытое «проксимальное» место помещает каталитическое ядро NatA очень близко к тому месту, где появляется растущая белковая цепь, сокращая расстояние, которое цепь должна пройти для модификации. Любопытно, что оба положения могут быть заняты одновременно, то есть на одной рибосоме могут сидеть два комплекса NatA. Более удалённая копия действует как каркас и якорь, тогда как проксимальная копия оптимально расположена для пометки новых белков. Две молекулы NatA также контактируют друг с другом, что указывает на способность NatA координировать собственные дубликаты в многоферментные команды.
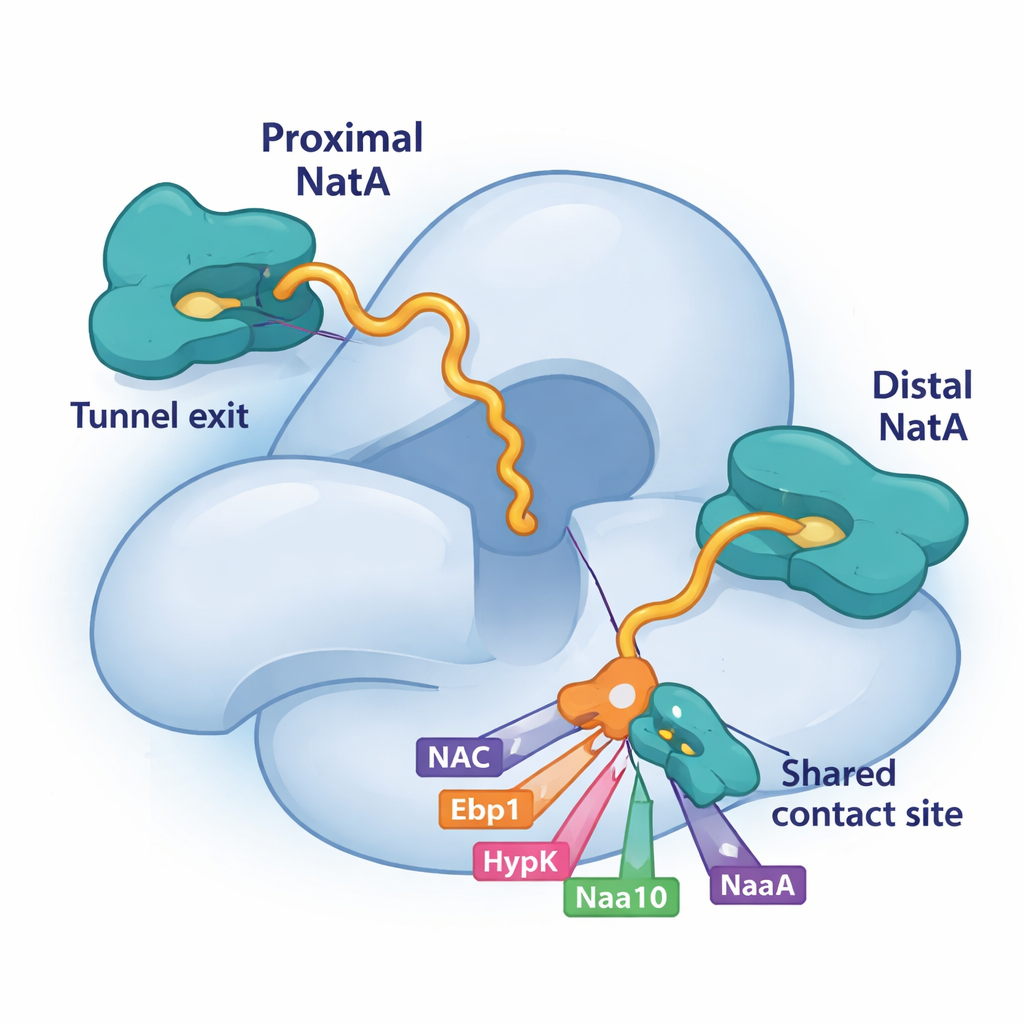
Конкуренция за общий посадочный участок на NatA
Ключевым элементом этой головоломки является небольшая бороздка на большой субъединице NatA, Naa15. Исследование показывает, что четыре разных фактора, ассоциированных с рибосомой — NAC, HypK, Ebp1 и даже хвостовой сегмент каталитической субъединицы NatA, Naa10 — используют короткие спирали, чтобы зацепиться за точно тот же участок на Naa15. Поскольку все они опираются на этот общий посадочный участок, им приходится конкурировать за доступ. Когда место занимает HypK, он не только подавляет активность NatA, но и препятствует образованию пар NatA с NAC или димеров NatA–NatA. Когда же там связываются NAC, псевдофермент Ebp1 или проксимальный Naa10, они могут перестраивать положение NatA или его связи на рибосоме. Такая конкуренция при связывании даёт клетке гибкий способ выбирать, какие партнёры будут собраны вокруг NatA в каждый конкретный момент.
Псевдофермент как диспетчер трафика
Белок Ebp1 особенно интересен. Он напоминает один из ферментов, удаляющих метионин, но лишён каталитической активности; это «псевдофермент». Предыдущие работы показали, что Ebp1 может располагаться на рибосоме возле выхода туннеля и зажимать длинный участок РНК. В этом исследовании авторы обнаружили, что когда NatA присоединяется к рибосоме, Ebp1 смещается, отпускает РНК и вместо этого использует свою собственную спираль, чтобы занять тот же сайт связывания на Naa15, который используют NAC и HypK. Такая перестройка указывает на то, что Ebp1 может действовать как «временный занявший место» или организатор: он может формировать локальную среду РНК, а затем передавать управление активным ферментам вроде MAPs и NatA, не участвуя непосредственно в химической реакции.
Почему это молекулярное регулирование важно
Неспециалисту детали спиралей и сайтов связывания могут показаться абстрактными, но смысл прост: клетки управляют строго срежиссированной, многоступенчатой системой качества прямо там, где рождаются белки. NatA стоит в центре этой системы, способный привлекать или отпускать разных партнёров в зависимости от того, кто получает доступ к критическому участку докинга и в каком положении на рибосоме находится NatA. Эта гибкая сеть помогает обеспечить, чтобы обрезка и ацетилирование происходили с правильным временем и порядком для тысяч различных белков. Поскольку ошибки в N-концевой обработке связаны с нарушениями развития, нейродегенерацией и раком, картирование того, как NatA и его партнёры собираются, даёт исследователям более чёткую схему того, как контролируется ранняя обработка белков — и как её можно было бы нацелить при сбоях.
Цитирование: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Ключевые слова: контроль качества белка, N-концевая ацетилирование, выход рибосомного туннеля, комплекс NatA, ко-трансляционная модификация