Clear Sky Science · ru
Фукозилтрансфераза растений FUT11 искажет принимающий сахар для катализа через кратковременный оксокарбониевый промежуточный механизм
Как растения точно настраивают сахара на своих белках
Белки в наших клетках и в клетках растений часто украшены сложными цепочками сахаров, которые работают как штрих‑коды, направляя сворачивание белков, их срок службы и выбор партнеров для связывания. В этом исследовании внимание сосредоточено на растительном ферменте FUT11, который присоединяет к этим цепочкам крошечный сахар — фукозу. Раскрыв, как FUT11 работает на атомном уровне, авторы показывают неожиданный прием: фермент кратковременно деформирует свой сахарный акцептор, чтобы преодолеть трудный химический шаг. Понимание этого процесса важно не только для базовой биологии, но и для разработки более безопасных лекарств, производимых в растениях, которые не вызывают нежелательные иммунные реакции у людей.
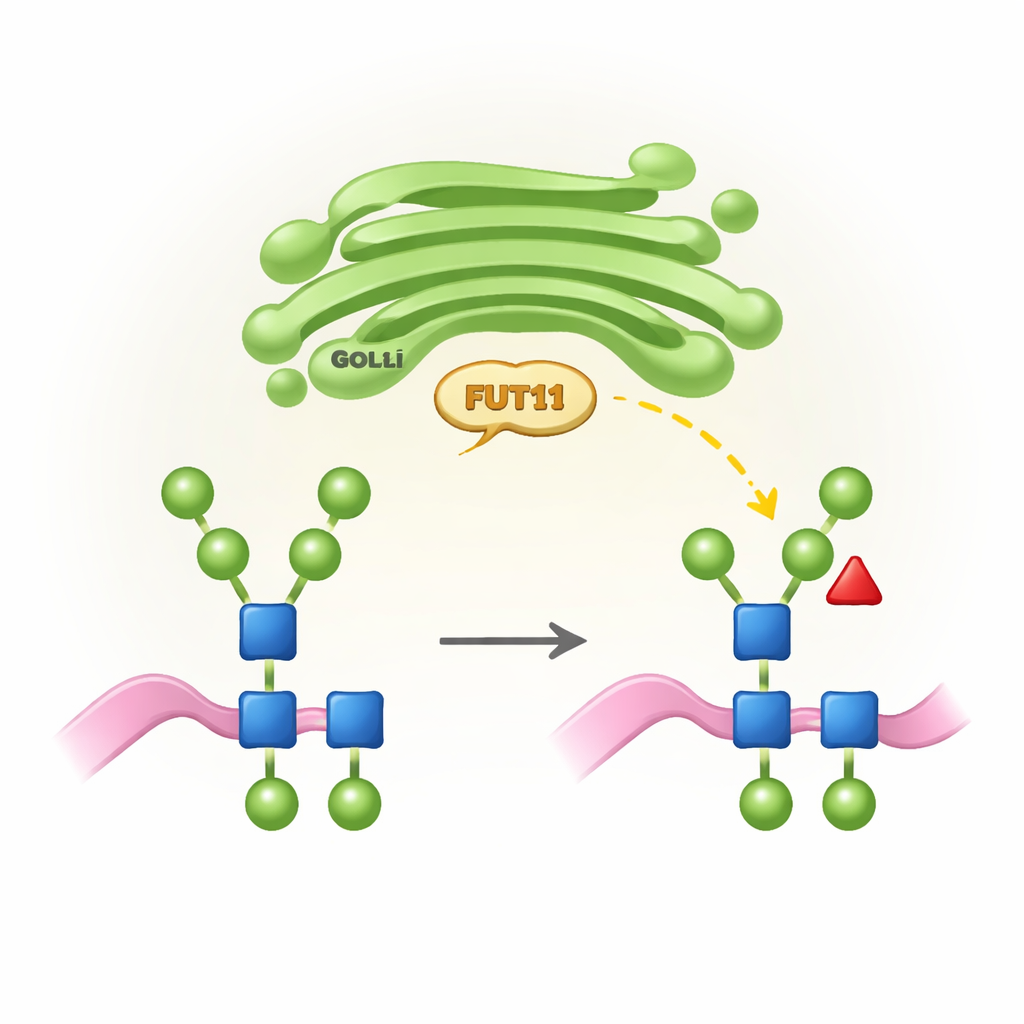
Растительные маркеры сахаров и почему они важны
Все высшие организмы используют процесс, называемый N‑гликозилированием, чтобы присоединять сахарные цепочки (N‑олигосахариды) к определенным участкам белков. У животных эти цепи в аппарате Гольджи клеток переделываются в сложные структуры, часто заканчивающиеся сиаловой кислотой и несущие корневую фукозу в одном специфическом положении. Растения же следуют другой «правиловой схеме»: их N‑олигосахариды обычно не содержат сиаловой кислоты, но несут корневую фукозу в другом положении (называемом b1,3), а также дополнительный ксилозный остаток. Эти растительно‑специфические особенности важны для нормального роста и плодовитости, но человеческая иммунная система может рассматривать их как чужеродные. FUT11 — один из ключевых растительных ферментов, который устанавливает эту корневую фукозу, и его активность формирует как развитие растений, так и то, как растительно‑произведенные терапевтические белки будут восприниматься в нашем организме.
Карта участков, где FUT11 может работать на сложных разветвлениях сахаров
Чтобы понять, что распознает FUT11, исследователи протестировали фермент на микрочипе с 144 различными структурами N‑олигосахаридов. Они обнаружили, что FUT11 довольно селективен в отношении одной ветви сахарного «дерева» — так называемой ветви b1,3, — которая должна нести определенный строительный блок (терминальную N‑ацетилглюкозамин — GlcNAc), чтобы реакция прошла. Вместе с тем FUT11 терпим к другим украшениям: он по‑прежнему работает, когда центральный манноз содержит растительную ксилозу, и даже если на корне уже добавлена фукоза в животном положении. Противоположная ветвь (b1,6) в основном открыта к раствору и образует лишь слабые контакты с ферментом, что объясняет, почему FUT11 способен справляться с широким спектром модификаций там. Эти предпочтения связывания помогают объяснить, почему растения формируют характерный набор структур N‑олигосахаридов, и показывают, как FUT11 можно использовать или избегать при инженерии растительных клеток для биотехнологий.
Уникальная структурная архитектура для захвата и позиционирования сахаров
С помощью рентгеновской кристаллографии команда получила трехмерную структуру FUT11 в комплексе с донором сахара (GDP‑фукоза) и N‑олигосахаридным акцептором. Фермент имеет двулопастную архитектуру типа «GT‑B»: одна лопасть охватывает GDP‑фукозу, тогда как необычно сложная акцепторная лопасть, включающая растительно‑специфическую N‑концевую подсекцию, обвивает N‑олигосахарид. Эта дополнительная подсекция, связанная с остальной частью фермента дисульфидными мостиками, фиксирует центральную часть гликана и помогает ориентировать реактивный остаток GlcNAc в сторону донора. Мутации ключевых аминокислот подтвердили их роли: замена единственного глутамата (Glu158) устраняла активность, а изменение двух близких остатков значительно ослабляло фукозилирование в генетически модифицированных человеческих клетках. Эти результаты связывают структурные снимки с реальной клеточной функцией, показывая, какие части белка незаменимы для связывания и катализа.
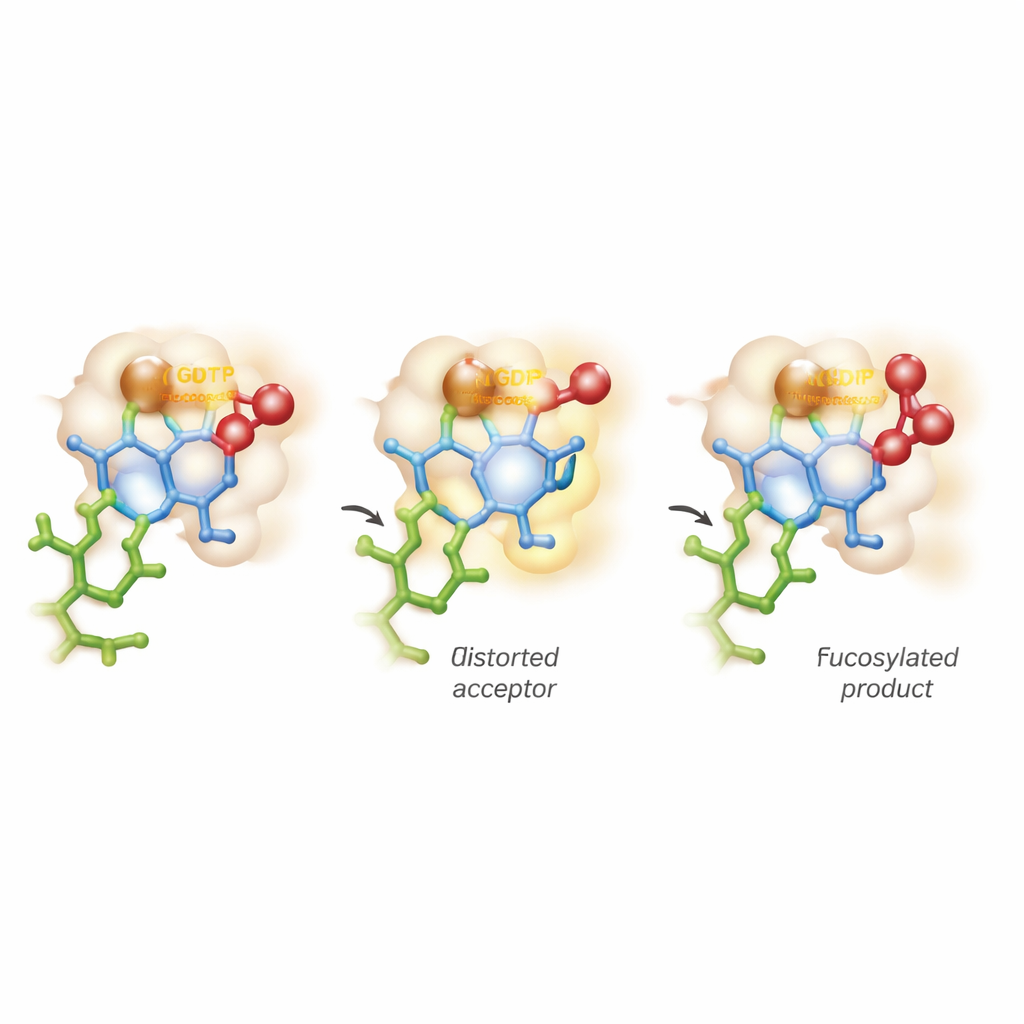
Искривление сахара и баланс между двумя путями реакции
Самое поразительное открытие получено с помощью продвинутых компьютерных моделирований, объединяющих квантовую механику и молекулярную динамику. Традиционный взгляд предполагает, что принимающий сахар сохраняет стабильную, кресловидную конформацию, пока фермент лишь активирует донора. Здесь FUT11 ведет себя более активно: взаимодействия, управляемые Glu158, временно искажают внутреннее кольцо GlcNAc в менее комфортную, «сжимаемую» форму. В этом напряженном положении критическая гидроксильная группа оказывается идеально выровненной для атаки на донор фукозы. Вычисления показывают, что по мере разрыва химической связи с GDP возникает короткоживущий, положительно заряженный «оксокарбониевоподобный» состояние на сахаре, прежде чем новая связь с акцептором полностью сформируется. Это означает, что реакция не укладывается строго в учебные категории SN1 или SN2, а протекает вдоль континуума, в асинхронной, почти поэтапной манере.
Скрытая гибкость и эволюционные отголоски
Сравнивая FUT11 с родственным человеческим ферментом FUT9, авторы обнаружили, что растительный фермент также может, пусть и слабо, модифицировать другой тип сахарного мотива (LacNAc), создавая структуру, известную как Lewis X. Эта побочная активность, вероятно, не имеет биологического значения у растений, где Lewis X обычно не встречается, но она подчеркивает, как схожие белковые каркасы могут быть переориентированы в процессе эволюции для работы в разных сахарных контекстах. Исследование показывает, что FUT11 и его родственники разделяют модульную основу распознавания N‑олигосахаридов, с тонкими изменениями, которые смещают специфичность между растительными корнями и животными «антеннками».
Почему этот прием с изгибом важен для науки и медицины
В совокупности работа демонстрирует, что FUT11 делает больше, чем просто сближает двух сахарных партнеров: он активно изгибает акцепторный сахар в реакционно‑способную позу и направляет химию через мимолетный, заряженный промежуточный этап. Для непрофессионального читателя это означает, что сахар на белке — не жесткая докинговая площадка, а гибкий участник, которого фермент формует по своему усмотрению. Эта новая перспектива «конформационного катализа» помогает объяснить, как ферменты достигают одновременно скорости и селективности, и дает план по перенастройке путей гликозилирования. В практическом плане знание того, как именно FUT11 распознает и модифицирует растительные N‑олигосахариды, может направлять инженерные работы по культурам и системам производства на растительной основе, чтобы минимизировать иммуногенные сахарные мотивы в человеческих терапиях или создавать дизайнерские гликопротеины с заданными биологическими свойствами.
Цитирование: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Ключевые слова: гликозилирование растений, фукозилтрансфераза FUT11, N-олигосахариды, механизм фермента, гликоинжиниринг