Clear Sky Science · ru
Терапия стимуляции спинного мозга при нарушениях походки при болезни Паркинсона: двойное слепое рандомизированное пилотное исследование с открытым продлением
Когда ходьба превращается в ежедневную борьбу
Многие люди с болезнью Паркинсона замечают, что ходьба из автоматического действия превращается в постоянную проблему. Казалось бы, ноги вдруг «приклеиваются» к полу, из‑за чего повседневные дела становятся рискованными и утомительными. В этом исследовании задали простой, но важный вопрос: может ли небольшое имплантированное устройство, посылающее мягкие электрические импульсы в спинной мозг, безопасно помочь таким пациентам ходить лучше и стоит ли испытывать этот подход в более крупных испытаниях?
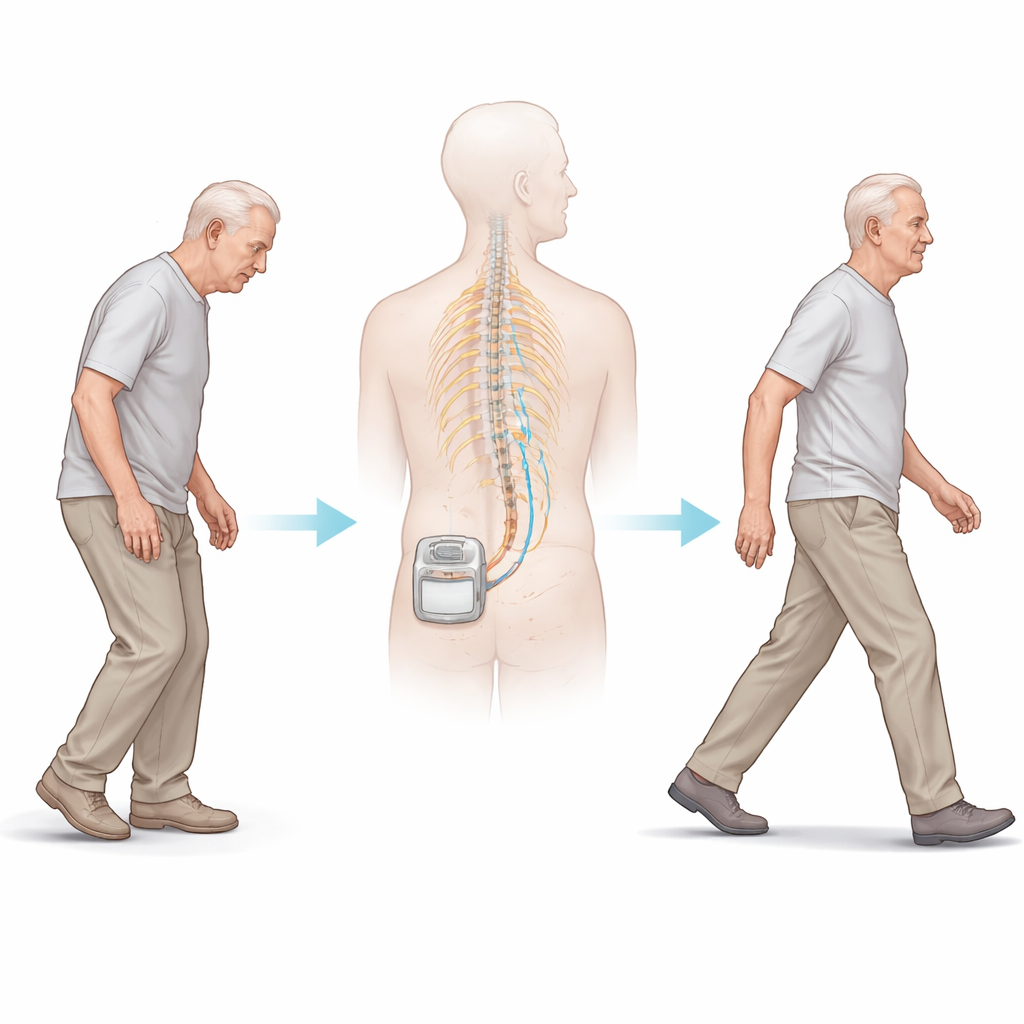
Новое применение для терапии боли
Стимуляция спинного мозга уже применяется для облегчения тяжёлой хронической боли. Хирурги помещают тонкий электрод вдоль позвоночника и подключают его к имплантируемому генератору импульсов под кожей. Устройство посылает крошечные электрические вспышки по нервным путям. За последнее десятилетие врачи отмечали, что некоторые пациенты с болезнью Паркинсона, получавшие такую терапию от болей в спине, казались более уверенными в ходьбе. Это наблюдение вдохновило исследование STEP-PD, в котором тестировали определённый «burst» (импульсный) режим стимуляции, разработанный так, чтобы не вызывать ощущения покалывания, что позволило честно сравнивать реальную стимуляцию с имитацией (устройство выключено).
Как было организовано исследование
Исследователи набрали людей с болезнью Паркинсона, у которых сохранялось изнуряющее «застревание» при ходьбе несмотря на оптимальную медикаментозную терапию. После операции по имплантации стимулятора в средней части спины двенадцать участников вступили в шестимесячную двойную слепую фазу: половина была случайным образом отнесена к получению импульсной стимуляции, а половина — к состоянию «выключено». Ни пациенты, ни врачи, проводившие осмотры, не знали, кто к какой группе относился. Затем все участники продолжили ещё шесть месяцев в открытой фазе, где все получали активную стимуляцию. На протяжении всего времени команда измеряла равновесие и ходьбу с помощью стандартных шкал двигательных расстройств, простых тестов ходьбы, домашних сенсоров и опросников о мобильности и качестве жизни. С помощью двух типов ПЭТ‑сканирования отслеживали изменения в активности мозга и в химической сигнальной системе, связанной с вниманием и движением.
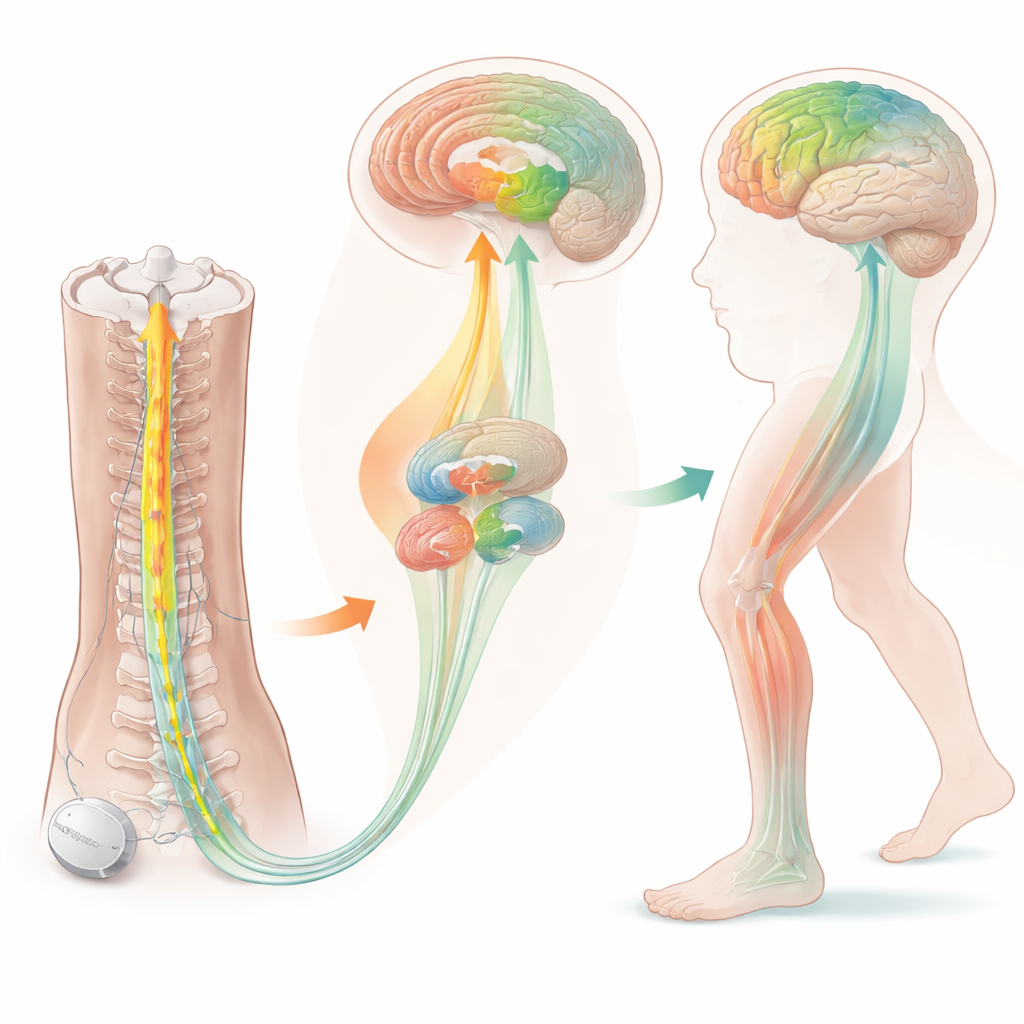
Безопасность прежде всего, сигналы — вторично
Исследование показало, что этот тип стимуляции спинного мозга в целом был безопасен и приемлем. Большинство проблем были связаны с самой операцией — временная боль, отёк или необходимость репозиционирования электрода — и эти осложнения разрешались без долговременного вреда. Важный вывод: основной клинический тест — суммарная шкала проблем с равновесием и ходьбой — не показал значимого улучшения после шести месяцев импульсной стимуляции по сравнению с группой имитации. Тем не менее при более детальном анализе были найдены обнадеживающие признаки: жёсткость и замедленность в ногах улучшались во время стимуляции, а детальная шкала «нижняя часть тела и походка» снижалась со временем, особенно после полного года лечения. При сравнении этих пациентов с подобной группой из большой базы данных по Паркинсону те, кто не получал стимуляцию, как правило, ухудшались в течение года, тогда как у получавших стимуляцию наблюдалась относительная стабилизация или небольшое улучшение.
Что показали сканы мозга
Мозговое сканирование дало представление о том, как может работать стимуляция. До лечения у людей с «застреванием» при ходьбе наблюдалась необычная активность в областях мозга, вовлечённых в внимание и контроль движения, включая правую лобную долю и узел, называемый передней островковой долей. После нескольких месяцев стимуляции использование глюкозы в таламусе — перевалочном пункте, помогающем координировать движение — уменьшилось, и сигналы от некоторых холинергических (использующих ацетилхолин) окончаний в моторных и привлекающих внимание областях также снизились. Вместо того чтобы указывать на повреждение, эти сдвиги, вероятно, отражают нормализацию чрезмерно активных цепей, которыми мозг компенсировал проблемы с ходьбой. Эти биологические изменения соответствовали постепенному уменьшению жёсткости и замедленности ног, наблюдавшемуся в клинических тестах.
Почему нужны более крупные и продуманные испытания
С точки зрения непрофессионала вывод смешанный, но обнадёживающий. Это небольшое хорошо контролируемое исследование показало, что импульсная стимуляция спинного мозга не даёт явного краткосрочного решения проблем с ходьбой при болезни Паркинсона, поэтому пока не может быть рекомендована как доказанная терапия походки. Однако терапия оказалась безопасной, а со временем, по‑видимому, уменьшала жёсткость и замедленность в ногах; сканы мозга указывают на существенные сдвиги в сетях движения. Исследование также выявило важные уроки по дизайну — кого включать, какие шкалы наиболее чувствительны, как долго проводить лечение — которые помогут в планировании более крупных и решающих испытаний. Иными словами, хотя стимуляция спинного мозга ещё не является «лекарством» для ходьбы, она может стать частью будущего арсенала мер, позволяющих людям с Паркинсоном дольше и безопаснее сохранять способность передвигаться.
Цитирование: Terkelsen, M.H., Hvingelby, V.S., Johnsen, E.L. et al. Spinal cord stimulation therapy for gait impairment in Parkinson’s disease: a double-blinded, randomised feasibility trial with an open extension. Nat Commun 17, 2168 (2026). https://doi.org/10.1038/s41467-026-68782-w
Ключевые слова: Болезнь Паркинсона, нарушение походки, стимуляция спинного мозга, глубокие мозговые сети, нейромодуляция