Clear Sky Science · ru
Структурная основа и патологические последствия димерного корового комплекса ERAD OS9-SEL1L-HRD1
Клеточная служба уборки под микроскопом
Внутри каждой нашей клетки работает оживлённая фабрика, превращающая генетические инструкции в функциональные белки. Как и на любой фабрике, здесь случаются ошибки. Когда белки неправильно сворачиваются, они могут засорять систему и способствовать развитию болезней. В этом исследовании подробно рассматривается одна из главных машин контроля качества в клетке — комплекс SEL1L‑HRD1 — чтобы показать его трёхмерную структуру и объяснить, как небольшие генетические изменения могут нарушить эту машину и потенциально привести к заболеваниям человека.
Скрытая конвейерная лента в клетке
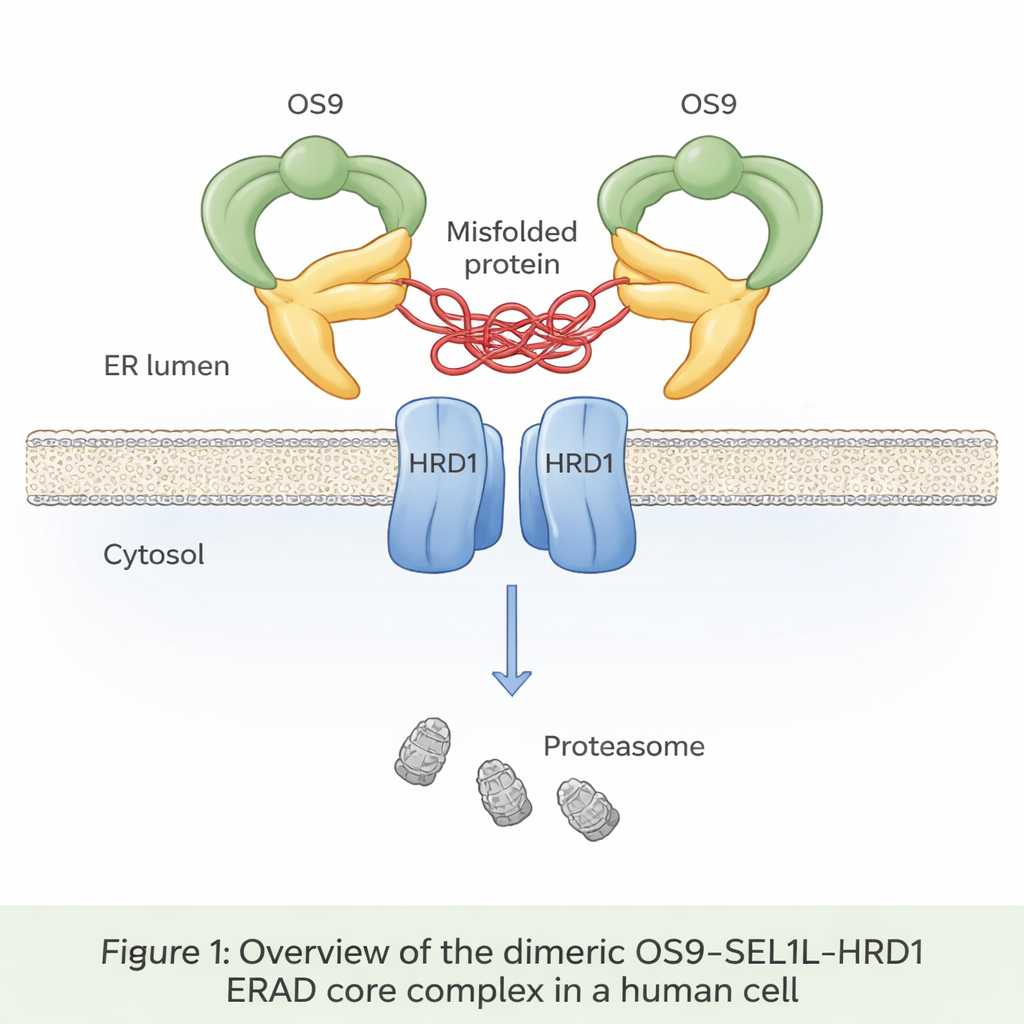
До трети всех недавно синтезированных белков попадают в отделение, называемое эндоплазматическим ретикулумом (ЭР), где их сворачивают и проверяют. Неправильно свернувшиеся белки обычно распознаются, вытягиваются обратно из ЭР и уничтожаются в процессе, известном как связанная с ЭР деградация белков (ER‑associated degradation, ERAD). В центре одного из основных путей ERAD находятся трое белков: OS9, SEL1L и HRD1. OS9 выполняет роль сенсора для дефектных, сахаром меченых белков; SEL1L служит каркасом; а HRD1 помечает обречённые белки небольшими флагами убиквитина, направляя их на утилизацию протеасомами клетки. Однако до сих пор никто не видел в атомных деталях, как эти три компонента сочетаются между собой в человеческих клетках.
Раскрывая форму ядра машины
Авторы использовали криоэлектронную микроскопию — метод, позволяющий визуализировать замороженные молекулы с почти атомным разрешением — чтобы увидеть очищенный из человеческих клеток комплекс OS9‑SEL1L‑HRD1. Они обнаружили, что он образует димер — по сути две идентичные копии, соединённые друг с другом — а не существует как отдельные одиночные единицы. На стороне люмена ЭР (внутри ЭР) два молекулы OS9 и два молекулы SEL1L собираются в кольцо, напоминающее крабьи клешни, с центральным отверстием, похоже предназначенным для захвата неправильно свернувшихся белков. В мембране сами две молекулы HRD1 образуют пару, формируя общий канал. Такая организация размещает «клешню» прямо над «дверью» HRD1, создавая непрерывный путь для перемещения дефектных белков из люмена ЭР через мембрану в цитозоль для последующей деградации.
Как крошечные изменения ломают большую систему
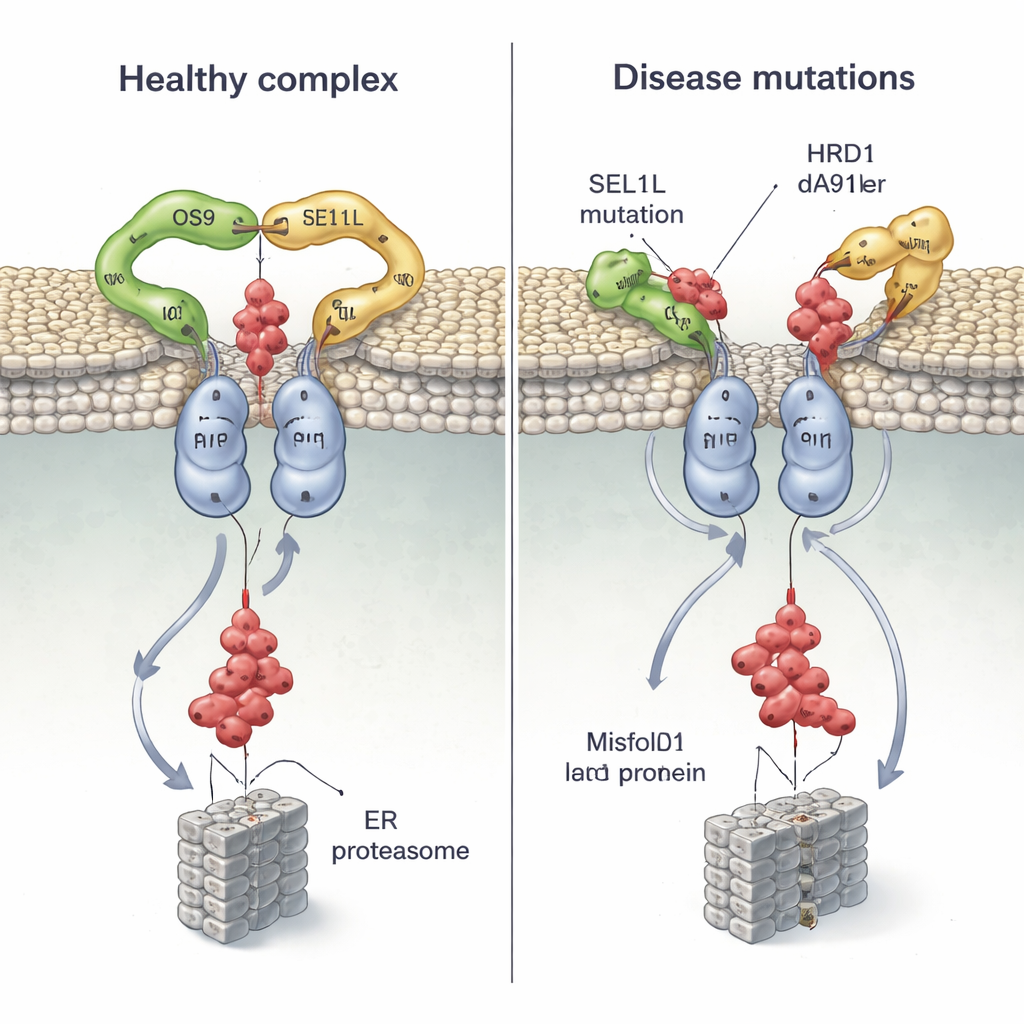
Поскольку мутации в SEL1L и HRD1 были обнаружены у пациентов с тяжёлыми нарушениями нейроразвития и другими расстройствами, исследователи нанесли несколько вариантов, связанных с болезнями, на их структуру и проверили их поведение в клетках. Две мутации в SEL1L, G585D и S658P, располагаются непосредственно в точках контакта с OS9 и HRD1 соответственно. В клеточных экспериментах G585D почти полностью лишала SEL1L способности связываться с OS9, тогда как S658P значительно ослабляла её взаимодействие с HRD1; сочетание обеих мутаций фактически разрушало коревой комплекс, при этом другие взаимодействующие белки оставались нетронутыми. В результате клетки испытывали трудности с пометкой и удалением неправильно свернувшегося предшественника гормона, что позволяло дефектным белкам задерживаться.
Болезнетворная мутация в мембранном канале
Структура также показывает, что третий трансмембранный сегмент HRD1 является ключевым интерфейсом, где две молекулы HRD1 встречаются, чтобы образовать канал. Исследователи встроили цистеиновые «ручки» в определённых позициях и использовали химическое сшивание, чтобы подтвердить, что эти области находятся в близком контакте в живых клетках, доказав, что HRD1 действительно димеризуется in vivo. Когда они нарушили один высокосохранённый остаток (T93) в этом интерфейсе, димер распался и активность ERAD рухнула, хотя комплекс по‑прежнему мог собираться с OS9 и SEL1L. Затем они изучили недавно обнаруженный вариант у пациента, HRD1 A91D, найденный у ребёнка с сердечно‑лёгочными проблемами. Эта замена, также лежащая в интерфейсе димера, примерно наполовину снизила димеризацию HRD1 и серьёзно нарушила уничтожение неправильно свернувшихся белков, опять же не меняя общего связывания партнёров.
Новый взгляд на контроль качества белков и болезни
Сочетая структурную биологию с клеточными тестами, эта работа показывает, что комплекс OS9‑SEL1L‑HRD1 функционирует как парный, димерный механизм: ловушка в форме клешни, связанная с общим каналом, который транспортирует дефектные белки из ЭР. Мутации, ослабляющие захват клешни или дестабилизирующие пару HRD1, не просто снижают эффективность — они фактически могут заклинить систему, позволяя повреждённым белкам накапливаться и способствовать заболеваниям человека. Для неспециалистов главный вывод таков: даже однобуквенные изменения в нашей ДНК могут тонко исказить форму жизненно важных клеточных машин, с далеко идущими последствиями для развития мозга, иммунитета и функции органов.
Цитирование: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Ключевые слова: контроль качества белков, эндоплазматический ретикулум, ERAD, комплекс SEL1L-HRD1, свертывание белков