Clear Sky Science · ru
Профилирование удаления экзонов в отдельных клетках выявляет события сплайсинга, формирующие экспрессию генов и динамику состояния клеток
Как крошечные правки РНК могут изменить поведение клетки
Наши клетки постоянно считывают и сплайсят РНК-инструкции, чтобы решить, какие белки синтезировать и как реагировать на стресс, расти или делиться. В этом исследовании показано, что изменение очень маленьких фрагментов этих РНК-посланий — отдельных сегментов, называемых экзонами — может существенно перестроить активность генов и даже сместить прохождение клеточного цикла. Работа представляет мощный инструмент, который позволяет учёным одновременно сканировать многие такие тонкие решения сплайсинга по единицам клетки, открывая новые пути для понимания болезней и поиска лекарственных мишеней.
Вырезание отдельных «слов» из генетического сценария
Гены записаны в виде длинных участков ДНК, но клетки не считывают их напрямую. Вместо этого они вырезают и склеивают вместе более мелкие блоки, называемые экзонами, чтобы собрать РНК-послание. Выбирая, какие экзоны сохранить, клетки могут получать несколько вариантов белка из одного гена, подобно тому как из одного исходного материала можно смонтировать разные версии фильма. Многие заболевания, включая рак и аутизм, связаны с ошибками в этом процессе, но для большинства экзонов мы ещё не знаем, какую функцию они выполняют. Авторы поставили цель исправить это, создав крупномасштабную систему, которая может удалять конкретные экзоны из множества генов и затем наблюдать, в тысячах отдельных клеток одновременно, как эти изменения влияют на внутреннюю сеть клетки.
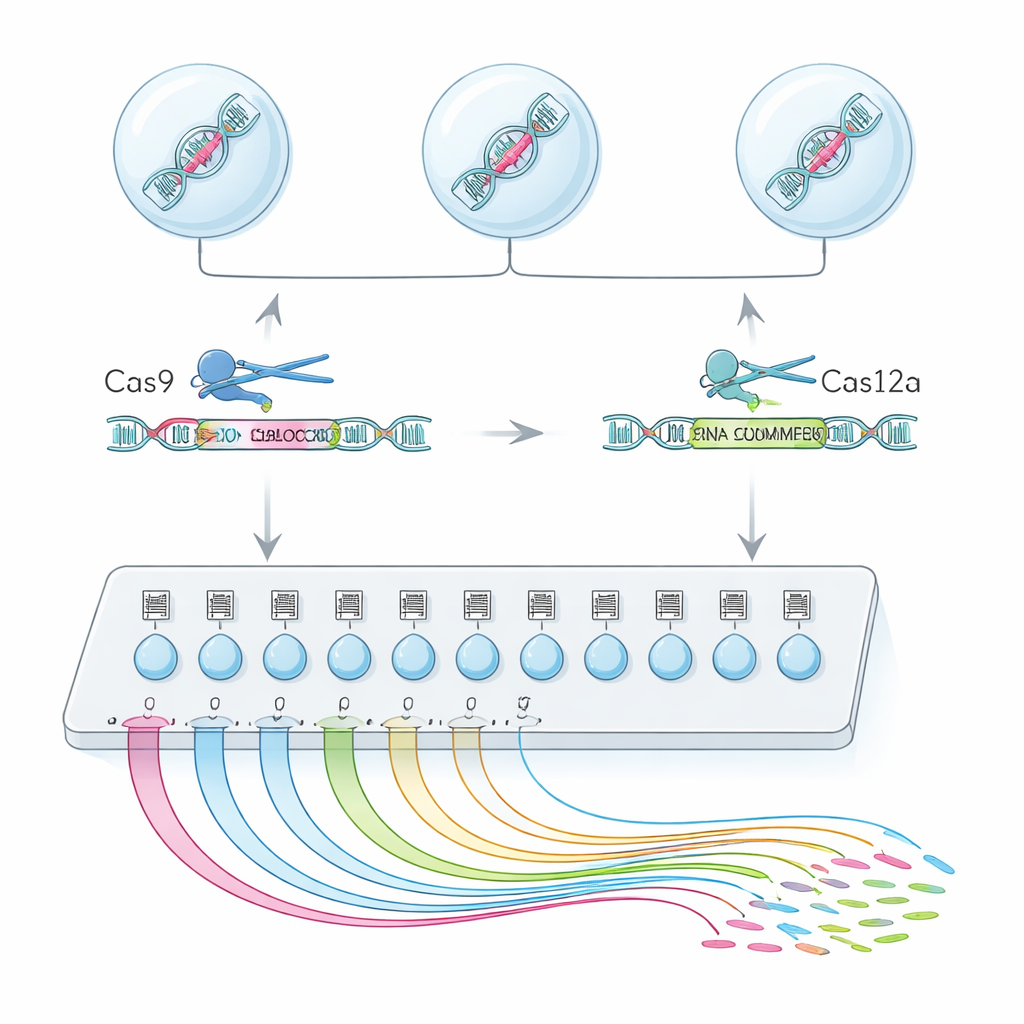
Поисковая система для функций экзонов на уровне одиночных клеток
Для этого команда объединила два фермента редактирования генома, Cas9 и Cas12a, в гибридную платформу под названием CHyMErA. Каждый фермент направляется к ДНК короткими РНК «адресами». Направляя оба фермента так, чтобы они разрезали сразу перед и сразу после выбранного экзона, можно аккуратно удалить этот сегмент, не повреждая остальную часть гена. Новый метод, scCHyMErA-Seq, связывает это точное удаление с технологией секвенирования РНК одиночных клеток. РНК каждой клетки захватывается в капле вместе со штрих-кодом и направляющими РНК, указывающими, какой экзон был удалён. Последующее секвенирование выявляет для десятков тысяч клеток и редактирование, которое получила каждая клетка, и подробную картину генов, которые она включила или выключила.
Проектирование инструмента, чтобы увидеть оба «лезвия» ножниц
Ключевой проблемой было надёжно обнаруживать направляющие Cas12a наряду с Cas9 в одном эксперименте на отдельных клетках. Первые варианты либо не улавливали направляющие Cas12a, либо снижали эффективность редактирования. Исследователи решили эту проблему, тщательно переработав последовательность рукояти Cas12a, удалив фрагменты, которые преждевременно останавливают транскрипцию, а также добавив небольшой стабилизирующий элемент РНК и целевой шаг амплификации. Эти изменения повысили способность обнаруживать оба направляющих примерно в 90 процентах клеток, при сохранении высокой эффективности удаления экзонов. С оптимизированной настройкой авторы просcreenировали 224 альтернативных экзона в 161 гене человеческих клеток, профилировав более 200 000 качественных одиночных клеток.
Выявление экзонов, контролирующих генетические программы и клеточные циклы
Когда команда сравнила активность генов в отредактированных клетках и в контроле, почти половина протестированных экзонов вызвала значительные сдвиги в сотнях других генов. Экзоны из генов, участвующих в обработке РНК и транскрипции, как правило, группировались вместе, формируя похожие отпечатки экспрессии и раскрывая общие биологические пути, такие как сборка рибосом или распад РНК. В некоторых случаях удаление одного экзона давало понятный и интерпретируемый эффект: удаление экзона в генах TAF5 или LSM11 нарушало правильную обработку гистоновых РНК, что приводило к необычному накоплению полиаденилированных гистоновых сообщений. Набор данных также выделил десятки экзонов, потеря которых меняла распределение клеток по стадиям клеточного цикла, связывая конкретные события сплайсинга с решениями о том, когда клетка приостанавливается, копирует ДНК или готовится делиться.
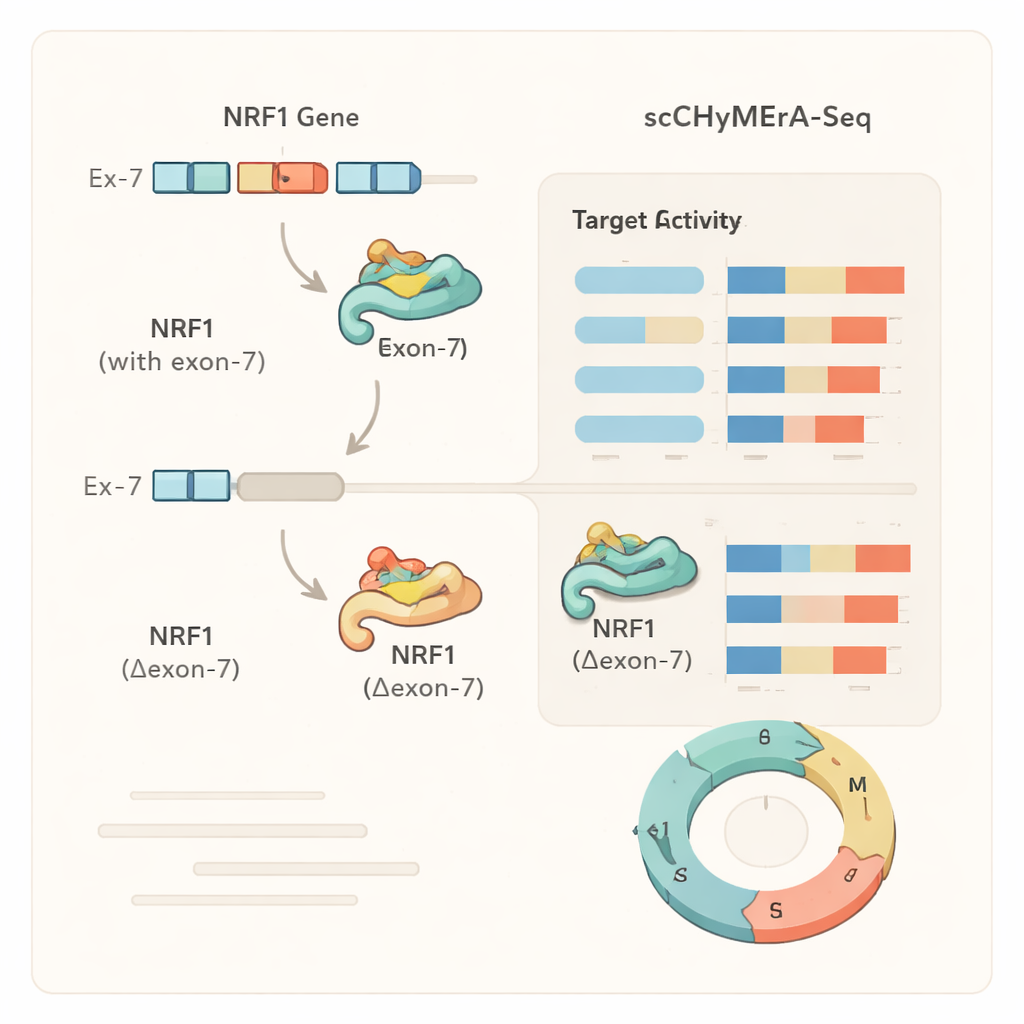
Кейс: один экзон, который настраивает главный регулятор
Одним из ярких примеров стал экзон 7 в гене NRF1, транскрипционном факторе, контролирующем множество генов, связанных с энергетическим метаболизмом клетки. Этот экзон частично перекрывается с областью связывания ДНК у NRF1. При удалении экзона 7 сотни управляемых NRF1 генов изменяли свою активность, а детальные эксперименты показали, что укороченный белок NRF1 значительно хуже связывается с целевыми промоторами в геноме. Авторы также выявили специфический фактор сплайсинга, SRSF3, который способствует включению этого экзона, что выявляет цепочку от фактора сплайсинга через выбор экзона в NRF1 к широким изменениям генетических программ и метаболизма клетки. Подобный анализ показал, что для некоторых генов удаление экзона имитирует полный нокаут гена, тогда как для других даёт более тонкую, зависящую от состояния клеточные изменения, что указывает на то, что альтернативные экзоны могут деликатно модулировать поведение белков, а не просто включать или выключать их.
Почему это важно для здоровья и будущих терапий
Для неспециалиста главный вывод в том, что клетки полагаются на включение или пропуск очень коротких сегментов РНК, чтобы точно настраивать работу генов, и что эти тонкие корректировки могут смещать крупные признаки, такие как скорость деления клеток или их реакция на стресс. Платформа scCHyMErA-Seq работает как высокопроизводительный лабораторный тест для этих выборов сплайсинга, позволяя определить, какие экзоны действительно функциональны и как они перестраивают состояния клетки. Поскольку многие виды рака и неврологические расстройства связаны с нарушенным сплайсингом экзонов или изменёнными транскрипционными факторами, этот подход может помочь приоритезировать варианты сплайсинга для целевой терапии лекарствами или РНК-терапиями и дать дорожную карту для понимания того, как небольшие правки в генетическом сценарии приводят к большим изменениям в поведении клеток.
Цитирование: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Ключевые слова: альтернативный сплайсинг, секвенирование РНК одиночных клеток, CRISPR-скрининг, регуляция генов, клеточный цикл