Clear Sky Science · ru
Нанозим, имитирующий гранзим B, для таргетных противораковых приложений в нановезикулах
Переосмысление клеток-убийц организма
Наша иммунная система располагает специализированными клетками, которые могут выискивать и уничтожать раковые клетки, но во многих солидных опухолях они испытывают трудности с проникновением, быстро истощаются или атакуют неверные мишени. В этом исследовании описана полностью искусственная наноразмерная система, которая имитирует одно из мощнейших орудий иммунной системы и доставляет его непосредственно внутрь опухолевых клеток. Работа важна тем, что указывает путь к методам лечения рака, которые ведут себя подобно живым иммунным клеткам, но изготовлены из стабильных, управляемых материалов, а не из хрупких человеческих клеток.
Превращение природного асассина в чертеж
Цитотоксические Т-клетки, тип лейкоцитов, уничтожают опасные клетки с помощью фермента под названием гранзим B. Узнав цель, они проделывают маленькие отверстия в её мембране и вводят гранзим B, который запускает программы самоуничтожения внутри клетки. Эта стратегия лежит в основе современных методов, таких как CAR-T, способных излечивать некоторые кровяные раки. Однако в солидных опухолях CAR-T‑клетки часто не справляются: они не могут достичь всех областей опухоли, истощаются или по ошибке поражают здоровые ткани. Авторы поставили вопрос, можно ли создать неживое наноустройство, которое воспроизводит ключевую функцию гранзима B — включение механизмов самоуничтожения клетки — без опоры на живые Т-клетки.
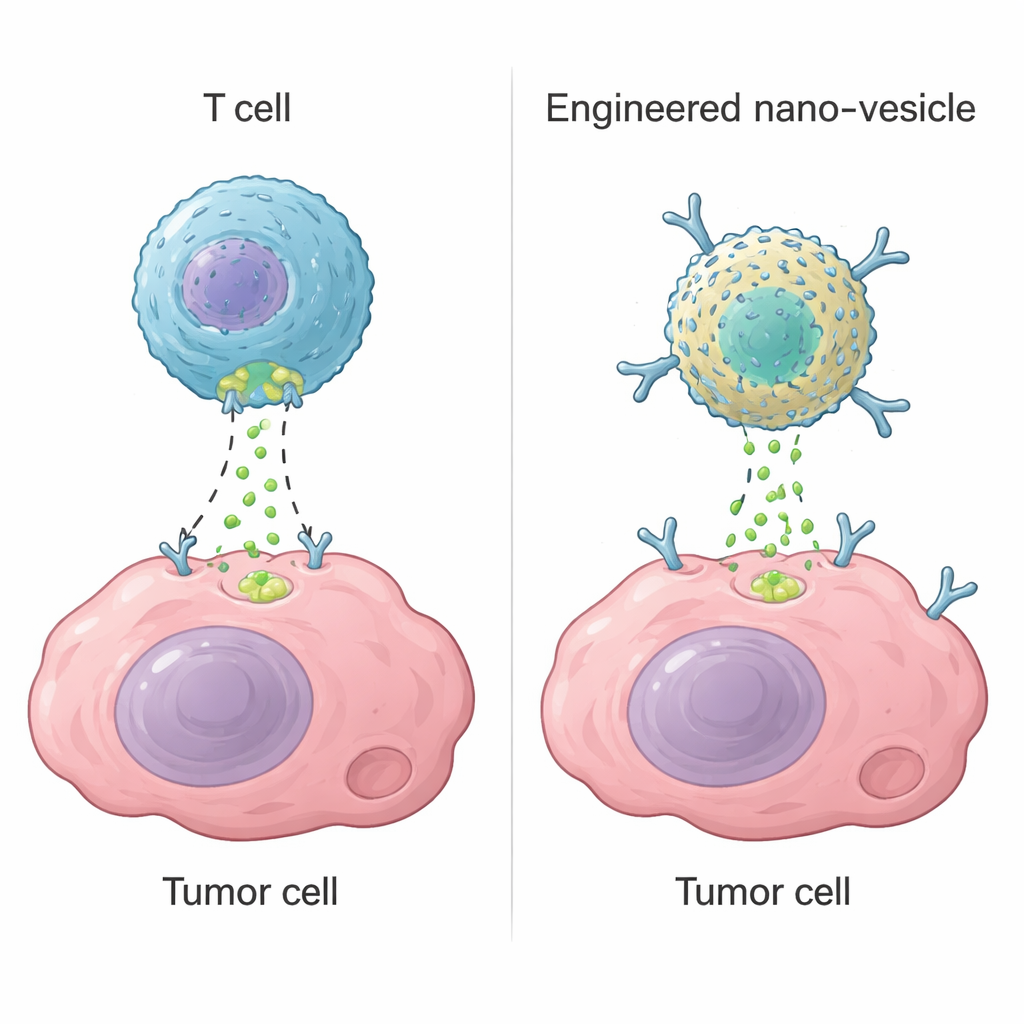
Проектирование крошечного искусственного фермента
Команда начала с ферритина, природного белка, который образует полые наноклетки и легко производится в больших количествах. Привязав ионы палладия к человеческому ферритину, они создали «нанозим» с ферментоподобным поведением. Тщательные структурные исследования показали, что два атома палладия располагаются в специфическом кармане на поверхности белка, удерживаемые аминокислотами, содержащими серу и азот, а также молекулами воды. Этот бинокулярный металлический центр действует как искусственный сайт расщепления, который распознаёт ту же короткую последовательность, на которую нацелен гранзим B, в ключевой мишени — каспазе‑3. В лабораторных тестах нанозим эффективно разрезал каспазу‑3 в нужном месте, активируя её, при этом игнорируя близкородственные белки. Искусственный фермент был немного менее эффективен, чем природный гранзим B, но заметно более стабилен в широком диапазоне температур и кислотности.
Контрабанда нанозима в опухолевые клетки
Ферменты вроде гранзима B работают только если попадают внутрь опухолевых клеток. Для этого исследователи поместили свой палладий‑ферритиновый нанозим внутрь липидных нановезикул — небольших мягких пузырьков, состоящих из молекул, похожих на жиры. Затем они покрыли эти везикулы фрагментами антител, которые распознают HER2 — белок, часто переэкспрессируемый в клетках рака молочной железы и мочевого пузыря. Когда такие «маскированные» везикулы встречают клетки с высоким уровнем HER2, они прочно связываются и сливаются с клеточной мембраной, что позволяет грузу‑нанозиму проникнуть прямо в цитоплазму вместо того, чтобы оказаться в отсеках утилизации и разрушиться. Микроскопия показала, что везикулы задерживаются на поверхности клетки, в то время как нанозим диффундирует внутрь, создавая предпосылки для контролируемого самоуничтожения изнутри.
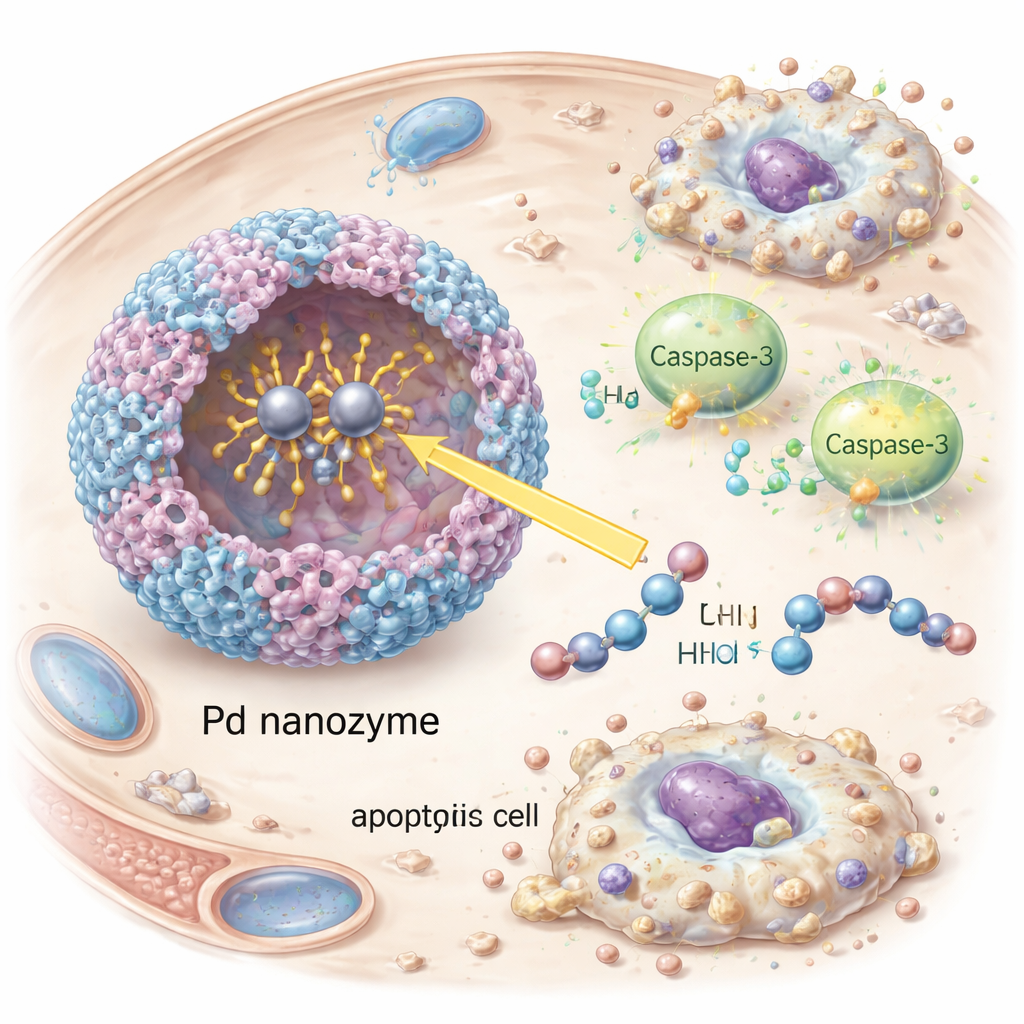
Точное запускание самоуничтожения раковых клеток
Оказавшись внутри раковых клеток, нанозим активировал каспазу‑3, центрального исполнителя программируемой смерти клетки. Исследователи наблюдали появление активированной каспазы‑3 и её нисходящей мишени PARP, а также явные признаки апоптоза — уменьшение и фрагментацию клеток — в культурах HER2‑позитивных опухолевых клеток. Подавление каспазы‑3 с помощью РНК‑интерференции резко снизило гибель клеток, что подтвердило зависимость эффекта от этого пути, а не от неспецифического повреждения. У мышей с HER2‑позитивными опухолями антителами украшенные везикулы дольше циркулировали в крови, сильнее накапливались в опухолях и более эффективно замедляли рост опухоли по сравнению с везикулами без целевых антител или без нанозима. Важно, что у обработанных животных не наблюдалось явной потери веса, отклонений в анализах крови или повреждений в основных органах, что указывает на благоприятный профиль безопасности в этих ранних испытаниях.
Что это может значить для будущей онкологической помощи
Для неспециалистов главный вывод состоит в том, что исследователи создали крошечное неживое устройство, которое ведёт себя как ключевая часть механизма иммунной системы по уничтожению рака. Вместо того чтобы генетически модифицировать живые Т‑клетки, они разработали стабильный нанозим, который активирует тот же переключатель самоуничтожения внутри опухолевых клеток, и поместили его в умную доставляющую оболочку, нацеленную на определённые виды рака. Хотя до применения у людей ещё далеко, этот подход предлагает гибкую платформу: в принципе, покрытие антителами можно заменить, чтобы нацелиться на другие опухолевые маркеры, а искусственный фермент — дополнительно оптимизировать. Исследование демонстрирует многообещающий путь к бесклеточной иммунотерапии, при которой тщательно разработанные наноматериалы, а не живые иммунные клетки, используются для поиска и уничтожения солидных опухолей.
Цитирование: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Ключевые слова: наномедицина против рака, иммунотерапия, гранзим B, нанозим, опухоли с экспрессией HER2