Clear Sky Science · ru
Биоортогональная химия, активируемая реактивными формами кислорода в живых системах, реализованная с помощью боронат-защищённых дигидротетразинов
Превращая клеточный стресс в точный переключатель
Многие заболевания — от рака до сердечных нарушений — сопровождаются окислительным стрессом в клетках, в результате чего образуются высокие уровни реактивных форм кислорода, таких как перекись водорода. В этом исследовании показано, как химики могут использовать сам этот стресс в качестве встроенного переключателя, включающего мощные терапии только там, где они нужны. Проектируя компоненты лекарств, которые реагируют только в таких стрессовых условиях, авторы стремятся убивать опухолевые клетки или разрушать вредные белки, пощадив при этом здоровые ткани.
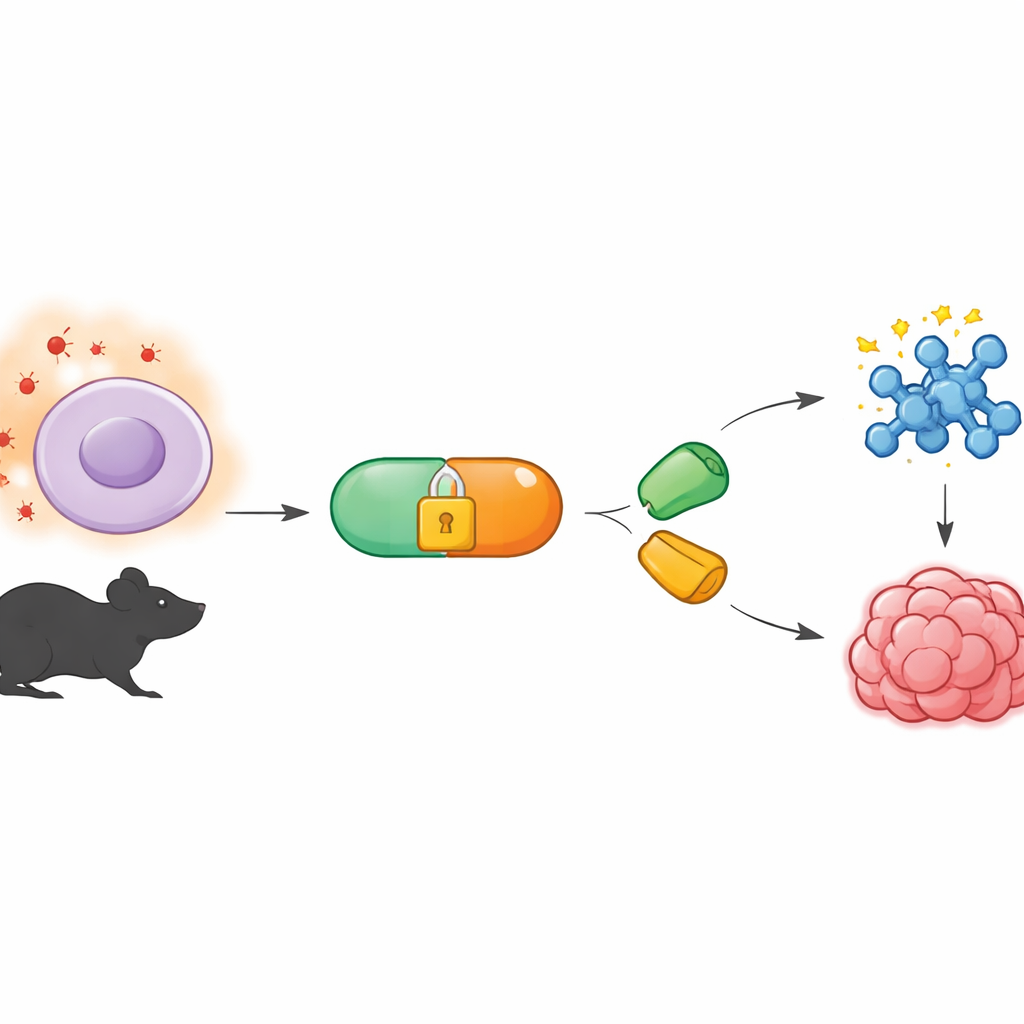
Химический инструмент, работающий незаметно на заднем плане
Работа опирается на область, называемую биоортогональной химией, которая разрабатывает реакции, способные протекать в живых организмах, не нарушая нормальную биологию. Популярный вариант использует специальные пары молекул, которые соединяются как детали пазла даже в тесной внутренней среде клетки. Один из партнёров, тетразин, реагирует очень быстро с подходящим «кольцевым» партнёром, известным как диенофил. До сих пор многие такие реакции контролировали с помощью света или добавления ферментов. Авторы же хотели создать систему, которая прислушивается к собственным химическим сигналам организма — в частности, к необычно высоким уровням реактивных форм кислорода, характерным для опухолей и других поражённых тканей.
Создание чувствительного к ROS химического триггера
Для этого команда создала предшественники тетразина, которых они называют BTz, химически «запертые» в капсуле так, чтобы оставаться неактивными в нормальных тканях. Клетка защёлки сформирована из боронатной группы, связанной с восстановленной формой тетразина. Когда перекись водорода в дефиците, BTz стабильны в воде и в клеточных культурах в течение многих часов. Но когда перекись водорода содержится в избытке — на уровнях, сопоставимых с измеренными в опухолях — боронатная группа окисляется и разрушается в последовательности самораспада, открывая активный тетразин. В пробирочных экспериментах поэтапное повышение концентрации перекиси водорода вызывало соответствующее увеличение образования активного тетразина, подтверждая, что реакция селективна и сильно зависит от дозы.
Использование клеточного стресса для уничтожения белка, управляющего раком
Исследователи сначала применили свой переключатель для управления современной стратегией лекарственной терапии — направленным разрушением белков. Они прикрепили BTz к талидомиду, малой молекуле, способной привлечь ферментный комплекс, маркирующий белки для утилизации. В раковых клетках этот BTz–талидомид оставался дремлющим, пока уровни перекиси водорода не повышались, после чего капсула открывалась и формировался активный тетразин. Этот тетразин затем соединялся с соответствующим партнёром, связанным с лекарством, нацеленным на BRD4, собирая крупную «химеру», которая направляла белок BRD4 к механизмам утилизации клетки. В линиях клеток рака лёгкого и шейки матки уровни BRD4 резко снижались только при наличии всех компонентов и перекиси водорода; блокирование реактивных форм кислорода предотвращало деградацию, что подчёркивает, что процесс действительно активируется стрессом.
Доставка токсичного препарата только туда, где он нужен
Далее команда превратила ту же химию в точную систему доставки для доксорубицина — мощного, но кардиотоксичного химиопрепарата. Они связали доксорубицин со структурой-диенофилом так, чтобы он находился в неактивной форме профармацевтического соединения. Когда этот профармакон попадал на BTz в среде, богатой перекисью водорода, вновь образованный тетразин реагировал с кольцом в процессе «click-to-release», соединяя части и выбрасывая свободный доксорубицин. В культурах клеток колоректального рака эта двухступенчатая система убивала клетки почти так же эффективно, как и свободный препарат, но только при наличии перекиси водорода; без неё клетки оставались в основном невредимыми. Проще устроенный перекисно-водородчувствительный профармакон доксорубицина оказался менее эффективен и менее селективен в этих тестах, что подчёркивает преимущество раздельного сенсора и механизма высвобождения в двух согласованных шагах.
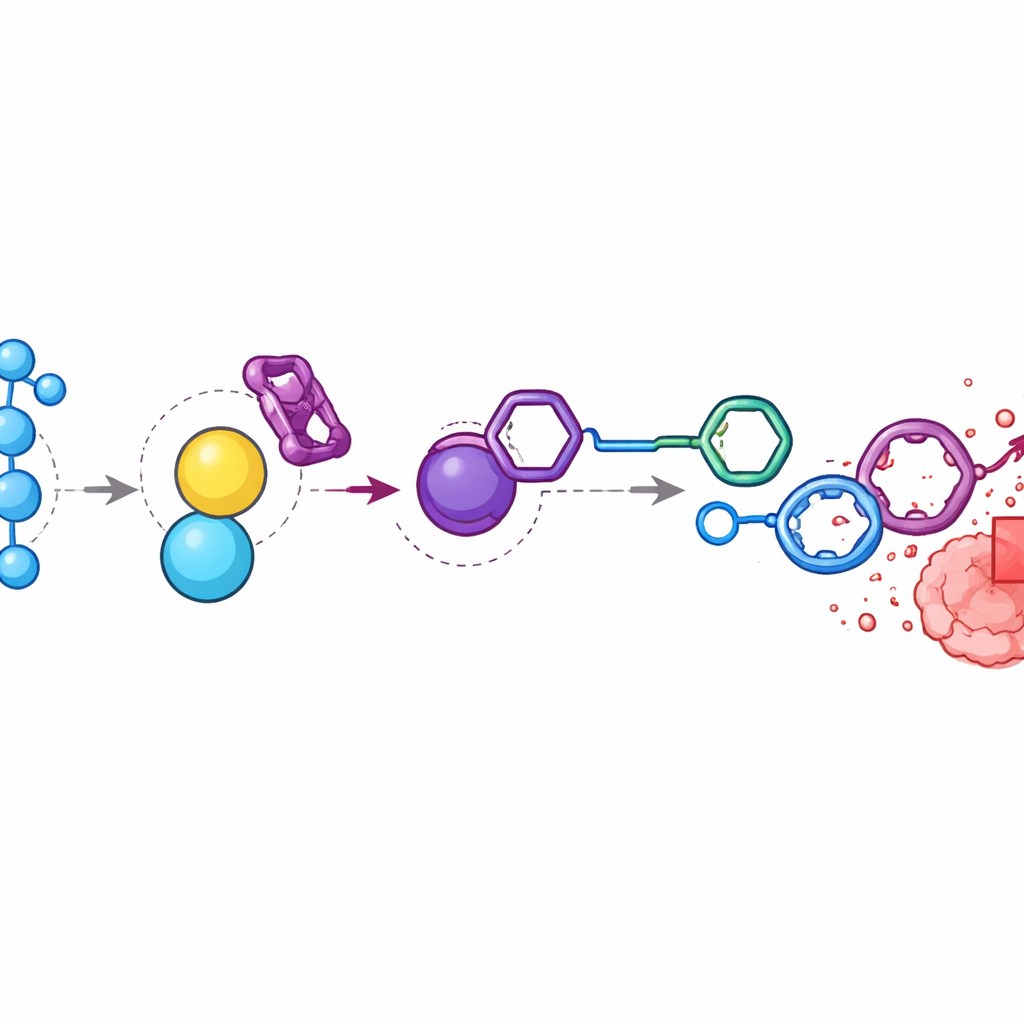
Фокусирование химиотерапии внутри опухолей
У мышей с колоректальными опухолями исследователи обнаружили, что уровни перекиси водорода в опухолях были почти в девять раз выше, чем в окружающей мышечной ткани. Они вводили профармакон доксорубицина и BTz в заданной последовательности, чтобы оба компонента накопились в районе опухоли. Химический анализ показал, что компоненты в значительной степени исчезают из крови и органов, но внутри опухолей образуется высокий уровень свободного доксорубицина. По сравнению с животными, получавшими стандартный доксорубицин, те, кого лечили активируемой системой, демонстрировали похожее или лучшее сокращение опухоли при сохранении стабильной массы тела и без тяжёлой токсичности, наблюдавшейся при больших дозах препарата. Когда команда разрушила сигнал перекиси водорода, вводя каталазу — фермент, удаляющий перекись водорода — высвобождение лекарства и избирательное накопление в опухоли существенно снижались, подтверждая, что ключевым фактором является окислительный стресс в месте опухоли.
От сигнала стресса к точной терапии
В целом это исследование демонстрирует универсальную химическую платформу, превращающую маркер заболевания — избыток реактивного кислорода — в точный регулятор мощных реакций в живых системах. Держа реакционный тетразиновый «хват» запертым до встречи с перекисью водорода, подход позволяет создавать сложные терапии прямо в организме только там, где они нужны, будь то разрушение способствующего раку белка или высвобождение токсичного препарата внутри опухоли. Поскольку окислительный стресс также играет роль при старении, воспалении, диабете и нейродегенеративных расстройствах, аналогичные реакции, чувствительные к стрессу, в конечном счёте могут быть адаптированы для многих состояний, где важны точность и безопасность.
Цитирование: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Ключевые слова: биоортогональная химия, реактивные формы кислорода, лигирование тетразина, целенаправленная доставка лекарств, PROTAC