Clear Sky Science · ru
Гомотипичное мембранное электрохимическое микрофлюидное исследование внеклеточных везикул для точной диагностики рака
Преобразование собственной брони рака в диагностический инструмент
Мембраны, окружающие раковые клетки, усыпаны характерными молекулярными «флажками». В этом исследовании показано, как учёные могут снимать эту броню, наносить её на крошечные золотые чипы и затем использовать для «выуживания» характерных частиц из крови. В результате получается высокочувствительный анализ крови, который может показать не только наличие рака молочной железы, но и его подтип — информация, критически важная для выбора правильного лечения.
Почему имеет значение подтип рака молочной железы
Рак молочной железы — это не одно заболевание. Опухоли делят на подтипы, такие как положительные по эстрогеновому рецептору (ER+), HER2-положительные и тройного отрицательного типа; каждый из них по‑разному реагирует на гормональную терапию, таргетные препараты или химиотерапию. Сегодня врачи обычно определяют подтип по тканевой биопсии, взятой непосредственно из опухоли. Эта процедура инвазивна, её нельзя проводить часто, и она может не уловить изменения, происходящие по мере эволюции болезни. Анализ крови, способный отслеживать сигнатуры подтипов с течением времени, позволил бы врачам раньше и точнее корректировать терапию.
Крошечные посланцы, плавающие в крови
Раковые клетки постоянно сбрасывают в кровь наносекундные пузырьки — внеклеточные везикулы (EV). Везикулы переносят белки, липиды и генетический материал, тесно похожие на содержимое родительских клеток, что делает их привлекательными кандидатами для «жидкостных биопсий». Но есть проблема: EV из разных подтипов рака молочной железы могут выглядеть очень похоже, если смотреть только на один‑два белка. Существующие тесты либо нацелены на общие маркеры — что затрудняет различение подтипов, — либо опираются на сложные генетические анализы, которые медленны и могут давать ложные результаты. Авторы поставили задачу считать более полный молекулярный отпечаток поверхности везикул простым и надёжным способом.
Создание биомиметической «удочки»
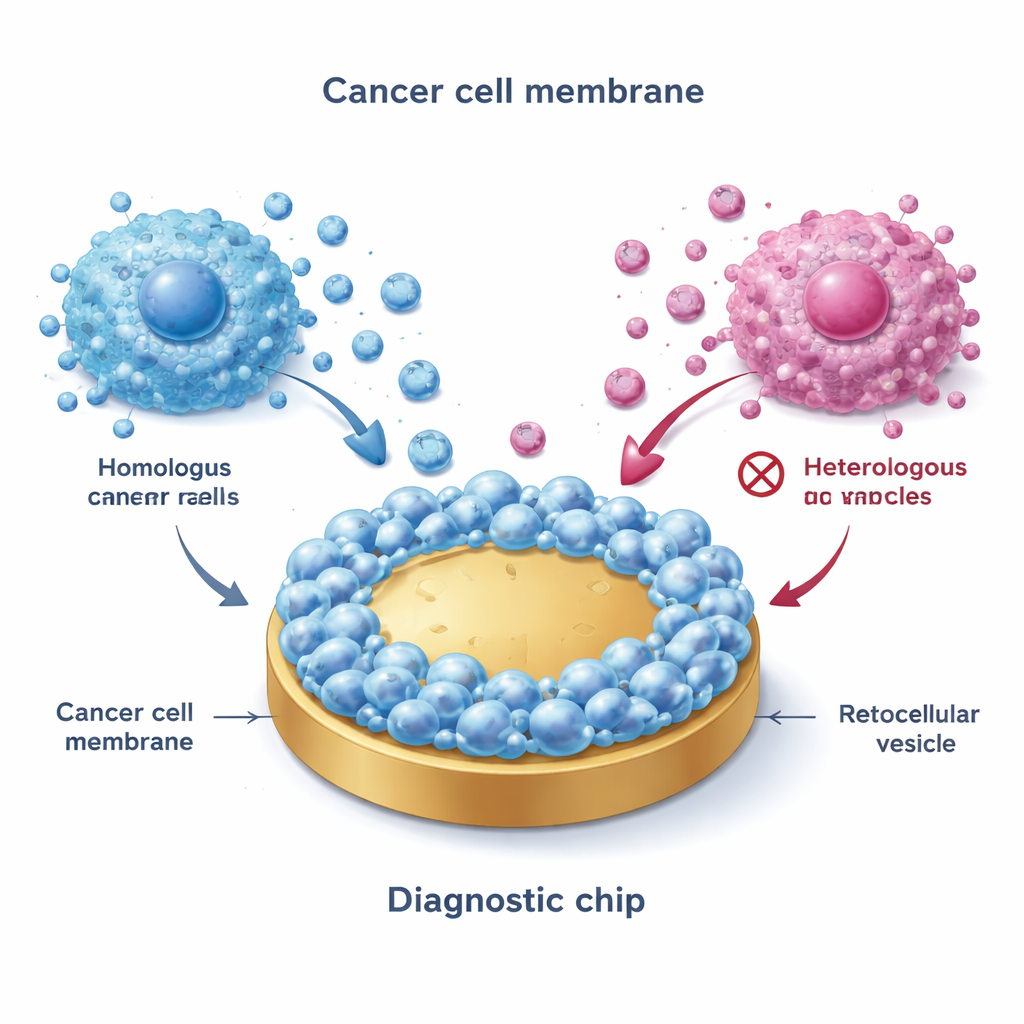
Команда начала с выделения мембран из культивируемых клеток рака молочной железы, представляющих основные подтипы: ER+ (например, MCF-7), HER2-положительные и тройного отрицательного типа. С помощью цикла замораживания–размораживания они разрушали клетки, выделяли наружные мембраны и затем сливали эти мембраны с плоскими золотыми поверхностями. Это создавало «биомиметический интерфейс», близко имитирующий внешний вид оригинальных раковых клеток. Примечательно, что когда везикулы прогоняли над такими покрытыми поверхностями, прочно прикреплялись только везикулы от соответствующих или близких по типу опухолей — явление, называемое гомотипичным связыванием. Передовые методы визуализации и электрические измерения подтвердили, что мембранные покрытия были более шероховатыми, более гидрофильными и значительно менее склонными к неспецифическому прилипанию по сравнению с голым золотом, что делает их пригодными для точных измерений в сложных жидкостях, таких как кровь.
Преобразование ловли везикул в электрический сигнал
Чтобы превратить связывание в читаемый сигнал, исследователи нацелились на обильный белок CD47 на поверхности EV. Они прикрепили антитела к CD47 к серебряным наночастицам с помощью короткого мостика из ДНК, создав крошечные электроактивные теги. После того как мембранное покрытие захватывало предпочитаемые везикулы, эти теги присоединялись к CD47 на связанных везикулах. При обработке кислотным раствором и последующих электрохимических измерениях серебро давало резкий, легко количественно оцениваемый ток. Сила этого сигнала линейно увеличивалась в широком диапазоне концентраций EV, вплоть до нескольких сотен везикул на миллилитр — значительно чувствительнее по сравнению с распространёнными методами, такими как наборы ELISA или отслеживание частиц. Каждый тип раковой мембраны давал сильный сигнал только с соответствующими везикулами, даже при наличии в образце везикул других подтипов, тромбоцитов или несвязанных клеток.
От лабораторного стола к образцам крови пациентов
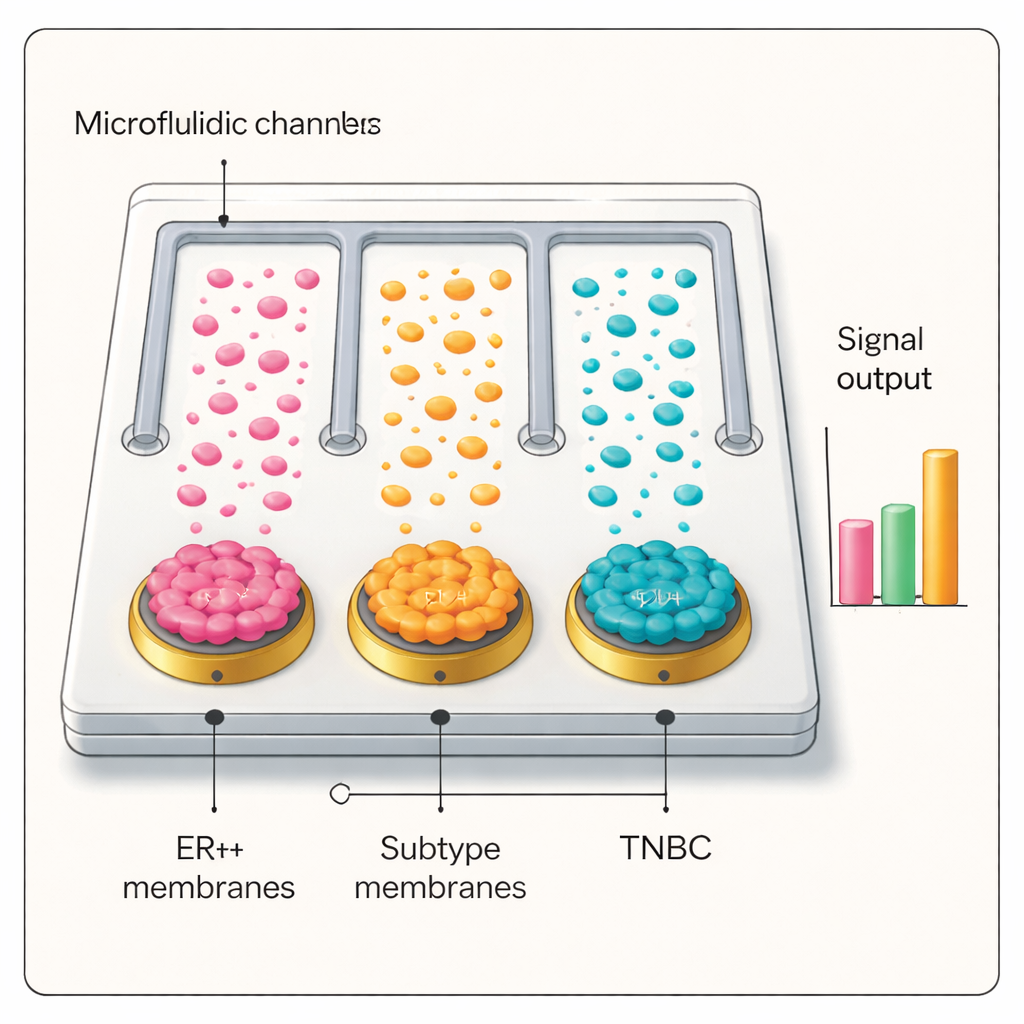
Вооружившись этим селективным и чувствительным интерфейсом, команда собрала микрофлюидную плату с параллельными каналами, каждый из которых был покрыт мембраной разных клеток рака молочной железы, а также оставлен непокрытый контрольный канал. Когда плазму пациентов прогоняли через чип и промеряли с помощью серебряно‑антительного маркера, только тот канал, чья мембрана соответствовала подтипу опухоли пациента, давал высокий электрический сигнал. В слепых испытаниях с десятками образцов — включая пациентов с ER+ и тройным отрицательным раком молочной железы, лиц с доброкачественными заболеваниями груди, пациентов с раком лёгкого и здоровых добровольцев — платформа точно различала рак и отсутствие рака и корректно идентифицировала подтипы рака молочной железы. Диагностическая эффективность во многих случаях сравнима или превосходит стандартную патологию и демонстрирует перспективы для стадирования заболевания и мониторинга его прогрессирования.
Что это может означать для будущей онкологической помощи
Проще говоря, исследователи превратили внешнюю оболочку рака в высокоселективную наживку для крошечных частиц, которые опухоли выбрасывают в кровь. Считывая электрический отпечаток того, какой канал «загорелся», врачи в будущем могли бы определить не только наличие рака, но и его тип, используя лишь образец крови. Хотя системе ещё требуются доработки — например, добавление большего числа маркеров и типов мембран, а также интеграция интеллектуального анализа данных — она указывает на будущее, в котором рутинные минимально инвазивные анализы крови помогут направлять персонализированное лечение рака и отслеживать, как опухоли меняются с течением времени.
Цитирование: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Ключевые слова: подтипы рака молочной железы, жидкостная биопсия, внеклеточные везикулы, микрофлюидная диагностика, сенсоры на клеточных мембранах