Clear Sky Science · ru
Эндотелиальный PDLIM5 стимулирует образование филоцитий кончиков клеток и антигенизацию опухолевой ангиогенезы путем регуляции ACTN1/ACTN4-зависимого упаковывания актина
Как рак присваивает себе кровеносные сосуды
Опухоль не может вырасти больше крошечного скопления клеток, если не заставит соседние кровеносные сосуды доставлять кислород и питательные вещества. В этом исследовании показано, как малоизвестный белок во внутренней выстилке сосудов помогает опухолям образовывать новые, аномальные ветви. Понимание этого процесса может открыть путь к более продуманным лечению, которые не только лишают опухоль питания, но и улучшают результаты иммунотерапии.
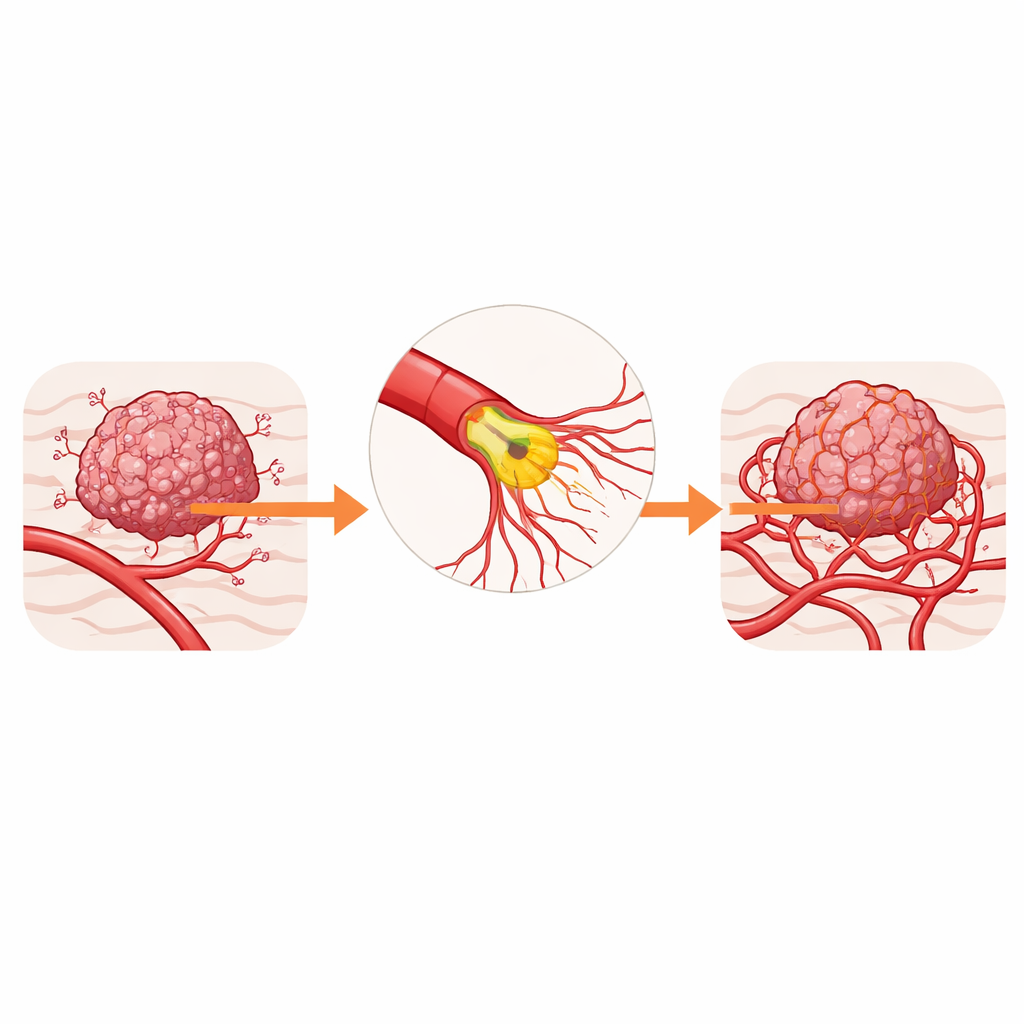
Скрытые архитекторы кровоснабжения опухоли
Кровеносные сосуды, питающие опухоли, построены из специализированных клеток — эндотелиальных клеток, выстилающих внутреннюю поверхность сосуда. На растущем переднем крае каждой новой ветви находится «кончиковая» клетка, которая выпускает длинные пальцеобразные отростки, называемые филоподиями. Эти отростки улавливают химические сигналы от опухоли и направляют новые побеги в зоны, лишенные кислорода. Во многих видах рака этот процесс идет в режиме усиленного роста, что приводит к образованию проницаемых, извитых сосудов, усугубляющих гипоксию и затрудняющих доставку лекарств и иммунных клеток к опухоли.
Белок, который ускоряет спрутинговый рост
Изучая отдельные клетки из человеческих опухолей легких, исследователи обнаружили, что ассоциированные с опухолью эндотелиальные клетки сильно активируют набор генов, контролирующих внутренний каркас клетки, особенно белок PDLIM5. PDLIM5 был более выражен в сосудах опухолей, чем в нормальных сосудах, и у пациентов с более высоким уровнем PDLIM5 в сосудах опухоли наблюдалась более короткая выживаемость. В моделях на мышах усиление экспрессии PDLIM5 в выстилке сосудов ускоряло рост опухолей и приводило к образованию более плотных сосудистых сетей, что указывает на то, что этот белок является мощным драйвером роста сосудов в опухоли.
Как PDLIM5 строит клеточные «щупальца»
Чтобы выяснить, как PDLIM5 влияет на поведение сосудов, команда использовала экспериментальные модели, где можно детально наблюдать за ростом побегов, например за растущими сосудами в сетчатке мыши и трехмерными культурами эндотелиальных клеток. При удалении PDLIM5 исключительно в эндотелиальных клетках побеги продвигались медленнее, число кончиковых клеток снижалось, и образовывалось значительно меньше филоподий. На микроскопическом уровне PDLIM5 связывался с двумя ключевыми белками, упаковывающими актин — ACTN1 и ACTN4, — и с длинными нитьями актина, которые формируют внутренний каркас клетки. Это «мостовое» действие помогало упаковывать нити актина в жесткие пучки, поддерживающие филоподии. Мутации в двух критических позициях PDLIM5 (S593 и F596) нарушали эту связь, ослабляли упаковывание актина и мешали восстановлению нормального спрутинга, доказывая, что это молекулярное взаимодействие необходимо для формирования «щупалец» кончиковой клетки.
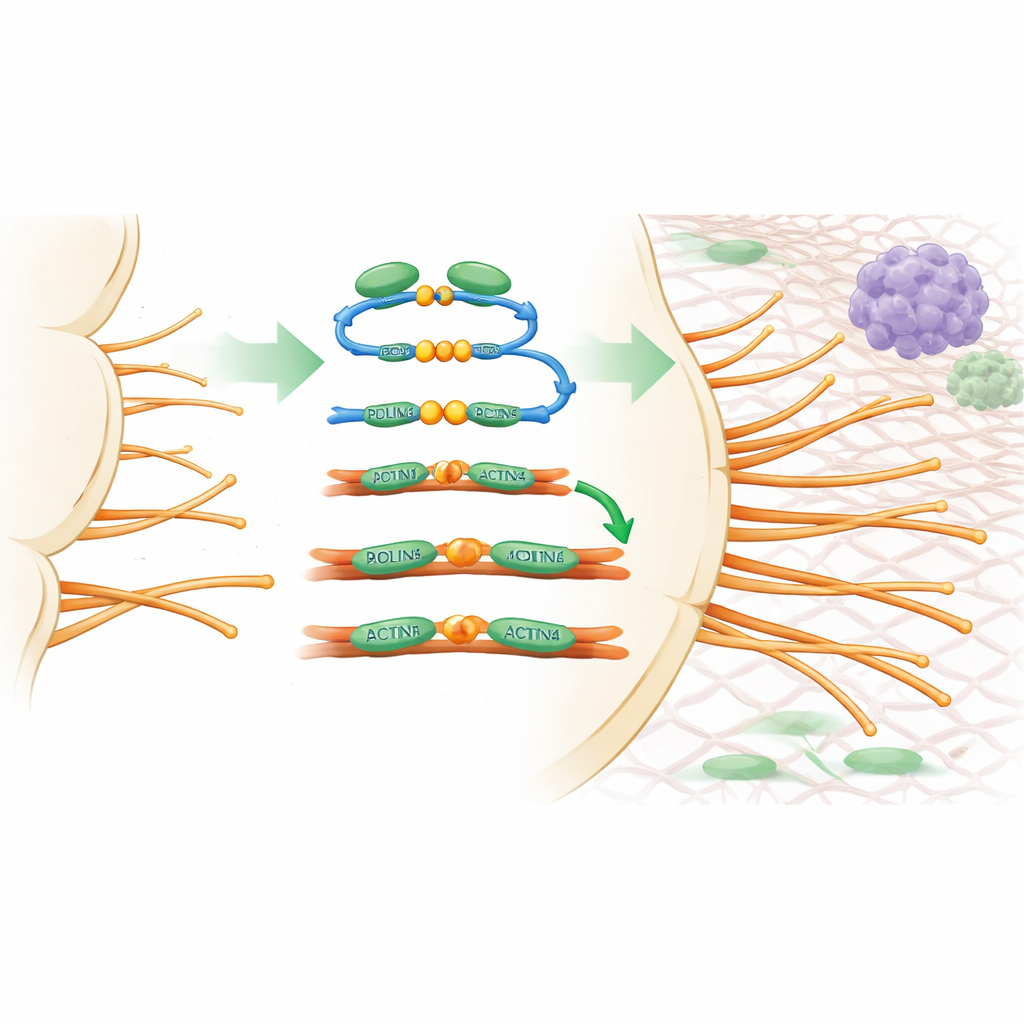
Перенастройка сосудов опухоли в пользу иммунной системы
Удивительно, но блокировка PDLIM5 в выстилке сосудов давала эффект, выходящий за рамки замедления роста опухоли. Сосуды опухоли становились более правильной формы, менее проницаемыми и лучше покрывались поддерживающими стабилизирующими клетками. В результате улучшалось снабжение кислородом, и зоны тяжелой гипоксии сокращались. Такие более «нормализованные» сосуды обеспечивали лучший приток иммунных Т-клеток в опухоль. Потеря PDLIM5 также меняла организацию адгезионных молекул на эндотелиальных клетках, облегчая прилипание Т-клеток к стенке сосуда и их прохождение в ткань опухоли. В мышиных моделях опухолей, обычно резистентных к ингибиторам контрольных точек, удаление PDLIM5 значительно усиливало эффект лечения антителом против PD-L1, уменьшая опухоли и увеличивая количество как хелперных, так и цитотоксичных Т-клеток в них.
Почему это важно для будущей терапии рака
В совокупности данные показывают, что PDLIM5 выступает центральным организатором актинового каркаса кончиковой клетки, обеспечивая формирование прочных филоподий и быстрый рост сосудистых побегов в сторону опухоли. Удаление или подавление PDLIM5 в эндотелиальных клетках замедляет расширение кровоснабжения опухоли, выпрямляет и стабилизирует оставшиеся сосуды, уменьшает кислородное голодание и способствует притоку иммунных клеток в опухоль. Для пациентов это означает, что препараты, направленные на разрушение взаимодействия PDLIM5 с ACTN1/ACTN4, могут одновременно лишать опухоль новых сосудов и преобразовывать хаотичную сосудистую сеть в такую, которая лучше поддерживает химио- и иммунотерапию.
Цитирование: Xu, Z., Shi, Y., Yang, Y. et al. Endothelial PDLIM5 promotes tip cell filopodia formation and tumor angiogenesis by regulating ACTN1/ACTN4-dependent actin bundling. Nat Commun 17, 2103 (2026). https://doi.org/10.1038/s41467-026-68765-x
Ключевые слова: опухолевый ангиогенез, эндотелиальные кончиковые клетки, PDLIM5, цитоскелет актина, иммунотерапия рака