Clear Sky Science · ru
Стабилизированный тандемный антигенный химера, вызывающая мощную активность по снижению передачи малярии
Почему важно прервать передачу через комаров
Действующие вакцины от малярии существенно снижают тяжесть заболевания и смертность у маленьких детей, но у них остаётся крупная брешь: люди, которые не чувствуют себя больными, всё ещё могут носить паразитов, заражающих комаров и поддерживающих передачу. В этом исследовании предложена конструкция вакцины следующего поколения, цель которой — не просто защитить одного человека, а разорвать цепочку передачи между людьми и комарами. Точное проектирование того, как ключевые белки паразита демонстрируются иммунной системе, направлено на выработку антител, делающих комаров плохими хозяевами для малярии и помогая сообществам приблизиться к ликвидации болезни.
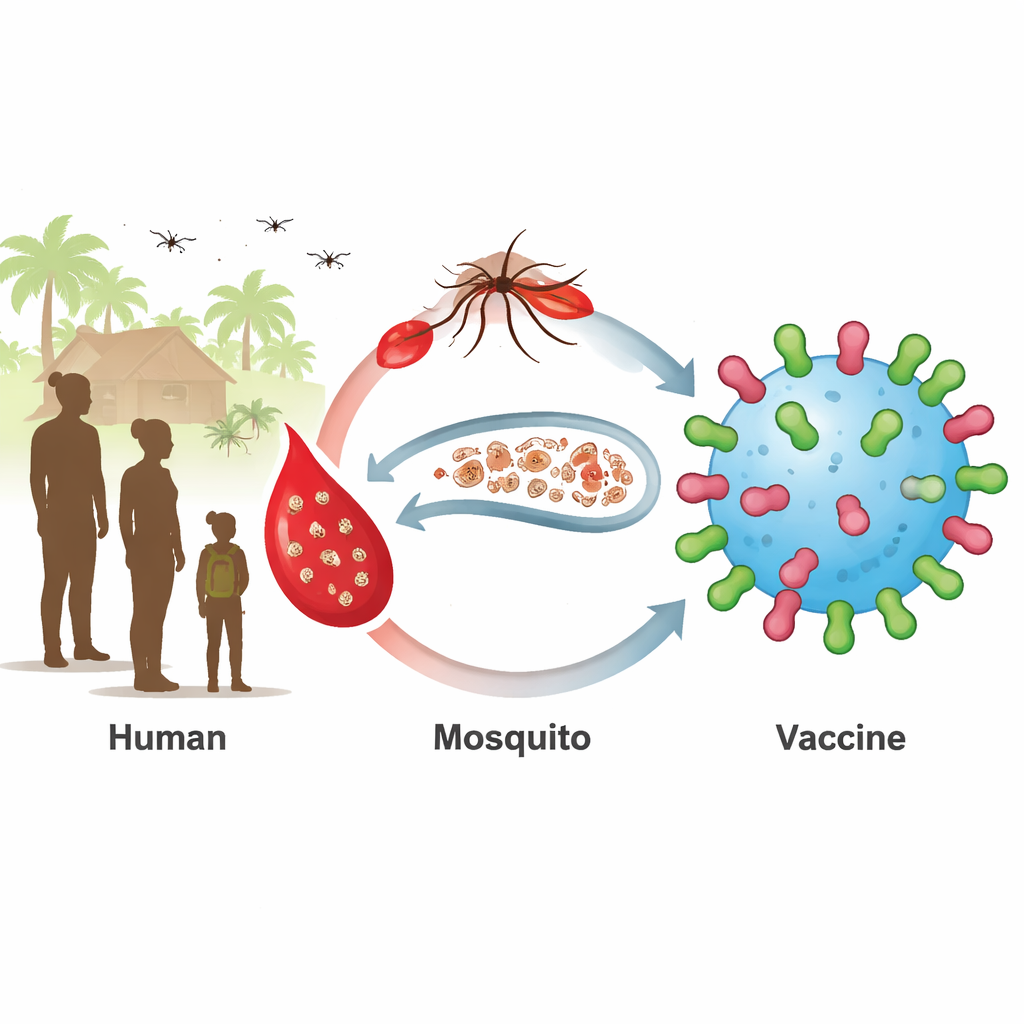
Скрытое резервуарное звено, которое поддерживает малярию
Современные вакцины против малярии нацелены на ранние стадии инфекции в печени и крови. Они наиболее эффективны у маленьких детей, но у старших детей и взрослых часто присутствуют зрелые половые стадии паразита — гаметоциты — без каких‑либо симптомов. Когда комары кусают таких людей, они подхватывают паразитов и распространяют их дальше. Два поверхностных белка паразита, известные как Pfs230 и Pfs48/45, находятся на этих половых стадиях и представляют собой привлекательные мишени для так называемых вакцин, блокирующих передачу. Вакцины на основе фрагментов этих белков вошли в клинические испытания, но им трудно вызывать сильные и долгоживущие антительные ответы у всех реципиентов.
Создание более умного приманочного антигена для иммунной системы
Чтобы улучшить предыдущие конструкции, авторы использовали подход структурной биологии, изучая с атомным разрешением, как мощные человеческие антитела связываются с Pfs230 и Pfs48/45. Они выделили небольшие участки, или эпитопы, которые особенно эффективны в блокировании развития паразита в комарах. Не менее важно, что они нанесли на карту «нефункциональные» эпитопы, которые привлекают антитела, связывающие, но не предотвращающие передачу — по сути зря расходующие иммунные ресурсы. С помощью компьютерного моделирования и инструментов белковой инженерии они слили наиболее сильный участок Pfs230 (его первый домен) с ключевым участком Pfs48/45 (его третий домен) в одном тщательно спроектированном белке, который назвали стабилизированной тандемной антигенной химерой, или STAC.
Скрывая бесполезные мишени, сохраняя полезные
Задача заключалась в том, чтобы предъявить эти два домена вместе так, чтобы это имитировало их положение на паразите, одновременно физически скрывая нефункциональные поверхности, которые в цельном белке обычно закрыты. Команда итеративно перерабатывала короткий линкер и интерфейс между доменами, тестируя каждую версию на стабильность, правильную укладку и способность по‑прежнему связываться с панелью хорошо охарактеризованных антител. Продвинутое программное обеспечение для дизайна предложило мутации, которые уплотняли интерфейс и улучшали экспрессию в культурах клеток. Структурные исследования с использованием рентгеновской кристаллографии, рассеяния малых углов и криоэлектронной микроскопии подтвердили, что в финальной конструкции STAC желаемые эпитопы демонстрируются с высокой достоверностью, тогда как известные нефункциональные участки стерически блокированы.
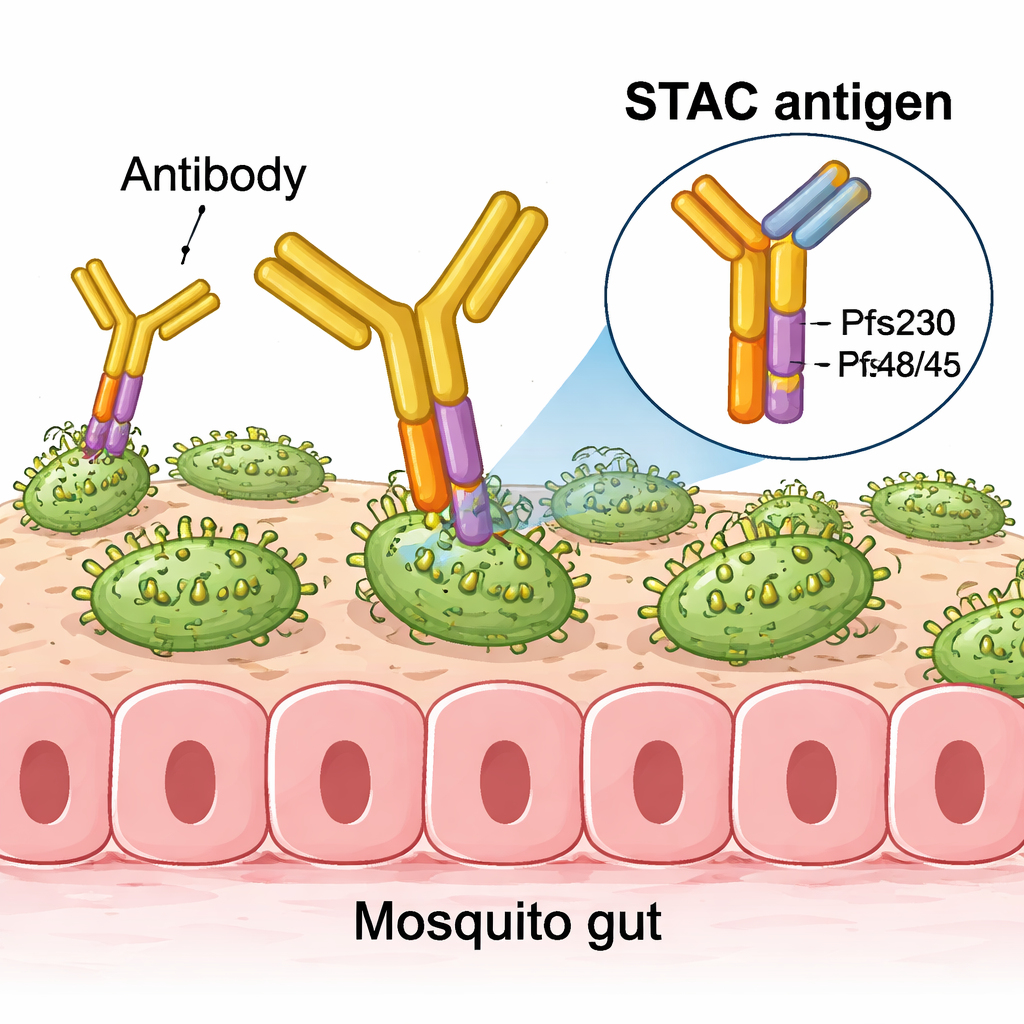
От одиночных молекул к мощным наночастицам
Испытания на мышах показали, что когда STAC прикрепляли к специализированным липосомам или к самосборочным белковым наночастицам, он вызывал сильные антительные ответы, способные значительно уменьшать развитие паразита в стандартных тестах кормления комаров. При равных или более низких дозах STAC часто соответствовал или превосходил вакцины на основе фрагментов Pfs230 и Pfs48/45, используемые по отдельности, смешанные вместе или совместно отображаемые на той же частице. В высокочувствительных тестах с многократным разведением сыворотки мышей антитела, вызванные наночастицами с декорированным STAC, сохраняли активность по снижению передачи лучше, чем антитела из других формуляций, что указывает на особенно мощный и сфокусированный ответ.
Что это может означать для контроля малярии
Для неспециалистов ключевая идея заключается в том, что STAC — это специально созданная приманка, которая показывает иммунной системе именно те части паразита малярии, которые наиболее важны для блокирования распространения, одновременно скрывая отвлекающие участки, которые не помогают. В моделях на животных такая конструкция даёт антитела, затрудняющие паразитам завершение жизненного цикла в комарах, даже при относительно низком уровне антител. Если похожие результаты подтвердятся у людей, STAC может стать мощным дополнением к существующим вакцинам от малярии: защищая вакцинированных от болезни и одновременно уменьшая инфекционный резервуар в сообществе. В более широком смысле работа демонстрирует, как детальные структурные знания и белковая инженерия могут быть использованы для создания многокомпонентных вакцин, которые являются мощными, стабильными и потенциально более дешевыми в производстве.
Цитирование: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Ключевые слова: вакцины от малярии, блокирование передачи, Pfs230, Pfs48/45, наночастичный иммуноген