Clear Sky Science · ru
Ключевая роль оси NONO‑HOXA1‑Wnt в дифференцировке кардиомиоцитов
Почему крошечные сердечные клетки важны для всех нас
Каждое сердцебиение зависит от миллиардов специализированных мышечных клеток, формирующихся в утробе. Если этот процесс идет неправильно, у новорожденных могут возникнуть серьёзные пороки сердца. В этом исследовании на людских стволовых клетках раскрыта важная управляющая система — созданная молекулами NONO и HOXA1 и хорошо известным сигналом Wnt — которая помогает ранним клеткам принять судьбу здоровой сердечной мышцы. Понимание этой скрытой схемы со временем может помочь в улучшении диагностики и лечения врожденных пороков сердца.
От клеток‑«чистой страницы» к ранним строителям сердца
Исследователи начали с индуцированных плюрипотентных стволовых клеток человека — универсальных клеток, которые можно направить в почти любой тип клеток. По стандартной методике они направляли эти клетки в кардиомиоциты, бьющиеся клетки сердца. При удалении гена NONO значительно меньше клеток успешно принимали сердечную идентичность. Ключевые ранние маркеры, которые обычно появляются, когда клетки покидают примитивное состояние и движутся к сердечной линии, были резко снижены. Одноклеточный РНК‑секвенсинг показал, что многие клетки с дефицитом NONO застревали на полпути, оставаясь в незрелом состоянии, подобном мезенденхиме, вместо того чтобы продолжать развитие в полноценную сердечную мышцу.
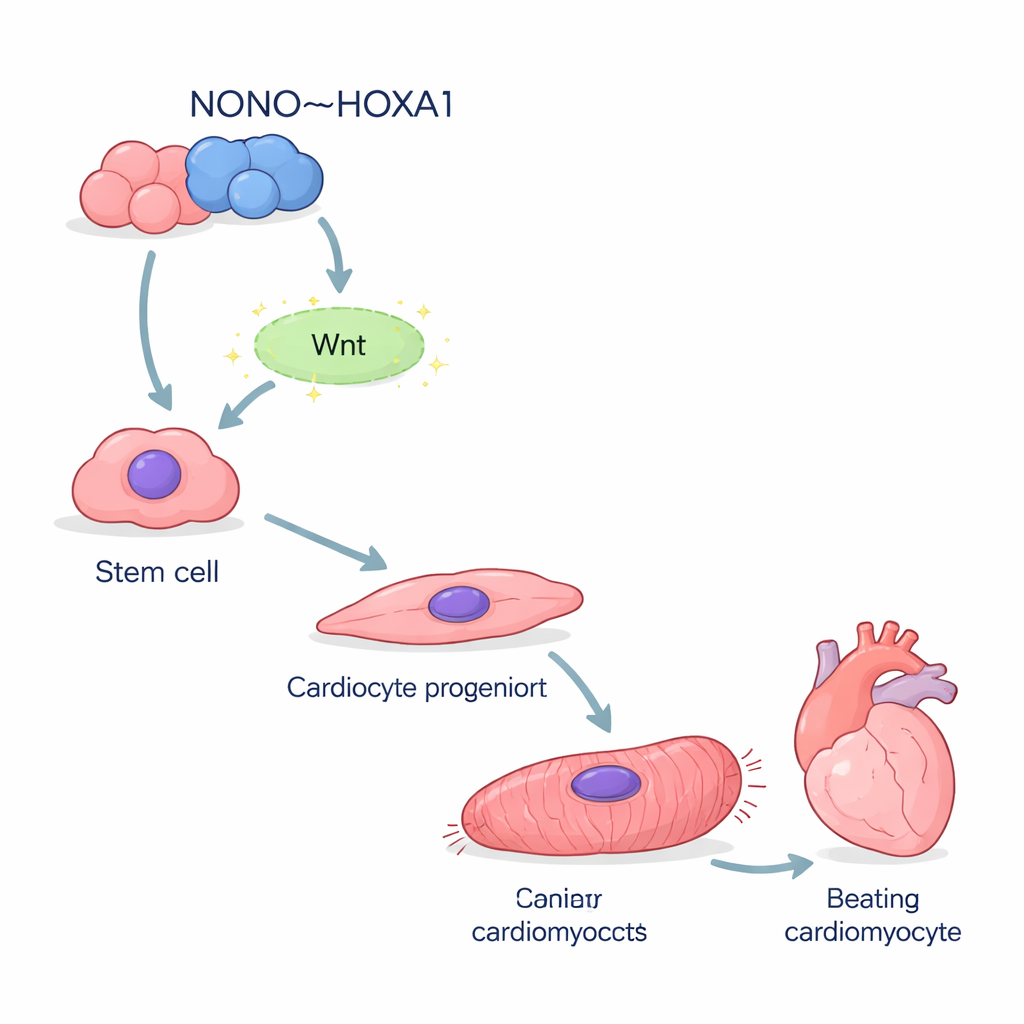
Когда каркас отсутствует, сердечные клетки дают сбой
Клетки, которые всё же становились кардиомиоцитами без NONO, были далеки от нормального состояния. Они экспрессировали значительно меньшие количества структурных белков, формирующих саркомер — микроскопический механизм, обеспечивающий сокращение. Под микроскопом у большинства мутантных клеток наблюдались дезорганизованные, фрагментированные сократительные волокна вместо аккуратных полос, характерных для нормальных клеток. Электронная микроскопия подтвердила, что обычные Z‑диски «ступеньки» сократительной лестницы отсутствовали или были деформированы. Функционально такие клетки сокращались медленнее и нерегулярно. Измерения кальциевых всплесков — электрических событий, запускающих каждое сердцебиение — показали нестабильные формы волн с задержанными пиками и медленным восстановлением, что отражает нарушения в экспрессии генов, отвечающих за кальциевый гомеостаз.
Восстановление развития и раскрытие партнерства NONO–HOXA1
Чтобы проверить, действительно ли проблемы вызваны потерей NONO, команда повторно ввела NONO контролируемо, индуцируемо лекарством, в течение первых двух дней дифференцировки. Этот короткий импульс NONO в значительной степени восстановил подъём ранних кардиальных генов, увеличил долю бьющихся сердечных клеток и восстановил организованные саркомеры и Z‑диски. Профилирование экспрессии генов подтвердило, что многие гены, связанные с мышечным сокращением и развитием сердца, вернулись к близким к норме уровням. Напротив, варианты NONO, обнаруженные у пациентов, не смогли обеспечить спасение, что поддерживает идею о том, что такие варианты вызывают болезнь, нарушая эту раннюю программу. Эксперименты по взаимодействию белков показали, что NONO физически связывается с фактором транскрипции HOXA1, и это взаимодействие стабилизирует HOXA1 и помогает ему образовывать димеры, необходимые для связывания с ДНК.
Включение сигнала Wnt для закрепления судьбы сердца
Картирование участков генома, куда эти белки привязываются, показало, что NONO и HOXA1 часто занимают одни и те же регуляторные области, в том числе контролирующие важные ранние сердечные и Wnt‑зависимые гены. При отсутствии NONO «захват» HOXA1 на многих таких сайтах ослабевал, особенно у генов, стимулирующих предсердечный мезодерм — самую раннюю ткань, формирующую сердце. Нисходящий путь Wnt/β‑катенин, который обычно помогает запускать формирование мезодермы и сердца, также был приглушён: в ядре накапливалось меньше β‑катенина, а тесты с репортером, реагирующим на Wnt, показывали снижение активности. Укрепление Wnt‑сигнала более высокой дозой препарата, активирующего Wnt, в самые ранние дни дифференцировки частично могло компенсировать отсутствие NONO, возвращая больше сердечных клеток и усиливая экспрессию кардиальных генов.
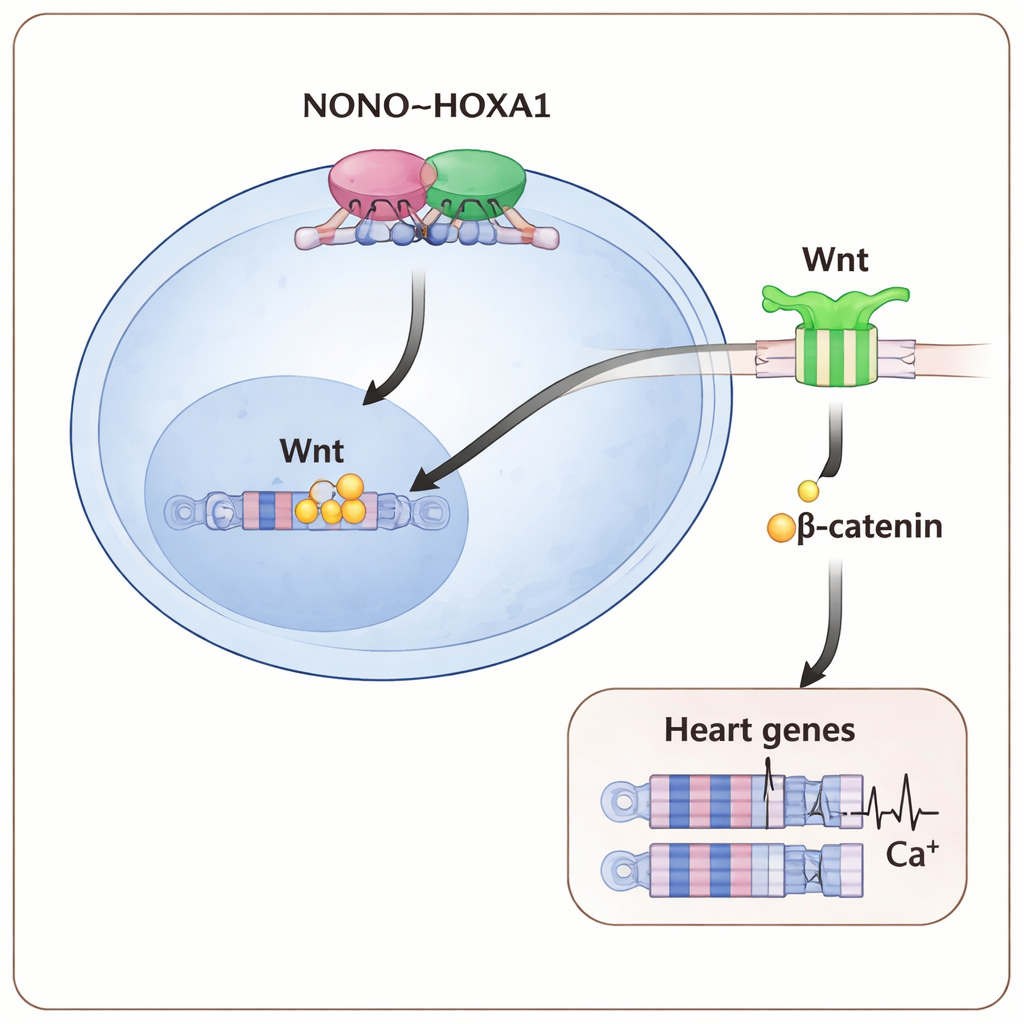
Что это означает для понимания врождённых пороков
Для неспециалистов главный вывод таков: небольшая молекулярная команда — NONO в тесном сотрудничестве с HOXA1, тонко регулирующая сигналы Wnt — действует как ранний «регулировщик трафика», который говорит молодым клеткам стать сердечной мышцей и оснащает их для нормального сокращения. Когда любая часть этой оси NONO–HOXA1–Wnt нарушена, клетки колеблются, ключевые сердечные гены остаются выключенными, и образующиеся кардиомиоциты становятся структурно и электрически уязвимыми. Эти открытия дают более ясное молекулярное объяснение тому, почему мутации в NONO связаны с врожденными пороками сердца, и указывают на пути для манипуляции этой системой в моделях на стволовых клетках или, возможно, в будущих терапиях, направленных на предотвращение или исправление сердечных дефектов.
Цитирование: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Ключевые слова: врожденные пороки сердца, дифференцировка кардиомиоцитов, Wnt‑сигнализация, модели сердца на стволовых клетках, регуляция генов