Clear Sky Science · ru
Электрографическая реактивность на сигналы соотносится с глубокой стимуляцией прилежащего ядра в случае опиоидного расстройства употребления
Почему эта история важна
Опиоидная зависимость остаётся смертоносной эпидемией: многие люди продолжают испытывать сильную тягу к наркотикам, несмотря на лекарственную терапию и психотерапию. Эта статья рассказывает историю одного молодого мужчины, чья команда лечащих врачей использовала имплантат в мозге не только для стимуляции, но и для прослушивания мозговой активности. Найдя специфический электрический сигнал, связанный с его опиоидной тягой, они смогли точно настроить глубокую стимуляцию мозга так, чтобы она работала лучше, с меньшей мощностью и помогла ему оставаться свободным от наркотиков.
Прослушивание тяги
Пациентом был 25‑летний мужчина с долгой историей тяжёлой опиоидной зависимости, начавшейся в ранней юности, в сочетании с депрессией, тревожностью и другими осложнениями. Стандартные методы лечения, включая очень высокие дозы метадона, не снижали его тягу до контролируемого уровня. Несколько лет ранее ему установили систему глубокой стимуляции мозга (ГСМ) в область глубоко внутри мозга, называемую прилежащим ядром — ключевой узел системы мотивации и вознаграждения. При включённой стимуляции его тяга уменьшалась, и в течение нескольких лет он сохранял воздержание от опиоидов. Однако хирургическое осложнение заставило врачей удалить батарею, и в течение нескольких недель тяга вернулась с новой силой, резко увеличив риск рецидива. Это создало редкую возможность: электрод в его мозге временно подключили к внешнему оборудованию для записи, позволив исследователям напрямую измерять мозговую активность во время переживания тяги.
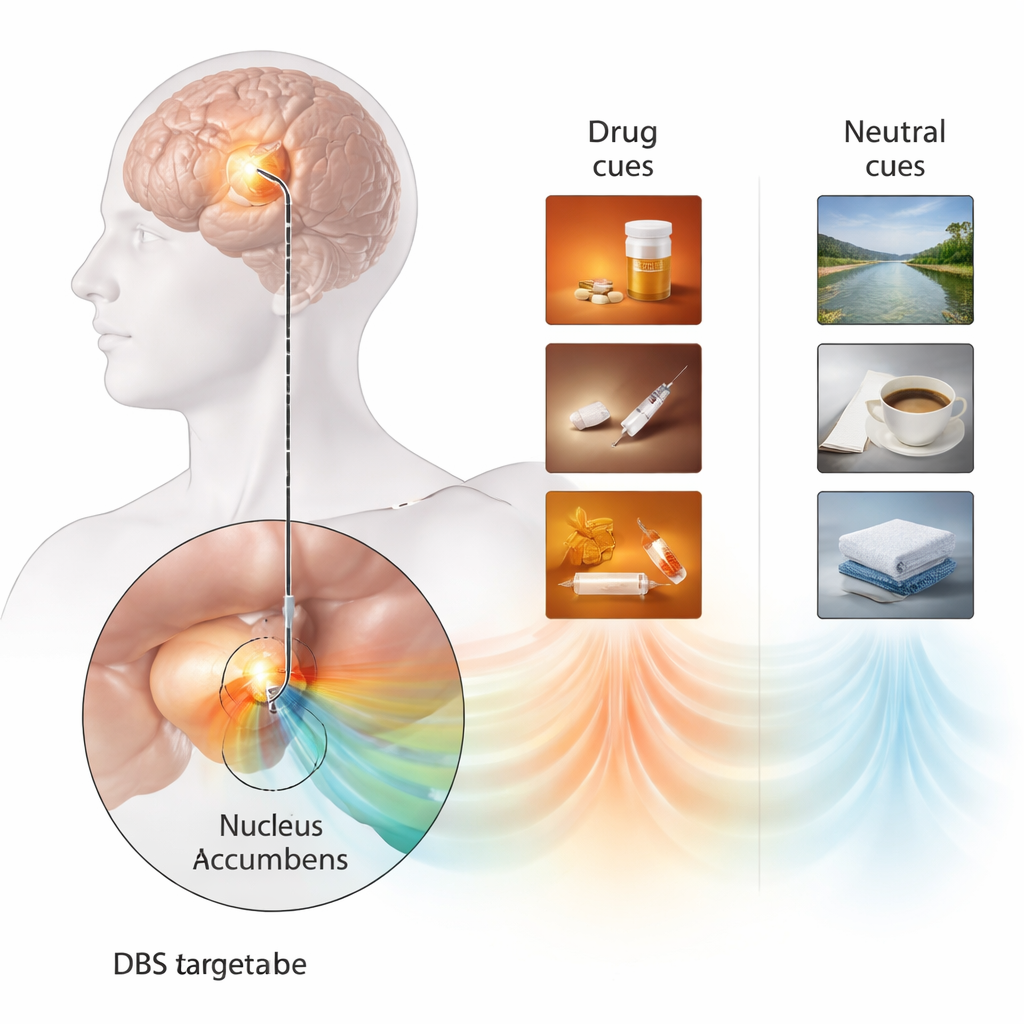
Индивидуальные триггеры выявляют мозговой сигнал
Чтобы поймать, как выглядит тяга в мозге, команда разработала высоко персонализированное задание на реактивность на сигналы. Вместо универсальных изображений наркотиков они создали короткие видеоролики, максимально соответствующие его прошлому употреблению — предпочитаемому опиоиду, инструментам для инъекций и ритуалам подготовки — и сопоставили их со спокойными сценами природы. После каждого шестисекундного клипа он оценивал, насколько сильным был его позыв к употреблению. Одновременно электрод ГСМ в прилежащем ядре действовал как крошечный микрофон, записывая локальные электрические ритмы мозга. При показе роликов с наркотиками в вентральной части прилежащего ядра, вероятно соответствующей подрегиону «шелл», появлялся характерный низкочастотный ритм (в диапазоне 1–6 Гц). Этот сигнал был значительно слабее при нейтральных видео и не регистрировался в других частях электрода. Важно, что высокая мощность этого ритма совпадала с более высокими самооценками тяги, что указывает на то, что это был прямой мозговой маркер реактивности на наркотические сигналы, а не общий индикатор возбуждения или внимания.
Преобразование стимуляции в целевой инструмент
Ключевой следующий вопрос заключался в том, сможет ли стимуляция именно в этой точке ослабить связанный с тягой мозговой ритм и соответствующее ему желание. Команда систематически тестировала разные пары контактов электрода, в реальном времени собирая данные о тяге, настроении и побочных эффектах при постепенном увеличении силы стимуляции. Вентральная пара контактов в «шелле» прилежащего ядра оказалась оптимальной: она обеспечивала сильное уменьшение тяги и улучшение настроения при относительно низком токе и с минимальными побочными эффектами. Более дорсальные пары контактов, в близком пучке волокон, называемом передним пучком внутренней капсулы, тоже помогали, но требовали значительно более сильной стимуляции и вызывали неприятные ощущения. На основе этих тестов исследователи затем повторили задание на реактивность на сигналы, подавая короткие серии стимуляции в шелл прилежащего ядра перед каждым видео. При этой «стимулируемой» условии ранее повышенный ритм 1–6 Гц во время показа наркотических роликов снизился до нейтральных уровней, а средние оценки тяги упали более чем наполовину.
Долговременное изменение при меньшей нагрузке
Основанные на согласующихся данных — анатомии, мозговых сигналах и поведении — клиницисты окончательно перепрограммировали его имплант для фокусной стимуляции в шелле прилежащего ядра при значительно более низком токе, чем раньше. В течение последующих шести месяцев он сообщал о стойком снижении как частоты, так и интенсивности опиоидной тяги, сохранял воздержание и соответствовал критериям ранней ремиссии, без существенных изменений в настроении, тревожности или уровне энергии. Моделирование мозговых сетей показало, что новые настройки активировали меньший, более сфокусированный объём ткани, одновременно задействуя ключевой путь между прилежащим ядром и областью под лобными долями, вовлечённой в эмоции и оценку. Поскольку стимуляция стала более эффективной, потребность в источнике питания заметно снизилась, что является важным преимуществом для молодого пациента, которому, вероятно, потребуется долгосрочная терапия.
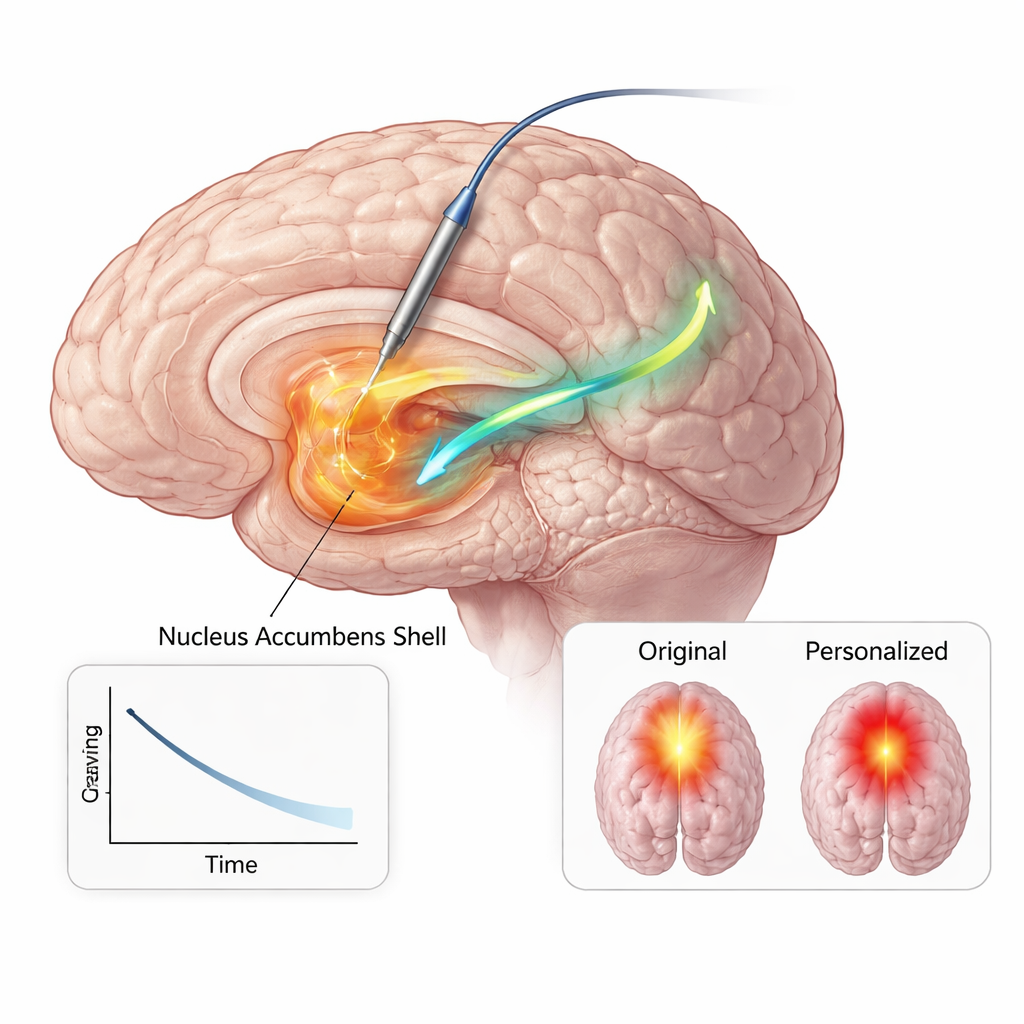
Что это может значить для будущей помощи
Этот случай «N‑of‑1» не доказывает, что тот же подход сработает для каждого человека с опиоидной зависимостью, но служит демонстрацией принципа. Он показывает, что по крайней мере у одного пациента специфический электрический ритм в «узле вознаграждения» мозга тесно отражал опиоидную тягу и мог быть подавлен прицельно направленной стимуляцией, что привело к стойкому облегчению симптомов при более низкой электрической дозе. Проще говоря, команда научилась «настраивать» стимулятор в соответствии с собственным сигналом тяги пациента. Если подобные мозговые маркеры удастся найти и отслеживать у большего числа людей, и если устройства, которые одновременно регистрируют и стимулируют, станут более доступными, будущие методы лечения смогут персонализировать стимуляцию мозга при зависимости — реагируя, когда цепи тяги активируются, и потенциально помогая людям опережать рецидив.
Цитирование: Qiu, L., Nho, YH., Seilheimer, R.L. et al. Electrographic cue-reactivity co-localizes with accumbens deep brain stimulation in a case of opioid use disorder. Nat Commun 17, 1708 (2026). https://doi.org/10.1038/s41467-026-68758-w
Ключевые слова: опиоидная зависимость, глубокая стимуляция мозга, приближенное ядро, биомаркеры мозга, тяга к наркотикам