Clear Sky Science · ru
Структурная основа обращения вилки и регуляции RAD51 комплексом убиквитин-лигазы SCF на базе хеликаза FBH1
Как клетки спасают застрявшую машину копирования ДНК
Каждый раз при делении клетки ей нужно быстро и точно скопировать миллиарды букв ДНК. Но этот копировальный аппарат часто сталкивается с проблемами — повреждения ДНК, трудно копируемые участки или лекарственные воздействия могут замедлить или остановить процесс. В таких случаях клетки полагаются на аварийные ремонтные бригады, которые стабилизируют и перезапускают репликационные вилки. Эта статья впервые в таком детальном структурном виде показывает, как один из руководителей такой бригады — белковый комплекс, построенный вокруг хеликазы FBH1 — перекраивает застрявшую ДНК и жестко контролирует другой ключевой белок ремонта, RAD51. Понимание этой хореографии помогает объяснить, как клетки избегают опасных разрывов генома и почему нарушения этих компонентов связаны с раком.
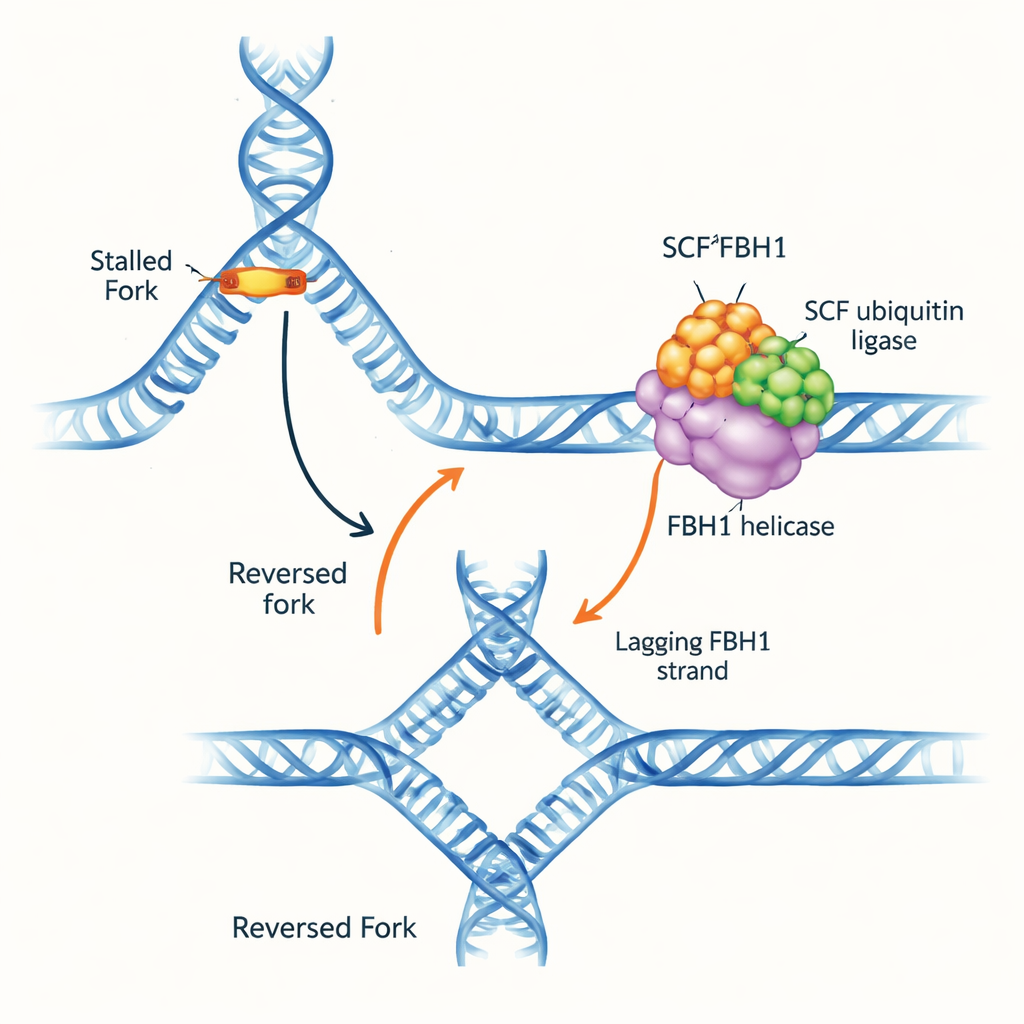
Пробка на ДНК-шоссе
Репликационные вилки ДНК — это Y-образные структуры, где двойная спираль расплетается и копируется. Когда вилка натыкается на препятствия, она может развернуться: родительские нити снова спариваются, а недавно синтезированные нити соединяются друг с другом, образуя четырёхветвевую ДНК-структуру. Такое «обращение вилки» может выиграть время для ремонта и безопасного возобновления репликации, но при неправильном управлении оно создаёт хрупкую ДНК, склонную к разрывам. Несколько молекулярных моторов умеют продвигать вилки назад, захватывая двухцепочечную ДНК перед вилкой. FBH1 выделялся тем, что ведёт себя иначе и часто изменяется в опухолях, что указывает на то, что он действует по уникальному и клинически важному пути.
Специалист по вилкам с выраженной «любимой» стороной
Авторы очистили человеческий комплекс SCFFBH1, который объединяет хеликазу FBH1 с модулем для прицепления убиквитина (SCF). Сначала они выяснили, какие формы ДНК предпочитает FBH1. С помощью анализов связывания и раскручивания они показали, что SCFFBH1 сильно предпочитает настоящие вилкообразные структуры, особенно там, где на шаблонной «запаздывающей» цепи — той, что копируется фрагментами — имеется короткий участок одноцепочечной ДНК. На таких структурах FBH1 раскручивает ДНК в сотни раз быстрее, чем на простом свободном конце, что указывает на то, что правильное захватывание на ответвлении вилки значительно усиливает его двигательную активность. Одиночномолекулярные магнитные пинцеты подтвердили, что комплекс может раскручивать, а затем двигаться по одноцепочечной ДНК на тысячи нуклеотидов, не слетая, действуя как мощный процессивный мотор.
Обращение вилки путём «тянущего» движения сзади
Чтобы понять, как этот мотор фактически разворачивает вилки, группа протестировала искусственные субстраты вилок с разрывами или без них. В отличие от других ремоделирующих вилку белков, SCFFBH1 не мог действовать на полностью спаренную вилку; ему был необходим зазор на запаздывающем шаблоне, и он двигался в направлении 3′→5′ по этой одноцепочечной нити. Такое «тянущее сзади» движение заставляет родительские нити заново спариваться, в то время как фермент остаётся зажатым в месте ответвления вилки. Крио-электронно-микроскопическая структура SCFFBH1, связанного с застрявшей вилкой, показывает, как это происходит: специальная положительно заряженная область, «мотив связывания ответвления», в одном поддомене FBH1 размещается прямо в точке ветвления, где сходятся три ДНК-ветви. Когда исследователи мутировали две ключевые аминокислоты в этом мотиве, эффективность обращения вилки в пробирках упала примерно в 25 раз, хотя базовый раскручивающий двигатель по-прежнему работал относительно хорошо. В клетках та же мутация мешала нормальному замедлению репликационных вилок в ответ на препарат, вызывающий стресс — признак неудавшегося обращения вилки.
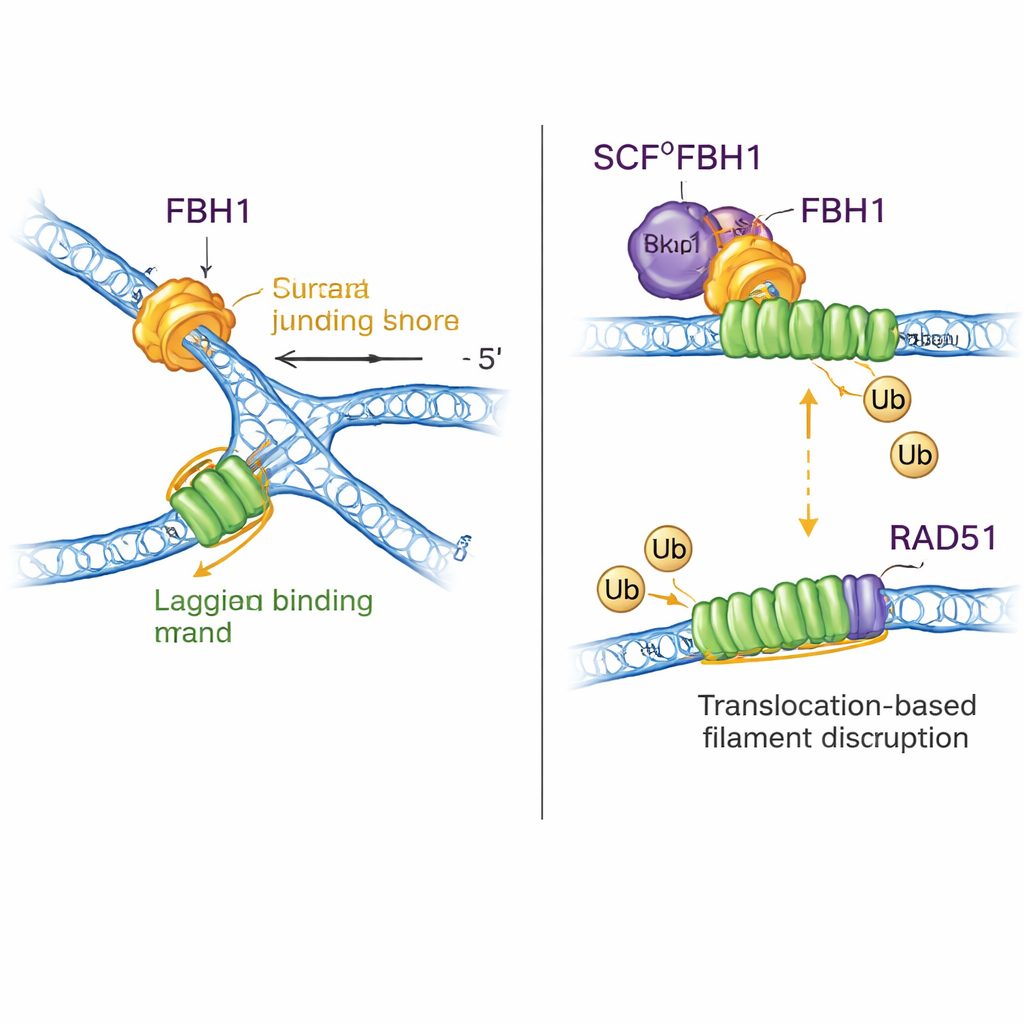
Двойная роль: перекройка ДНК и удаление RAD51
FBH1 — это не только мотор; через комплекс SCF он также способствует прицеплению коротких убиквитиновых меток к белкам. Новые структуры собирают почти весь комплекс SCFFBH1–ДНК и показывают, что «голова» лигазы, ответственная за перенос убиквитина, находится менее чем в 45 ангстремах от запаздывающей цепи ДНК, выходящей из FBH1. На основе встраивания известных структур других убиквитин-лигаз авторы предлагают, что такая геометрия выводит RAD51 — фермент, формирующий нити на ДНК для содействия рекомбинации — как раз на линию огня на запаздывающей цепи застрявшей вилки. Предыдущие работы показали, что FBH1 может механически снимать RAD51 с ДНК и также помечать его убиквитином, чтобы он не мог быстро снова связаться. Новая модель объединяет эти идеи: по мере того как FBH1 тянет по запаздывающей цепи, перекраивая вилку, соседний модуль SCF может помечать субъединицы RAD51, помогая разрушать или предотвращать чрезмерные нити RAD51, которые в противном случае мешали бы правильной обработке вилки.
Что это значит для стабильности генома и рака
В совокупности исследование показывает, что SCFFBH1 обращает застрявшие репликационные вилки ДНК механизмом, отличным от других известных ремоделирователей вилок: он крепко захватывает точку ветвления, одновременно перемещаясь по запаздывающему шаблону сзади, способствуя безопасному перематыванию родительской ДНК без образования долговременной мобильной четырёхветвевой структуры. Одновременно встроенная убиквитин-лигаза стратегически расположена для удаления RAD51 с той же нити, предотвращая неконтролируемую рекомбинацию при стрессe репликации. Поскольку FBH1 часто теряется или мутирует в опухолях, эти структурные и механистические наблюдения помогают объяснить, почему такие раки накапливают повреждения ДНК и почему они могут по-разному реагировать на препараты, вызывающие стресс репликации или нацеленные на связанные пути.
Цитирование: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Ключевые слова: стресс репликации ДНК, обращение вилки, хеликаза FBH1, регуляция RAD51, стабильность генома