Clear Sky Science · ru
Протеогеномный атлас 1032 метастазов в мозге выявляет молекулярные подтипы, иммунные ландшафты и терапевтические уязвимости
Почему рак распространяется в мозг
По мере улучшения онкологической помощи всё больше людей доживают до стадии, когда их опухоли распространяются в новые органы, в том числе в мозг. Метастазы в мозге теперь — распространённое и часто разрушительное осложнение, однако врачи по‑прежнему в основном ориентируются на первичную локализацию опухоли — лёгкие, грудь, кожа, кишечник — а не на то, как рак адаптировался к жизни в мозге. В этом исследовании создан подробный «атлас» более тысячи метастазов в мозге, чтобы понять их скрытую биологию, взаимодействия с клетками и иммунной системой мозга и возможные новые терапевтические точки воздействия.
Построение масштабной карты опухолей мозга
Исследователи собрали данные о 1 032 метастазах в мозге, произошедших из разных первичных опухолей, а также о нескольких десятках соответствующих первичных опухолей и некоторых агрессивных первичных опухолях головного мозга для сравнения. Они объединили несколько передовых подходов: секвенирование ДНК и РНК, масштабные измерения белков и метаболитов, картирование опухолевых и иммунных клеток на уровне отдельных клеток и в пространственной организации, а также миниатюрные органоиды, полученные от пациентов и выращенные в лаборатории. Интегрируя все эти слои данных, авторы стремились не просто перечислить гены, а увидеть, как целые биологические системы функционируют в метастазах в мозге.
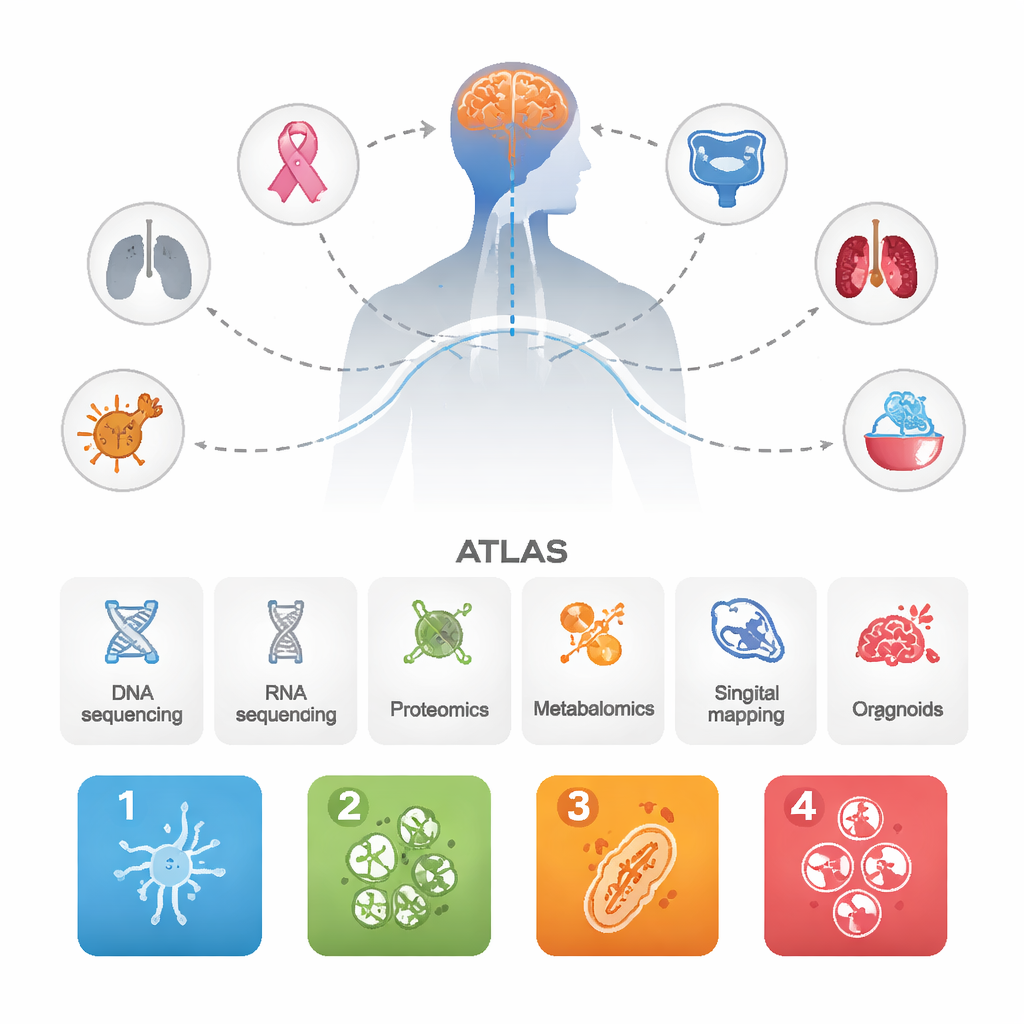
Четыре повторяющиеся «личности» метастазов в мозге
Несмотря на происхождение из разных органов, метастазы в мозге устойчиво делились на четыре основные молекулярные подтипа. Первый, названный BrMS1, напоминает «нейронный» — опухолевые клетки и окружающие ткани экспрессируют многие программы мозга и нервных клеток и демонстрируют относительно активный иммунный надзор. BrMS2 — «проницаемый иммунитетом», наполнен иммунными клетками, особенно Т‑клетками, и характеризуется программой эпителиально‑мезенхимального перехода, которая ослабляет клеточные прикрепления и перестраивает локальную среду. BrMS3 — «метаболический», доминируют высокоактивные раковые клетки, перенастраивающие использование энергии — с усилением путей, таких как метаболизм жирных кислот и окислительное фосфорилирование. BrMS4 — «пролиферативный», отмечен быстрым делением клеток, стволоподобными признаками и высокой геномной нестабильностью, но примечательно малым количеством иммунных клеток.
Что раскрывает окружение опухоли
При изучении на уровне отдельных клеток и с пространственным разрешением команда показала, что каждый подтип обитает в своём уникальном «районе» мозга. Очаги BrMS1 богаты поддерживающими клетками мозга, такими как астроциты и нейроны, что указывает на то, что опухоль тесно имитирует и эксплуатирует нормальную мозговую ткань. Опухоли BrMS2, напротив, усеяны плотными скоплениями Т‑клеток, включая множество «истощённых» Т‑клеток, экспрессирующих контрольные молекулы вроде PD‑1, и характеризуются активированными сосудами и воспалительными сигналами. Очаги BrMS3 располагаются в метаболически активных зонах, а очаги BrMS4 формируют островки быстро делящихся клеток, окружённые относительно бедной иммунной средой. В целом исследование выявило, что в метастазах в мозге — но не в первичных опухолях — сильная активация эпителиально‑мезенхимального перехода часто сопровождается более высокой инфильтрацией Т‑клеток, что наводит на мысль, что эта программа может способствовать проникновению иммунных клеток.
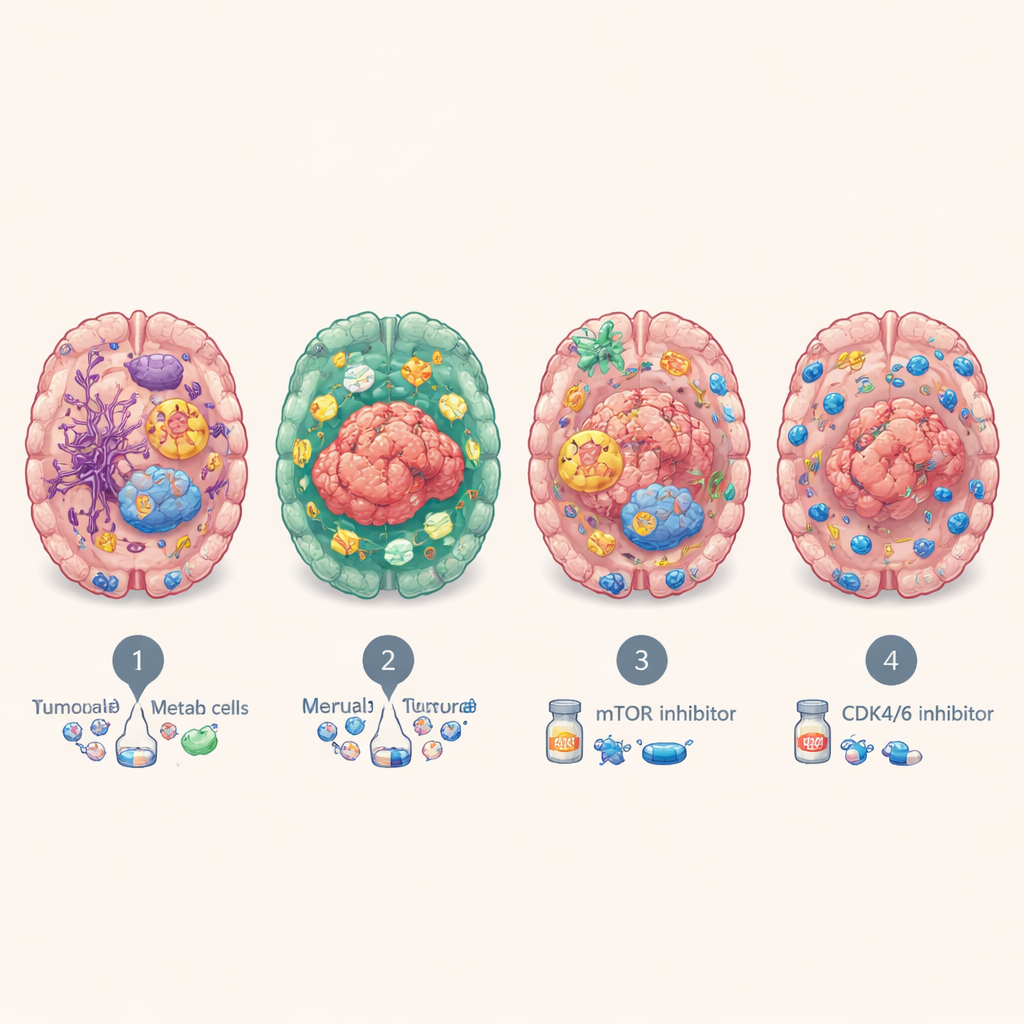
Подсказки для лечения и прогноза пациентов
Эти молекулярные «личности» имеют клиническое значение. Пациенты с иммунно‑проницаемым подтипом BrMS2 в целом жили дольше, чем пациенты с пролиферативным подтипом BrMS4, который последовательно демонстрировал худшие исходы. Тестирование препаратов на органоидах, полученных от пациентов, показало, что метаболические опухоли BrMS3 особенно чувствительны к блокированию сигнального пути mTOR, который регулирует рост и метаболизм клеток, а быстро делящиеся BrMS4 более уязвимы к ингибиторам CDK4/6, замедляющим клеточный цикл. Отдельные анализы предположили, что опухоли BrMS1 могут лучше реагировать на лучевую терапию, в то время как воспалённая, богатая контрольными молекулами среда BrMS2 может сделать их более пригодными для иммунотерапий, восстанавливающих активность истощённых Т‑клеток — хотя это нужно подтвердить в клинических исследованиях непосредственно у пациентов с метастазами в мозге.
Что это значит для людей с метастазами в мозге
Этот атлас показывает, что после попадания в мозг раковые клетки, как правило, сходятся в несколько общих биологических состояний, которые не зависят от их первичного происхождения. Понимание того, относится ли метастаз в мозге пациента к нейроноподобному, иммунно‑богатому, метаболическому или сильно пролиферативному типу, в будущем может помочь подобрать более точное лечение — например выбрать между радиотерапией, иммунотерапией или препаратами, направленными на метаболизм или деление клеток. Хотя это исследование ещё не меняет стандарт лечения, оно даёт подробную дорожную карту для дальнейших исследований и клинических испытаний, задача которых — превратить эти молекулярные уязвимости в более точные и эффективные терапии для пациентов с метастазами в мозге.
Цитирование: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Ключевые слова: метастаз в мозге, подтипы опухолей, микроокружение опухоли, онкоиммуннотерапия, метаболизм рака