Clear Sky Science · ru
Кинуренин опосредует химиотерапевтическую токсичность кишечника через модуляцию микробиоты
Почему это важно для людей, проходящих химиотерапию
Химиотерапия спасает жизни, но часто сопровождается тяжёлыми побочными эффектами со стороны кишечника — болью, диареей, потерей веса, которые могут вынудить врачей снизить дозы или преждевременно прекратить лечение. В этом исследовании раскрывается скрытая цепочка взаимодействий между молекулой в крови, иммунными клетками и кишечной микробиотой, что помогает объяснить, почему распространённый противораковый препарат оксалиплатин так сильно повреждает кишечник, и указывает на новые способы защитить пациентов, не ослабляя противоопухолевую терапию.
Химическая связь между лечением и повреждением кишечника
Исследователи начали с пациентов с колоректальным раком, получавших химиотерапию на основе оксалиплатина. Они сравнили образцы крови у людей, у которых развились тяжёлые кишечные побочные эффекты, и у тех, кто переносил лечение лучше. Прицельный химический профиль показал, что несколько продуктов распада аминокислоты триптофана были повышены в группе с высокой токсичностью, и одна молекула — L‑кинуренин — выделялась как самая значительно повышенная. У пациентов с более высоким уровнем L‑кинуренина в крови также наблюдались более выраженные признаки воспаления и пониженное количество лейкоцитов, что наводит на мысль о прямой связи этой молекулы с вредом, связанным с лечением.
Доказательство причинно-следственной связи на мышах
Чтобы выйти за рамки корреляции, команда обратилась к модельным исследованиям на мышах. Когда здоровым мышам вводили большие дозы оксалиплатина, у них возникали типичные признаки повреждения кишечника: потеря веса, укорочение толстой кишки, отёк стенки кишечника, уменьшение числа делящихся клеток и увеличение числа погибающих клеток в эпителии. У этих животных также отмечалось резкое повышение уровня L‑кинуренина в крови, что соответствовало данным у людей. Когда мышам, получавшим оксалиплатин, дополнительно давали L‑кинуренин, повреждение кишечника усиливалось — при этом противоопухолевая активность препарата против опухолей сохранялась. Наоборот, при удалении или блокировании фермента IDO1, используемого в организме для превращения триптофана в L‑кинуренин, мыши оказались гораздо более устойчивы к кишечной токсичности, при этом не утрачивали пользы от химиотерапии.
Иммунные клетки и микробы кишечника в перекрёстном огне
Углубляясь, учёные выяснили, какие клетки отвечают за избыточное производство L‑кинуренина во время лечения. Они обнаружили, что оксалиплатин стимулирует определённые иммунные клетки (CD8 T‑лимфоциты) выделять сигнальный белок интерферон‑гамма, который затем включает IDO1 в соседних миелоидных клетках — типе лейкоцитов. У мышей, у которых IDO1 отсутствовал только в миелоидных клетках, уровень L‑кинуренина был значительно ниже, и они были защищены от повреждения кишечника, тогда как удаление IDO1 только в клетках эпителия давало мало эффекта. Одновременно состав микробиоты кишечника изменился. У обычных мышей оксалиплатин и высокий уровень L‑кинуренина были связаны с исчезновением полезной бактерии Lactobacillus johnsonii. Напротив, у мышей с пониженным уровнем L‑кинуренина L. johnsonii сохранялась в больших количествах. Когда кишечные бактерии уничтожали антибиотиками, защитный эффект низкого L‑кинуренина исчезал, а при пересадке микробиоты от животных с низким уровнем L‑кинуренина к обычным реципиентам последние становились более устойчивыми к повреждению кишечника оксалиплатином.
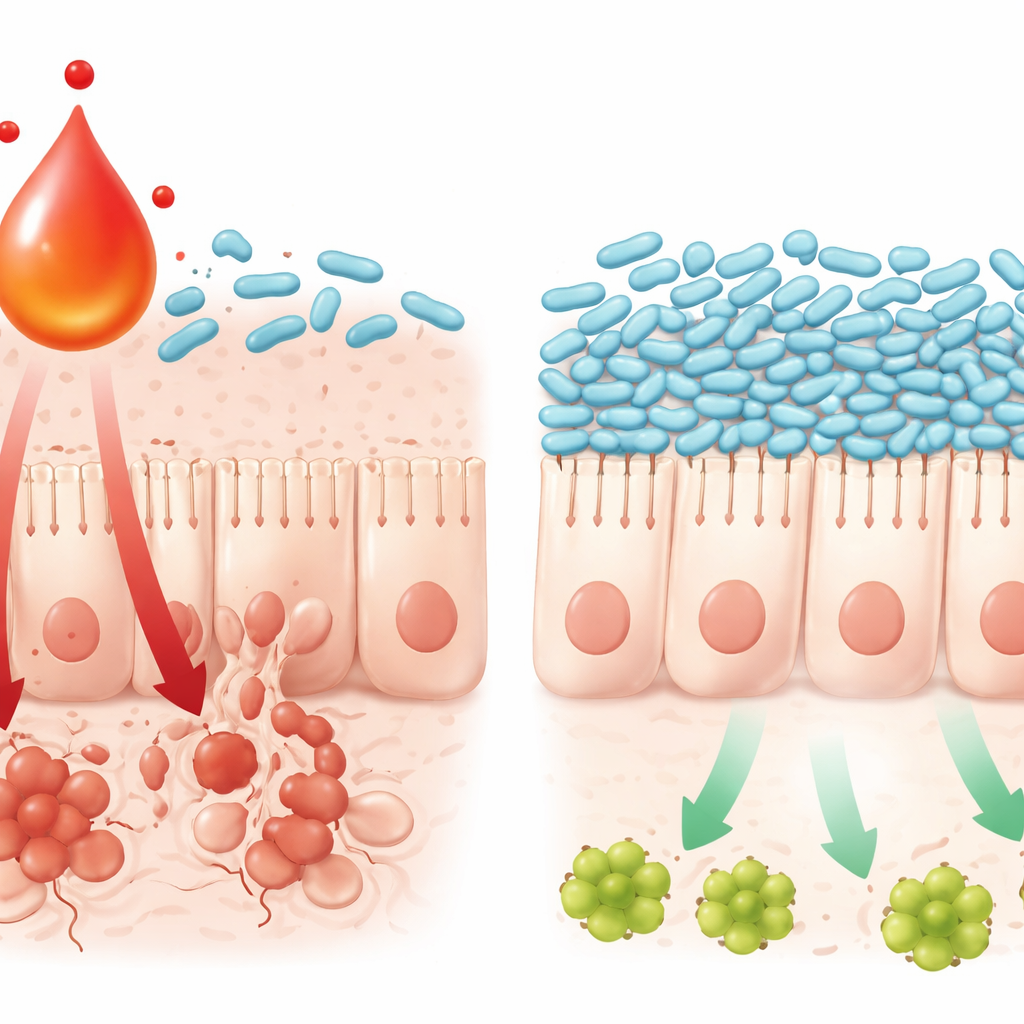
Как один метаболит вызывает гибель клеток в кишечнике
Исследование также проследило, как это взаимодействие «химия–микробиота» повреждает эпителий кишечника. Высокие уровни L‑кинуренина ассоциировались с повышенной активностью известного воспалительного пути в кишечной ткани — TNFα/JNK, который направляет клетки к программируемой гибели. В культуре клеток сочетание оксалиплатина и L‑кинуренина делало кишечные клетки более склонными к активации этого пути и гибели, тогда как добавление бактерий L. johnsonii ослабляло сигнал и сохраняло выживаемость клеток. Сам L‑кинуренин замедлял рост и нарушал механизмы выживания L. johnsonii в лабораторных условиях, что помогает объяснить исчезновение бактерии при накоплении метаболита. В совокупности эти результаты описывают самоподдерживающуюся петлю: химиотерапия запускает иммунную сигнализацию, иммунные клетки повышают уровень L‑кинуренина, это нарушает полезные бактерии вроде L. johnsonii, а изменённое микробное сообщество усиливает воспалительные сигналы, приводящие к гибели клеток кишечника.
Новые подходы для защиты пациентов во время лечения
Обнадеживающе, работа также указывает на практические стратегии. Лечение мышей препаратом эпакадостатом, ингибирующим IDO1, снижало уровни L‑кинуренина и заметно уменьшало повреждение кишечника, вызванное оксалиплатином, не ослабляя при этом контроля над опухолью. В дополнительном подходе команда модифицировала безопасный штамм E. coli так, чтобы он сверхэкспрессировал фермент, разрушающий L‑кинуренин в кишечнике. Мыши, получавшие эти модифицированные бактерии, также были защищены от кишечной токсичности, опять-таки без ущерба для противоопухолевого действия химиотерапии. Добавление самой L. johnsonii тоже облегчало симптомы и сохраняло структуру кишечника.
Что это значит для людей с раком
В сумме исследование показывает, что один метаболит, индуцируемый лечением — L‑кинуренин — выступает ключевым посредником между химиотерапией, иммунной системой, кишечными микробами и повреждением кишечника. Демонстрация того, что блокирование его синтеза, усиление его распада или восстановление защитных бактерий могут смягчить вред химиотерапии для кишечника, открывает путь к адъювантным стратегиям, которые помогут пациентам оставаться сильнее и чувствовать себя комфортнее во время борьбы с раком.
Цитирование: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Ключевые слова: побочные эффекты химиотерапии, микробиом кишечника, метаболизм триптофана, L‑кинуренин, колоректальный рак