Clear Sky Science · ru
Определение накопления молекул в Escherichia coli с помощью реакции «click»
Почему мелким препаратам сложно добраться до опасных бактерий
Современная медицина зависит от антибиотиков, но некоторые из самых опасных бактерий теперь защищены прочными внешними оболочками, которые удерживают многие лекарства снаружи. Грамположительные (исключение) — нет; грам‑отрицательные бактерии, такие как Escherichia coli, обладают особенно эффективным барьером внешней мембраны, что затрудняет создание препаратов, которые действительно проникают внутрь и достигают своих целей. В этой работе представлен новый лабораторный тест, названный CHAMP‑ассай, который позволяет учёным быстро измерять, насколько хорошо тысячи различных малых молекул преодолевают эти защиты и накапливаются внутри живых клеток E. coli.
Новый способ наблюдать за проникновением препаратов в бактерии
Традиционное открытие антибиотиков опиралось на природные соединения и простые тесты роста, которые показывали, выжили ли бактерии. Эти тесты не раскрывают, сколько препарата действительно попало в клетку и куда он направился внутри. Авторы поставили цель создать прямой и широко применимый метод отслеживания проникновения препарата в цитозоль бактерии — жидкую внутреннюю среду, где находятся многие мишени антибиотиков. Их задача — уйти от грубых показателей вроде минимальной ингибирующей концентрации (MIC), которые смешивают эффекты поглощения препарата, связывания с мишенью и последующей биологии, и вместо этого получить чистое измерение внутриклеточного накопления.
Преобразование бактерий в крошечные химические регистраторы
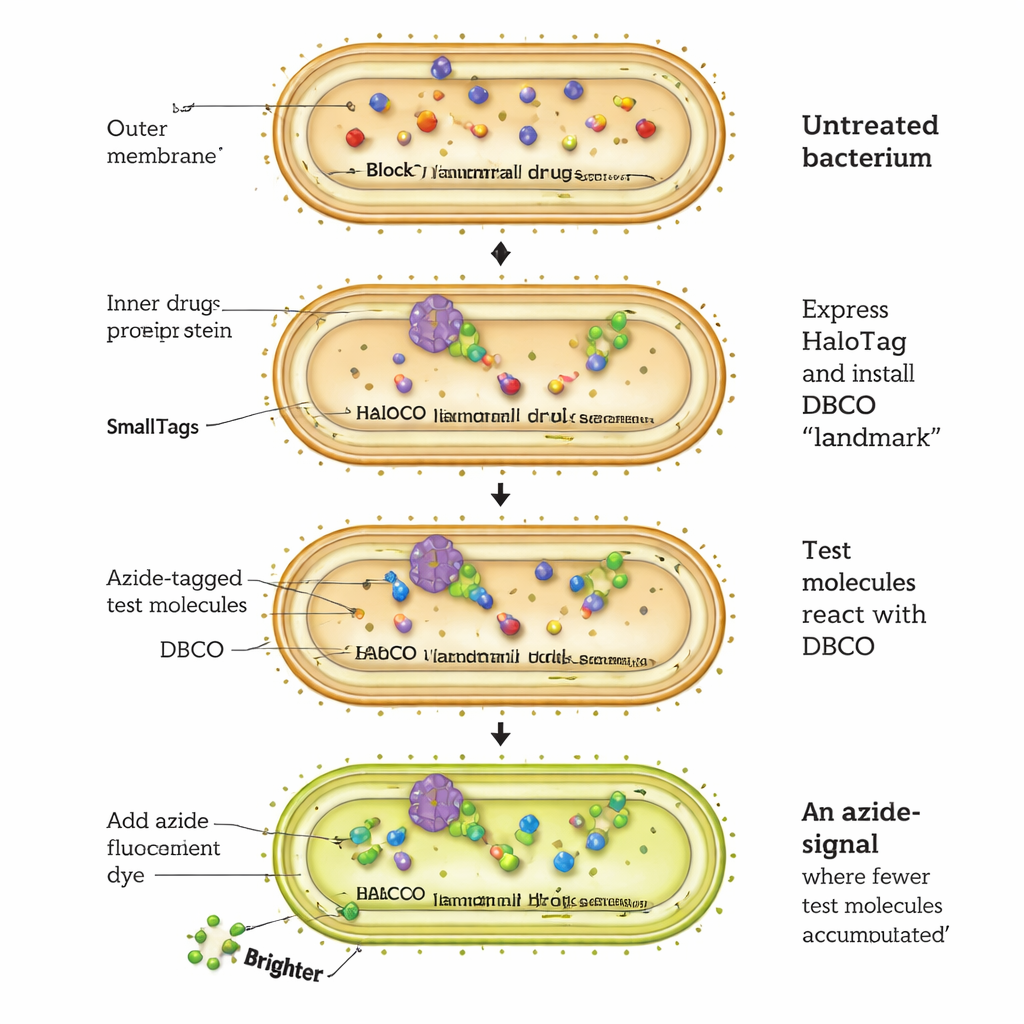
CHAMP‑ассай работает путём перепрограммирования бактериального белка HaloTag в некую молекулярную посадочную площадку. Клетки E. coli генетически модифицированы для продукции HaloTag в цитозоле. Сначала исследователи прикрепляют к HaloTag специальную химическую ручку — «напряжённый» алкин DBCO — через короткий хлороалкильный линкер. Затем бактерии подвергают воздействию испытуемых молекул, каждая из которых несёт очень маленькую азидную метку. Только те молекулы, которые пересекли внешнюю мембрану, прошли через внутреннюю мембрану и достигли цитозоля, могут вступить в реакцию с DBCO в высокоспецифичной «click»‑реакции, навсегда пометив HaloTag. Наконец клетки обрабатывают флуоресцентным красителем с азидной меткой, который может связаться только с оставшимися неоккупированными DBCO. Чем ярче флуоресценция, тем меньше испытуемых молекул попало в цитозоль; более тусклые клетки указывают на лучшее накопление.
Исследование того, как химия и биология формируют проникновение
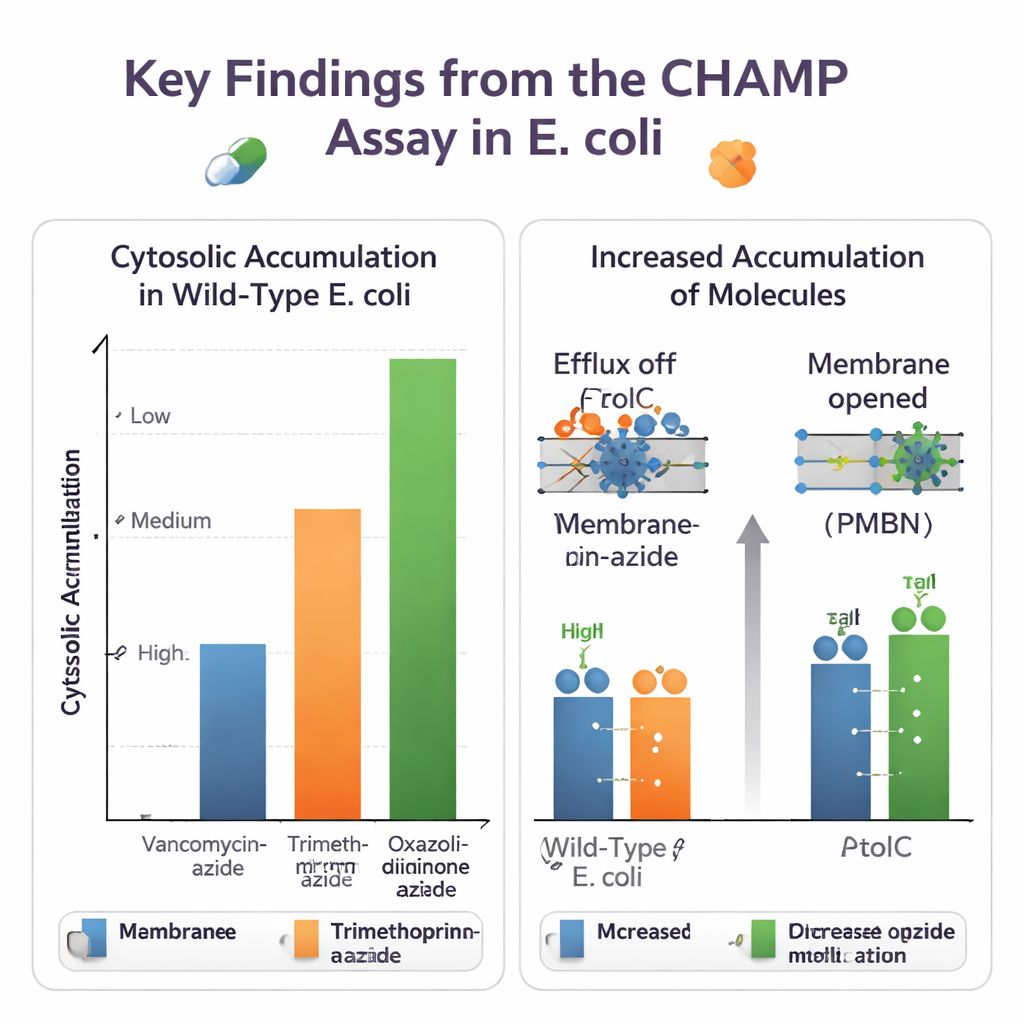
С помощью CHAMP команда сначала тонко настроила экспрессию HaloTag, количество якоря DBCO и выбор флуоресцентных красителей, чтобы получить большое и надёжное окно сигнала. Затем они использовали наборы близкородственных малых молекул, чтобы увидеть, как химические правки влияют на проникновение. Превращение карбоновых кислот в амиды и добавление или удаление основных аминокислотных групп заметно меняли уровни в цитозоле. Во многих случаях первичные амины усиливали накопление, что созвучно независимым «правилам eNTRy», разработанным другими группами. Ассай также работал с азид‑помеченными версиями реальных антибиотиков, выявляя большие различия: массивные препараты, такие как ванкомицин, едва достигали цитозоля, в то время как более мелкие антибиотики, например производные триметоприма и некоторые оксазолидиноны, проникали значительно легче.
Обнажение бактериальных защит, выкачивающих препараты обратно
Поскольку метод проводится в живых генетически программируемых бактериях, он может распутать роли разных клеточных защит. Авторы сравнили нормальные E. coli со штаммами, лишёнными TolC — ключевого компонента крупного многопрепаратного эффлюкс‑насоса, — а также с клетками, обработанными малой молекулой‑ингибитором TolC. Для новобицина и нескольких других азид‑помеченных антибиотиков CHAMP ясно показал более высокое цитозольное накопление при выключенном TolC, подтвердив эти соединения как субстраты эффлюкса. Они также проверили способы ослабления барьера внешней мембраны — химически с помощью пептида PMBN или генетически за счёт сверхэкспрессии широко открытого порина. Многие молекулы, которые ранее плохо накапливались, показали значительный прирост при пермеabilизации мембраны, подчёркивая, как проникновение и эффлюкс совместно определяют внутренние уровни препарата.
Масштабирование до тысяч молекул для выявления закономерностей и правил
Чтобы продемонстрировать действительно высокую пропускную способность, исследователи просcreenировали коммерческий набор из 404 азид‑помеченных соединений и пользовательскую библиотеку из 1 152 азид‑несущих молекул. Они измеряли накопление в нескольких бактериальных контекстах, включая необработанные клетки, клетки, обработанные PMBN, гиперпоринизированные клетки и гиперпоринизированные клетки без TolC. Сравнивая одни и те же молекулы в разных условиях, можно было увидеть, какие изменения обусловлены клеточной биологией, а не особенностями скорости click‑реакции. Объединяя данные CHAMP с вычислительным анализом, они связали определённые физико‑химические характеристики — такие как полярная поверхность, способность к образованию водородных связей и специфические кольцевые скелеты — с более сильным распознаванием со стороны эффлюкса на базе TolC. Такое масштабное профилирование начинает вырисовывать правила проектирования молекул, которые либо избегают насосов, либо более эффективно используют порины.
Что это значит для будущих антибиотиков
Проще говоря, эта работа превращает E. coli в высокопроизводительный сенсор, который сообщает, сколько тестового соединения попало в ту часть клетки, где находятся многие мишени препаратов. CHAMP не заменяет тесты, показывающие, убиты ли бактерии, но заполняет важный пробел, отделяя «попадание внутрь» от «вызванного вреда». С возможностью измерять более тысячи молекул в разных мутантных или химически модифицированных штаммах за несколько дней, исследователи теперь могут систематически изучать, какие химические особенности способствуют проникновению, уменьшают эффлюкс или выигрывают от партнёров, разрушающих мембрану. Эти знания должны ускорить разработку новых антибиотиков и вспомогательных препаратов, способных пробить грозные защиты грамотрицательных патогенов, прежде чем резистентность отнимет ещё большую часть арсенала антибиотиков.
Цитирование: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Ключевые слова: антибиотикорезистентность, Escherichia coli, проницаемость лекарств, эффлюксные насосы, click‑химия