Clear Sky Science · ru
Географическое распространение устойчивости к антимикробным препаратам после массового распределения азитромицина
Почему это важно для детского здоровья
Азитромицин, широко используемый антибиотик, применяли в массовых кампаниях по раздаче лекарств, чтобы спасти жизни маленьких детей в некоторых районах субсахарской Африки, в том числе в Нигере. Эти кампании сократили детскую смертность, но вызвали серьёзную озабоченность: не способствуют ли они также распространению устойчивых к препаратам бактерий из обработанных деревень в соседние общины, которые никогда не получали лекарство? В этом исследовании задают вопрос, происходит ли такое «перетекание» устойчивости между деревнями — ключевой вопрос для стран, взвешивающих преимущества и риски расширения таких программ.
Жизнеспасающие кампании и их скрытый риск
Ранние крупные испытания показали, что двукратное в год назначение азитромицина всем маленьким детям в районах с высокой смертностью снижает число погибших примерно на 14–18 процентов. Этот успех побудил Всемирную организацию здравоохранения и правительства, в том числе Нигера, рассмотреть более широкое применение этой стратегии. Однако антибиотики убивают не только вредные бактерии — они также создают благоприятные условия для выживания штаммов, способных к ним противостоять. В предыдущих работах та же группа исследователей наблюдала явные признаки бактерий, устойчивых к азитромицину, у обработанных детей. Не было известно, остаются ли эти устойчивые микробы внутри обработанных деревень или распространяются наружу, подрывая эффективность антибиотика для других.
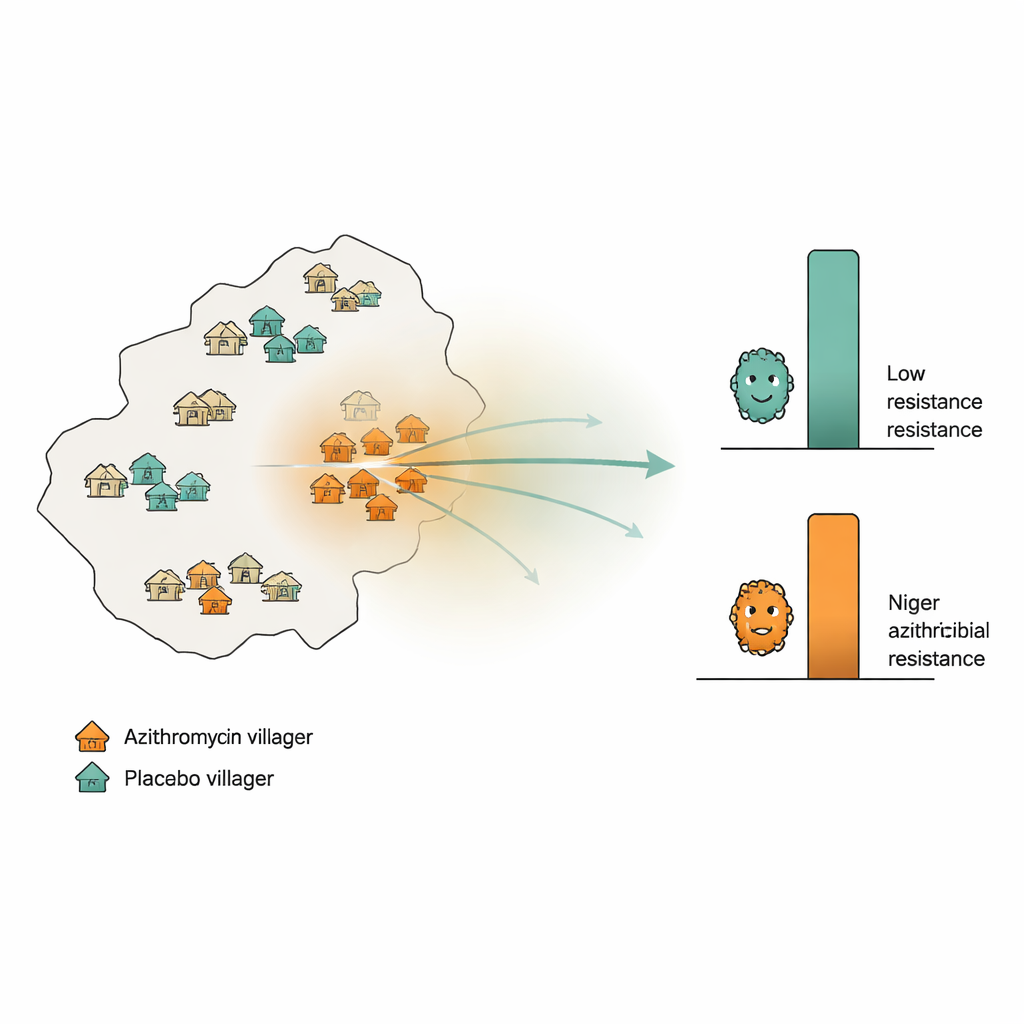
Отслеживание устойчивости в сельском ландшафте
Исследователи воспользовались крупным испытанием по снижению детской смертности в регионе Доссо в Нигере, где 594 деревни были случайным образом распределены для получения азитромицина или неактивного плацебо дважды в год в течение двух лет. Кроме того, было случайно отобрано 30 отдельных «мониторинговых» деревень: половина получила азитромицин, половина — плацебо. Из этих мониторинговых деревень команда взяла ректальные мазки у 10 детей в каждой деревне в начале испытания и снова через 24 месяца. С помощью глубокого секвенирования ДНК они измеряли, сколько генов, связанных с устойчивостью к макролидам (классу антибиотиков, к которому относится азитромицин), в среднем присутствовало в каждой деревне. Они также рассчитали для каждой мониторинговой деревни интенсивность использования азитромицина в окружающей местности — считая все дозы, выданные в ближайших деревнях, и придавая больший вес более близким деревням.
Поиск признаков распространения между деревнями
Если бы устойчивая популяция распространялась географически, исследователи ожидали бы увидеть более высокий уровень генов устойчивости в деревнях с плацебо, которые окружены интенсивно обрабатываемыми соседями, по сравнению с плацебо-деревнями в зонах с низким использованием азитромицина. Они проверяли эту идею несколькими способами: изучали простые ранговые корреляции между интенсивностью лечения поблизости и устойчивостью; повторяли анализ в различных диапазонах дистанций (в пределах 10, 20 или 30 километров); и использовали строгую стратегию перестановок, при которой метки лечения в большем испытании перемешивали, чтобы выяснить, могли ли наблюдаемые закономерности возникнуть случайно. Также был проведён «негативный контроль» — те же расчёты повторяли, используя дозы плацебо вместо доз азитромицина; похожая картина в этом анализе указывала бы на конфаундирование, а не на реальное перетекание.
Что показали данные об устойчивости
Во всех этих проверках в деревнях с плацебо наблюдались низкие уровни генов устойчивости к макролидам, которые оставались близки к исходному уровню, независимо от того, сколько азитромицина использовалось вокруг них. Статистические тесты не обнаружили значимой связи между окружающим использованием препарата и уровнем устойчивости в этих необработанных общинах. В противоположность этому, в деревнях, где собственные дети получали азитромицин, за два года наблюдалось заметное увеличение генов устойчивости, что согласуется с прямым отбором под воздействием лечения — но это увеличение не становилось систематически сильнее в районах с более высокой интенсивностью лечения вокруг. Когда исследователи анализировали живые пневмококковые бактерии из носовых полостей детей, они вновь не обнаружили связи между географической интенсивностью лечения и устойчивостью. Анализы с использованием разных математических моделей и альтернативных определений интенсивности лечения пришли к тому же общему выводу.
Ограничения, оговорки и более широкая перспектива
Исследование не может полностью исключить небольшие эффекты перетекания, особенно учитывая, что только 30 мониторинговых деревень были тщательно обследованы, и в нём не рассматривалось очень мелкомасштабное распространение внутри домохозяйств или внутри отдельных деревень. Оно также предполагает, что расстояние и число доз являются основными факторами распространения, и фокусируется на двухлетнем временном окне; долгосрочные эффекты или другие варианты программ, например обработка всех сообществ для профилактики заболеваний глаз, могут проявлять иные паттерны. Тем не менее имеющиеся свидетельства указывают на то, что в этом контексте большая часть давления по отбору устойчивости от массовых кампаний с азитромицином ограничена сообществами, которые фактически получают препарат, а не бессимптомно распространяется по ландшафту.
Что это значит для будущих антибиотикальных кампаний
Для чиновников здравоохранения в таких странах, как Нигер, эти результаты дают осторожное успокоение. Хотя массовые обработки азитромицином действительно повышают устойчивость внутри обработанных деревень, это исследование не выявило убедительных признаков того, что такая устойчивость в течение 24 месяцев просачивается в соседние необработанные деревни. Это означает, что предыдущие оценки риска развития устойчивости в этих испытаниях по снижению детской смертности вряд ли сильно искажены незамеченным географическим перетеканием. Политики по-прежнему должны взвешивать спасающие жизни преимущества таких кампаний против локального роста устойчивости, но теперь они могут делать это с большей уверенностью, что, по крайней мере в среднесрочной перспективе и на уровне «деревня — деревня», проблема не быстро распространяется наружу.
Цитирование: Srivathsan, A., Arzika, A.M., Maliki, R. et al. Geographic spillover of antimicrobial resistance from mass distribution of azithromycin. Nat Commun 17, 2152 (2026). https://doi.org/10.1038/s41467-026-68691-y
Ключевые слова: устойчивость к антимикробным препаратам, азитромицин, массовое распределение лекарств, детская смертность, Нигер