Clear Sky Science · ru
Функциональные и структурные сведения о взаимодействиях между β-аррестином 1 и Gαs или Gαi1
Почему это важно для здоровья и медицины
Многие современные лекарства — от противоаллергических таблеток до препаратов для сердца и психиатрических средств — действуют через большую семью белков на поверхности клеток, называемых рецепторами, сопряжёнными с G-белками (GPCR). Эти рецепторы передают сигналы в клетку при помощи двух основных помощников: G-белков и белков, называемых бета-аррестинами. В данном исследовании изучается, как один бета-аррестин (β-аррестин 1) непосредственно взаимодействует с двумя типами G-белков внутри клетки. Понимание этой скрытой «переписки» может помочь учёным разрабатывать более точные лекарства с меньшими побочными эффектами, тонко настраивая поток сигналов внутри клеток.
Два главных посредника внутри клетки
Когда гормон или лекарство связывается с GPCR на поверхности клетки, запускаются два основных пути передачи сигнала. Один путь использует G-белки, которые функционируют как молекулярные таймеры, переключаясь путём замены одной малой молекулы (GDP) на другую (GTP). Другой путь использует бета-аррестины, которые могут как прекращать сигнализацию через G-белки, так и запускать собственные сигнальные каскады. Долгое время исследователи в основном изучали, как рецепторы взаимодействуют либо с G-белками, либо с бета-аррестинами по отдельности. Более поздние работы намекали, что G-белки и бета-аррестины могут также связываться друг с другом или даже образовывать большие «мега-комплексы» с рецептором. Однако детали того, как эти белки соединяются и что это значит для сигнализации, оставались неясными.
Измерение того, кто с кем связывается
В этом исследовании учёные сосредоточились на β-аррестине 1 и двух «альфа»-субъединицах G-белков: Gαs, который обычно усиливает клеточную активность, и Gαi1, который, как правило, её подавляет. Используя чувствительный метод измерения связывания, они проверяли, насколько прочно очищенный β-аррестин 1 и каждый G-белок соединяются друг с другом в разных условиях. Они обнаружили, что ключевой фактор — не в том, «включён» ли G-белок, а в том, находится ли β-аррестин 1 в более активной, гибкой форме. Вариант β-аррестина 1 без хвостовой части — который ведёт себя как рыхлый, активный ансамбль конформаций — прочно связывался и с Gαs, и с Gαi1. Напротив, покоящаяся форма β-аррестина 1 или форма, заблокированная пептидом, подобным хвосту рецептора, связывались слабо или вовсе не связывались. Это указывает на то, что G-белки предпочитают распознавать β-аррестин 1, когда он принимает активоподобные конформации, которые могут возникать после активации рецептора. 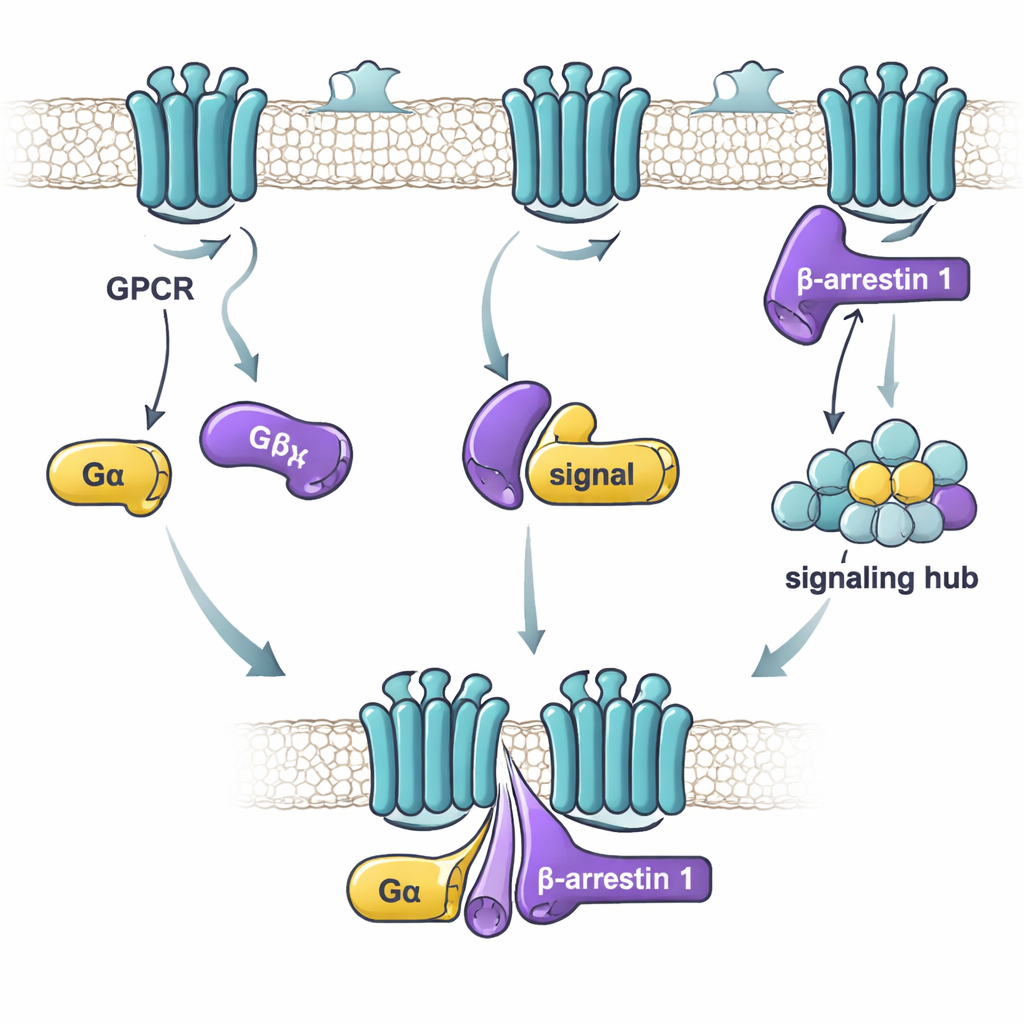
Наблюдение тонких изменений формы
Чтобы увидеть, как связывание влияет на конформацию белков, команда использовала метод, отслеживающий скорость замены атомов водорода в цепочке белка на тяжелый водород из раствора. Более медленная замена обычно означает, что участок стал более защищённым или жёстким; более быстрая замена указывает на повышение гибкости или оголённость. Когда активоподобный фрагмент β-аррестина 1 связывался с Gαs или Gαi1, оба G-белка демонстрировали чёткие изменения паттернов в нескольких областях, что указывает на перестройку их структуры вокруг комплекса. В то же время сам β-аррестин 1 менялся лишь незначительно, в основном в гибких петлях. Работая с изолированными доменами G-белков, исследователи также показали, что и основная каталитическая «Ras-подобная» часть, и окружающая её альфа-спиральная область вносят вклад в связывание. Для Gαs спиральная область играет особенно важную роль; для Gαi1 обе области примерно одинаково значимы.
Функция без переключения главного выключателя
Далее возник вопрос: меняет ли этот прямой контакт то, как G-белки «включаются». Команда использовала флуоресцентный зонд, имитирующий GTP, который светится при переходе G-белка от GDP к GTP — стандартный показатель активации. К удивлению, добавление β-аррестина 1 не изменяло скорость или степень этой нуклеотидной замены ни для Gαs, ни для Gαi1. Иными словами, β-аррестин 1 не действует как классический фермент, включающий G-белки. Вместо этого его влияние проявлялось на собственной структуре. Используя искусственно модифицированный β-аррестин 1, движение хвоста которого можно было отслеживать по флуоресценции, они выяснили, что активный Gαs, но не Gαi1, усиливает высвобождение C-концевого хвоста β-аррестина в присутствии пептида, происходящего от рецептора. В живых клетках дополнительная визуализация и сенсоры переноса энергии подтвердили, что Gαs и β-аррестин 1 сближаются при стимуляции гормоном и что Gαs способствует сдвигу β-аррестина 1 в более активную конформацию. 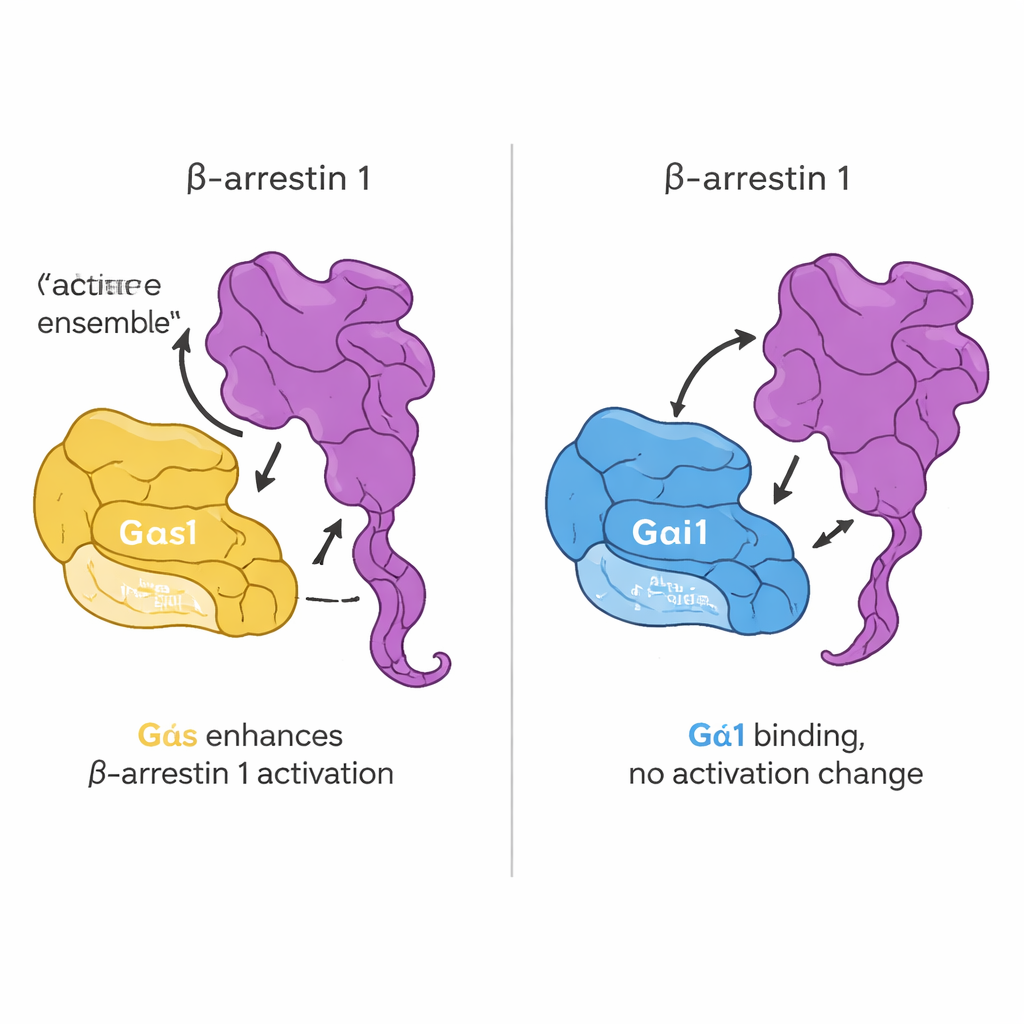
Новый уровень регуляции в клеточной сигнализации
Сводя эти результаты воедино, исследование предлагает, что Gαs и Gαi1 оба напрямую связываются с β-аррестином 1, но несколько по-разному и с отличающимися последствиями. Ни один из G-белков при этом не меняет своего основного «включён/выключен» поведения из-за этого контакта. Вместо этого, особенно в случае Gαs, взаимодействие действует скорее как точная настройка для β-аррестина 1, подталкивая его к более активной, с освобождённым хвостом форме или стабилизируя её. Это добавляет ранее недооценённый уровень к GPCR-сигнализации: рецепторы не только координируют работу G-белков и бета-аррестинов, но и G-белки и бета-аррестины могут напрямую модулировать друг друга. В долгосрочной перспективе картирование этих тонких взаимодействий может помочь разработчикам лекарств направлять сигнализацию по полезным путям — усиливая благоприятные каскады и избегая тех, которые вызывают побочные эффекты.
Цитирование: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Ключевые слова: рецепторы, сопряжённые с G-белками, бета-аррестин, G-белковая сигнализация, механизмы клеточной сигнализации, структурная биология