Clear Sky Science · ru
Эпигеномный анализ выявляет метилирование ДНК — медиаторы кардиометаболического риска, связанного с лечением, у переживших рак в детстве
Почему последствия рака остаются в организме
Благодаря улучшению методов лечения большинство детей с раком выживает и вырастает. Но многие из этих переживших столкнутся с новыми проблемами со здоровьем через десятилетия, включая ожирение, повышенное кровяное давление и состояния, сходные с диабетом. В этом исследовании поставлен важный вопрос: как лечение, проведённое в детстве, оставляет такие долгие следы в сердечно-сосудистой и метаболической системах? Анализируя химические метки на ДНК в клетках крови, исследователи находят подсказки, что прошлые химио‑ и лучевые терапии могут «перепрограммировать» организм так, что это повышает долгосрочный кардиометаболический риск.
Отслеживание скрытых рисков у взрослых, переживших рак в детстве
Группа изучала почти 3000 взрослых, переживших рак в детстве, наблюдаемых в долгосрочном когортном исследовании St. Jude Lifetime Cohort. Эти пациенты в детстве получали разные виды химиотерапии и облучение головы или туловища (грудной клетки, живота, таза), а затем через годы приходили на детальные обследования и сдавали кровь. Учёные сосредоточились на пяти ключевых кардиометаболических проблемах, известных как факторы риска сердечных заболеваний и преждевременной смерти: ожирение, нарушение регуляции сахара в крови, высокий уровень триглицеридов, высокий холестерин и повышенное кровяное давление. Сравнивая переживших с этими состояниями и без них, они искали различия в метилировании ДНК по миллионам позиций в геноме — крошечные химические «выключатели», помогающие регулировать, какие гены включаются или выключаются.
Химические метки на ДНК как память о лечении
По всему геному исследователи обнаружили почти 1900 участков ДНК, где уровни метилирования были связаны по крайней мере с одной из пяти кардиометаболических проблем. Большинство этих сайтов ассоциировались с одной проблемой, но небольшая группа выступала как «узлы», связанные сразу с несколькими состояниями. Пять ключевых сайтов, расположенных рядом с двумя генами CPT1A и LMNA, были связаны со всеми пятью рисками одновременно. Эти гены известны тем, что влияют на обмен жиров и на поддержание структуры клеток, что указывает на то, что лечение может нарушать общие метаболические и сердечно‑сосудистые пути. Многие изменения метилирования перекрывались с сигналами, ранее выявленными в общей популяции, особенно с теми, что связаны с воспалением, но другие изменения казались характерными именно для переживших рак — что указывает на то, что лечение оставляет свой отличительный биологический след.
Связывание терапии, изменений ДНК и болезни
Следующим шагом было проверить, действительно ли эти изменения метилирования помогают объяснить, как лечение приводит к поздним заболеваниям, а не просто сопутствуют им. Исследователи сосредоточились на новых или ухудшающихся кардиометаболических проблемах, которые развились только после взятия образца крови, что сохраняет хронологию: от лечения к изменению ДНК к болезни. С помощью статистических медиаторных анализов они выявили 24 сайта метилирования, которые в совокупности объясняли до примерно четверти связи между конкретными видами лечения и последующими кардиометаболическими проблемами. Особенно сильные шаблоны наблюдались при облучении головы и туловища: группы сайтов метилирования совместно объясняли примерно 10–20% воздействия этих радиотерапий на нарушение регуляции сахара в крови. Один примечательный сайт, рядом с геном ANTXR2, по-видимому, опосредовал около 20% эффекта облучения туловища на последующие проблемы с глюкозой.
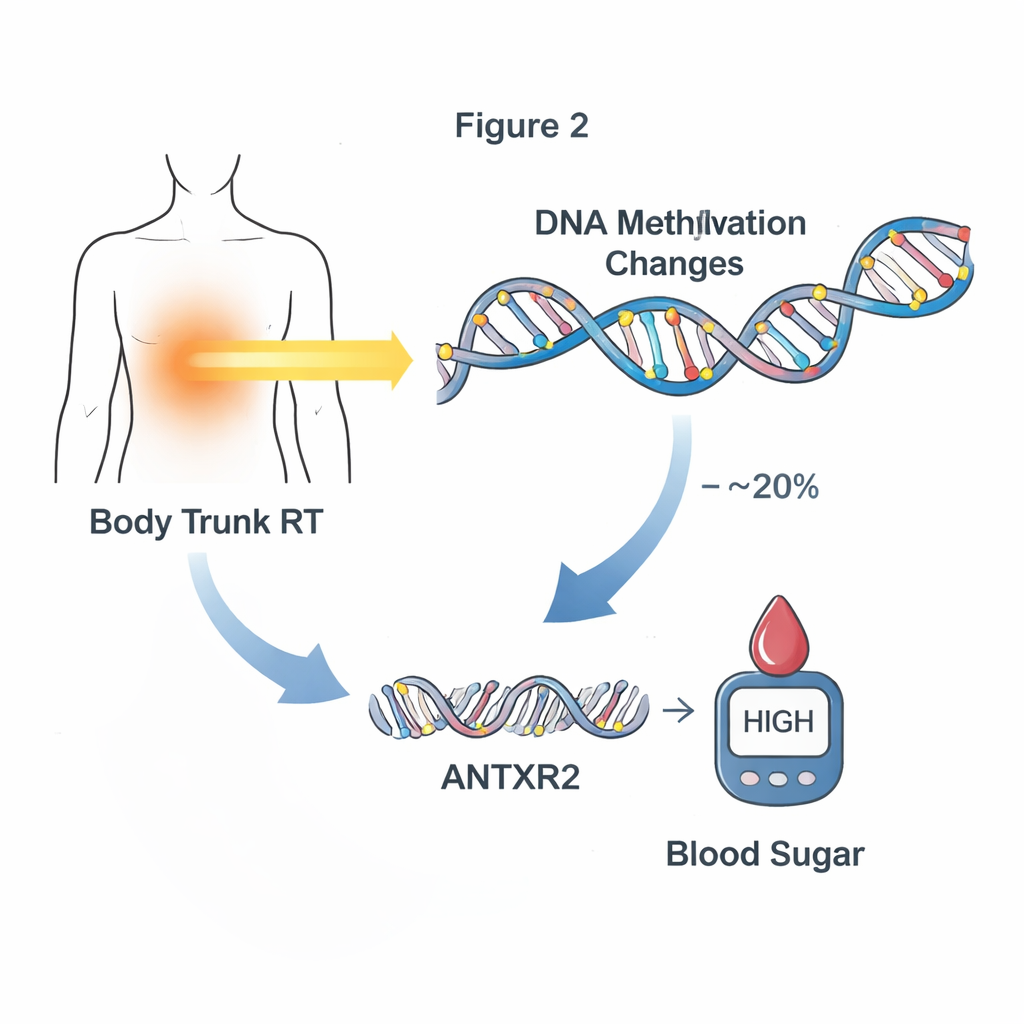
От меток ДНК к активности генов
Чтобы понять, как эти метки метилирования могут менять биологию, команда изучила активность генов у подгруппы переживших, для которых были доступны как данные ДНК, так и РНК из крови. Они обнаружили десятки сайтов метилирования, где более высокое или более низкое метилирование было связано с изменением экспрессии соседних генов. Среди них был ключевой медиаторный сайт рядом с ANTXR2, где уровни метилирования тесно коррелировали с уровнем экспрессии этого гена, особенно у переживших, получивших облучение туловища. ANTXR2 участвует в регуляции кровеносных сосудов и внеклеточного каркаса тканей — систем, влияющих на транспорт глюкозы и инсулина в организме. Такая картина указывает на цепочку событий, в которой радиация изменяет метилирование, это меняет активность генов, что, в свою очередь, может подтолкнуть организм к нарушению регуляции сахара в крови.
Что это значит для переживших и будущей помощи
Для неспециалистов главный вывод таков: лечение рака в детстве не только повреждает ткани в момент терапии; оно может также оставлять долговременные «заметки» на ДНК, формирующие здоровье на десятилетия вперёд. В этом исследовании некоторые из таких заметок — изменения метилирования ДНК — помогают объяснить, почему определённые пережившие имеют более высокую вероятность развития ожирения, повышенных липидов в крови или нарушений глюкозы, связанных с диабетом и сердечными заболеваниями. Хотя эти химические метки — лишь часть истории, они в перспективе могут служить маркёрами в крови для выявления переживших с наибольшим риском и для проверки, могут ли изменения образа жизни или новые терапии безопасно «переписать» часть этой эпигенетической истории. Работа приближает уход за пережившими к персонализированной медицине: использованию молекулярных следов прошлой терапии для более ранней и более точной профилактики сердечно‑сосудистых и метаболических заболеваний.
Цитирование: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Ключевые слова: пережившие рак в детстве, метилирование ДНК, кардиометаболический риск, лучевая терапия, эпигенетика