Clear Sky Science · ru
Ко-трансляционная определённость тетрагичных структур в фабриках шаперонов
Как клеточные «сборочные линии» поддерживают крупные машины в порядке
Внутри каждой нашей клетки тысячи белковых деталей должны точно собираться в сложные молекулярные машины — от двигателей, копирующих ДНК, до фабрик, синтезирующих другие РНК. В этом исследовании задаётся на первый взгляд простой, но важный вопрос: как клетки в реальном времени решают, какие вспомогательные белки будут сопровождать каждую новую деталь в момент её сборки, и как они удерживают этот процесс организованным в хаотичной клеточной среде?
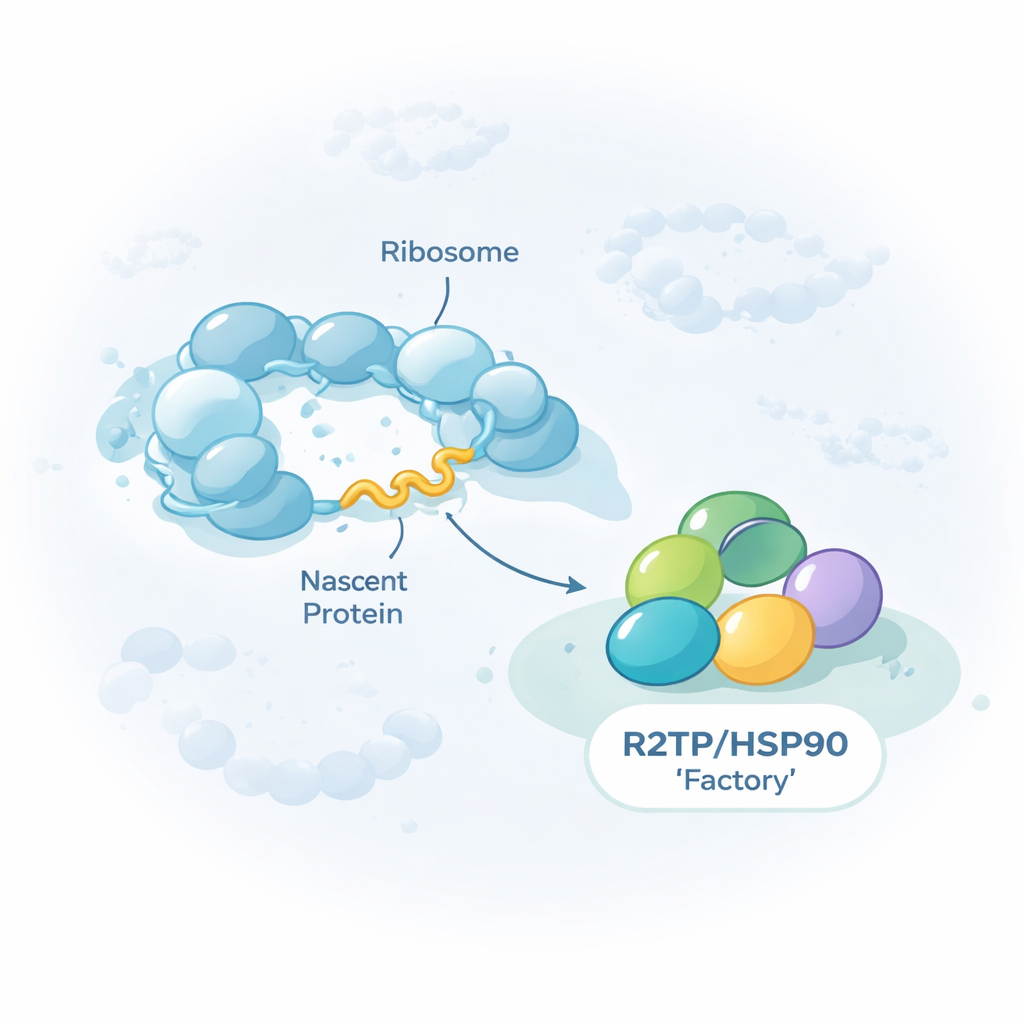
Универсальный помощник для клеточных мегамашин
Работа сосредоточена на группе вспомогательных белков, или шаперонов, известных как HSP90/R2TP. В отличие от шаперонов, которые помогают свернуть отдельные белки, этот комплекс специализируется на сборке гигантских многокомпонентных комплексов, включая три ядерные РНК‑полимеразы, транскрибирующие ДНК в РНК, отдельные рибо-РНК‑частицы и крупные риформирующие комплексы, меняющие упаковку ДНК. Авторы показывают, что R2TP не встречает своих клиентов только после их окончательной сборки. Напротив, он часто присоединяется ещё во время синтеза каждого белка на рибосомах — клеточных «фабриках» белка. Путём вычленения R2TP из человеческих клеток и секвенирования сопутствующей РНК они обнаружили около 150 матричных РНК, кодируемые белки которых контактируют с R2TP в ходе собственной трансляции.
Помощники, которые «ехать» по нарастающим полипептидным цепям
Чтобы проверить, действительно ли это связывание происходит во время синтеза белка, исследователи применяли препараты, замораживающие или нарушающие трансляцию. Когда использовали соединения, срывающие нарастающие белковые цепи с рибосом, большинство матричных РНК исчезало из связей с R2TP. Но при применении препарата, который просто приостанавливает рибосомы, оставляя незрелые цепи прикреплёнными, связывание R2TP увеличивалось. Эксперименты с конструкциями‑репортёрами подтвердили это: если трансляция искусственно прекращалась преждевременно, шаперон больше не связывался с сообщением. В совокупности эти результаты указывают на ясное правило взаимодействия: R2TP распознаёт своих клиентов прежде всего по возникающей белковой цепи, выходящей из рибосомы, а не по последовательности РНК как таковой.
«Фабрики», собранные шаперонами, которые собирают конкретные сообщения
С помощью продвинутой одиночномолекулярной визуализации авторы сделали неожиданное открытие. Вместо множества разных сообщений, случайно разбросанных по цитоплазме, они наблюдали, что некоторые ключевые сообщения — особенно кодирующие крупные субъединицы РНК‑полимеразы II и большой фактор сплайсинга PRPF8 — часто собираются в яркие очаги в цитоплазме. Эти очаги были обогащены R2TP и его партнёром HSP90, а также компонентами рибосом и самими синтезирующимися белками, что указывает на то, что это активные сайты трансляции. При блокировании трансляции или энергоёмкой АТФазной активности R2TP или HSP90 эти очаги растворялись. Авторы предлагают называть эти структуры «фабриками R2TP»: специализированными конденсатами, где избирательные матричные РНК и шапероны концентрируются для своевременного и защитного контакта между возникающими белковыми цепями и их сборочными помощниками.
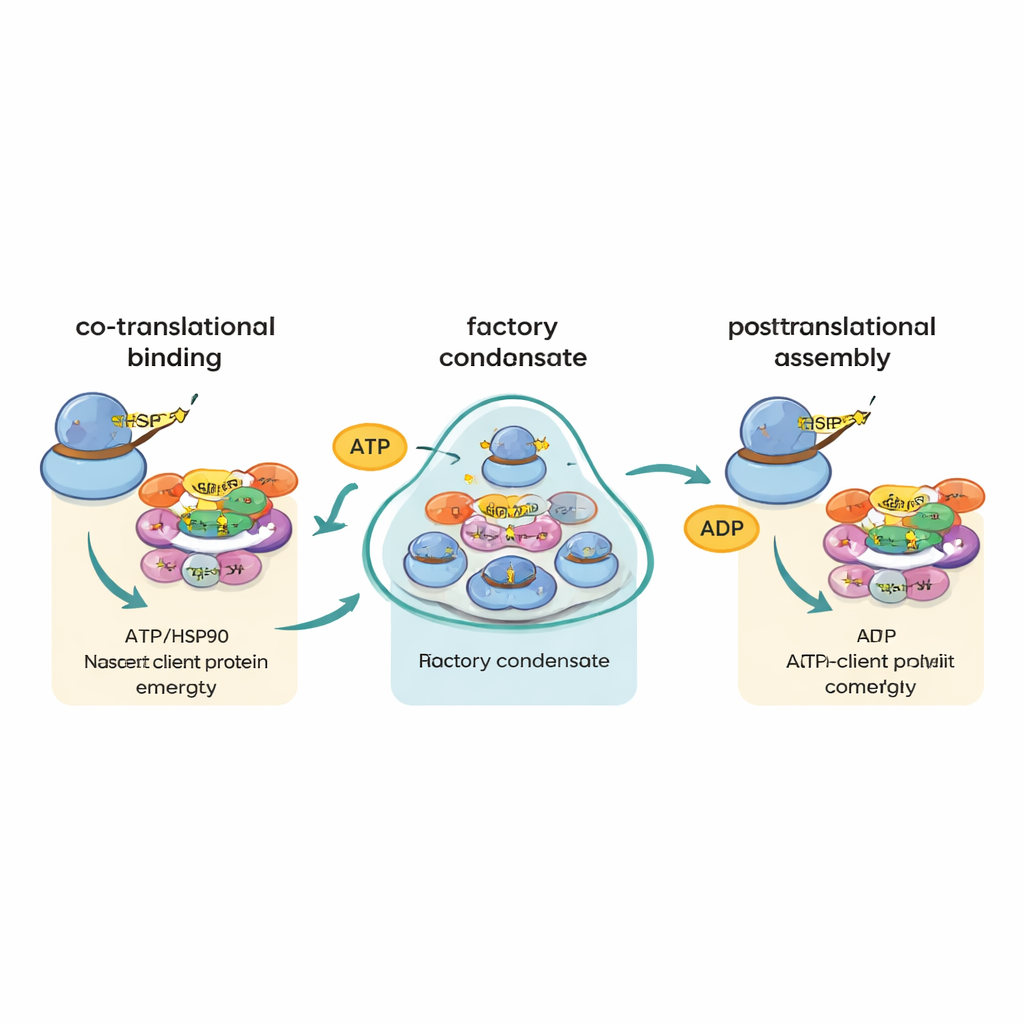
Маршрутизация деталей без сопоставления чертежей
Ранее предполагали, что сообщения, кодирующие разные части одного комплекса, могут находить друг друга и переводиться рядом, что позволило бы их продуктам сразу же собираться вместе. Новая работа в значительной мере опровергает эту модель «ко‑локализованных чертежей». Даже для пар белков, известных тем, что они входят в один комплекс, их матричные РНК редко находились вместе. Вместо этого данные поддерживают другую стратегию, которую авторы называют «ко‑трансляционным шаперонным канальцированием» или «ча‑ча». В этой схеме, когда каждая большая или склонная к агрегированию белковая цепь начинает выходить из рибосомы, R2TP и HSP90 захватывают её и определяют дальнейшую судьбу, направляя через последующие этапы сборки. Сами фабрики в основном не сводят вместе соответствующие сообщения; скорее они повышают вероятность того, что уязвимые новые белки быстро встретят нужный шаперон.
Почему эта скрытая организация важна для здоровья и болезней
Показав, что R2TP и HSP90 не только защищают хрупкие белковые фрагменты, но и формируют места и способы их трансляции, исследование открывает неожиданный уровень внутриклеточной организации. Механизм «ча‑ча» помогает объяснить, как клетки надёжно собирают огромные молекулярные комплексы, несмотря на то, что сообщения для их составных частей редко находятся в одном и том же месте. Это также проясняет, почему дефекты в шаперонах или их энергетических циклах могут дестабилизировать жизненно важные машины, такие как РНК‑полимераза и факторы сплайсинга, с последствиями от нарушений развития до рака. По сути, работа показывает, что клетки полагаются на динамичные шаперонные «фабрики», которые направляют только что синтезированные части в нужные сборки, сохраняя свою внутреннюю машину эффективной и упорядоченной.
Цитирование: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Ключевые слова: белковые шапероны, ко-трансляционная сборка, молекулярные машины, РНК-полимераза, клеточный контроль качества