Clear Sky Science · ru
Дифференциальное нарушение мембранных липидов липопептидными антибиотиками: колистин и турнерцикламицины
Почему это важно для будущих антибиотиков
Ожидается, что к середине века лекарственно-устойчивые инфекции будут уносить десятки миллионов жизней в год; одними из самых смертоносных виновников являются грамотрицательные бактерии, которые уже противостоят многим антибиотикам. Колистин — один из немногих оставшихся препаратов, способных лечить такие инфекции, но он силён для пациентов и бактерии всё чаще находят способы уклоняться от него. В этом исследовании проанализировано, как действует колистин в сравнении с новой семейством природных антибиотиков — турнерцикламисинами, — что показывает: крошечные химические изменения могут порождать принципиально разные механизмы гибели бактерий и, возможно, приводить к более безопасным лекарствам.
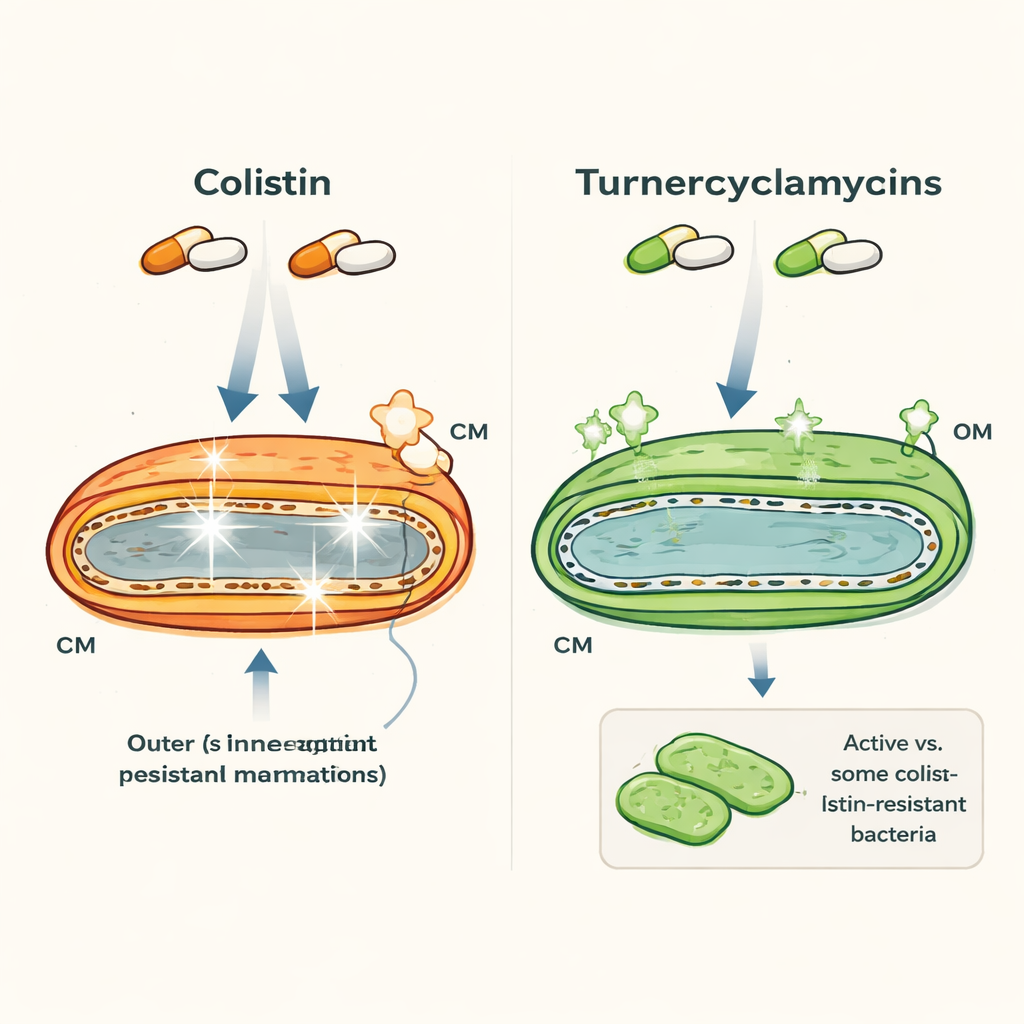
Два похожих на вид препарата с очень разным поведением
Колистин и турнерцикламисины — оба липопептиды: молекулы, объединяющие жирный хвост и пептидное кольцо, и они нацелены на грамотрицательные бактерии, такие как Escherichia coli и Acinetobacter. На первый взгляд они похожи, но их свойства сильно расходятся. Колистин — препарат последней инстанции, действующий быстро, но способный повредить почки и нервы человека, и бактерии всё чаще несут гены резистентности, такие как mcr-1. Турнерцикламисины, выделенные из бактерий, ассоциированных с корабельными червями, могут убивать многие те же патогены, включая некоторые штаммы, устойчивые к колистину, и при этом в лабораторных тестах проявляют гораздо меньшую токсичность. Любопытно, что две версии, отличающиеся лишь небольшим удлинением жирного хвоста, уже демонстрируют разные профили резистентности, что намекает на важность очень тонких структурных особенностей.
Как колистин прокалывает мембраны, а турнерцикламисины действуют постепенно
Авторы использовали флуоресцентные красители, эксперименты по учёту гибели клеток во времени и электронную микроскопию, чтобы наблюдать, как эти препараты воздействуют на бактериальные мембраны. Колистин быстро делает проницаемыми и внешнюю, и внутреннюю (цитоплазматическую) мембраны, что приводит к быстрой гибели клеток в течение нескольких часов. Турнерцикламисины, напротив, убивают медленнее — требуется 6–10 часов для полного очищения культур — и в основном нарушают внешнюю мембрану. Красители, светящиеся при нарушении внутренней мембраны, давали сильный сигнал для колистина, но лишь скромные и запаздывающие сигналы для турнерцикламицинов, а высокоразрешающие изображения подтверждали минимальные видимые повреждения внутренней мембраны даже при гибели клеток. Это указывает на то, что турнерцикламисины не убивают классическим «формированием пор», характерным для многих мембрано-таргетных антибиотиков.
Липидные строительные блоки как скрытые регуляторы
Обе группы препаратов в конечном счёте зависят от бактериального компонента — липополисахарида (LPS), который синтезируется в внутренней мембране и обычно экспортируется на внешнюю поверхность. Когда исследователи отключали ранние шаги биосинтеза LPS, и колистин, и турнерцикламисины теряли активность; но при блокировании транспорта, вывозящего LPS наружу, препараты всё ещё действовали. Это означает, что наличие предшественников LPS необходимо, а их конечное местоположение — нет. Существенная разница появилась при прямом измерении связывания: колистин прочно связывается с очищенным LPS в микромолярном диапазоне, тогда как у турнерцикламицинов измеримого связывания не обнаружилось. Вместо этого активность турнерцикламицинов сильно зависела от других мембранных липидов. Определённые фосфолипиды, особенно фосфатидилглицерин, могли ослаблять или модулировать их действие, и препараты легко захватывались везикулами внешней мембраны — крошечными липидными пузырьками, испускаемыми бактериями.
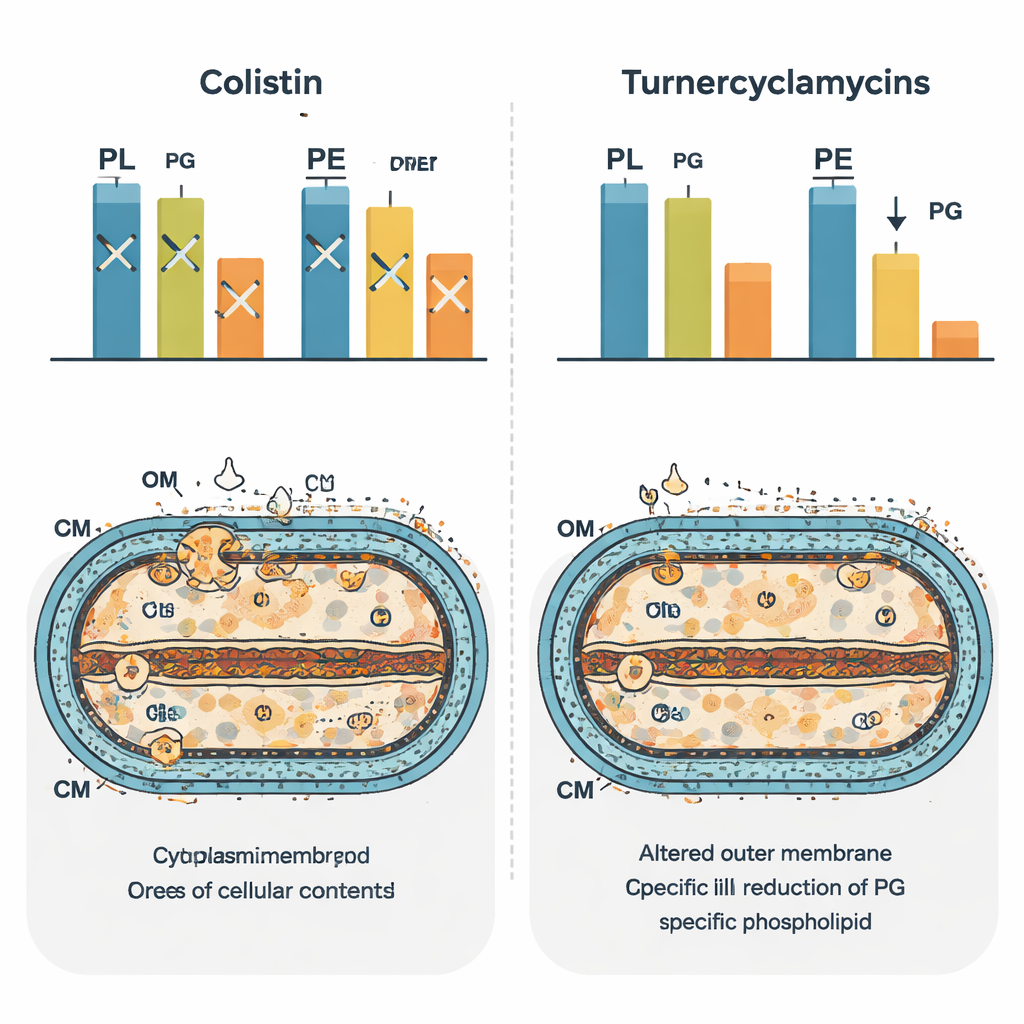
Перестройка липидного ландшафта бактерии
Чтобы увидеть более широкий эффект на клетку, команда использовала масс-спектрометрический «фосфолипидомный» анализ, чтобы каталогизировать сотни липидных видов после обработки. Колистин вызвал характерный набор изменений, отражающий его широкое нарушение гомеостаза мембран. Турнерцикламисины породили иной сигнатурный профиль, который сильно напоминал бактерии, лишённые белка-транспортёра липидов MlaA. В таких клетках определённые диацил-липиды истощались, а моноацильные формы увеличивались, что предполагает нарушение нормального циклинга и ремоделирования фосфолипидов между мембранами. Примечательно, что уровни фосфатидилглицерина падали в клетках, обработанных турнерцикламисинами, что усиливает идею о прямой связи этого липида с их эффективностью. Авторы предполагают, что турнерцикламисины могут действовать как молекулярные мимики, блокирующие пути, связывающие синтез или транспорт жирных кислот, LPS и фосфатидилглицерина.
Что это значит для разработки лучших препаратов
Проще говоря, исследование показывает: колистин убивает, быстро разрывая обе защитные оболочки грамотрицательной бактерии, чему способствует плотное связывание с LPS, тогда как турнерцикламисины действуют скорее как саботажники липидной цепочки поставок клетки. Они внедряются в наружную мембрану, постепенно нарушают синтез и переработку специфичных липидов и в конечном итоге приводят к разрушению наружного конверта — при этом внутреннюю мембрану они сильно не повреждают. Поскольку этот более щадящий и прицельный механизм связан с меньшей токсичностью и иным профилем резистентности, понимание его открывает дорожную карту для создания следующего поколения липопептидных антибиотиков. Тонкая настройка таких параметров, как длина и степень ненасыщенности жирного хвоста, может позволить химикам создать препараты, щадящие ткани человека, сохраняющие активность против штаммов, устойчивых к колистину, и сохраняющие преимущество в продолжающейся гонке с лекарственно-устойчивыми бактериями.
Цитирование: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
Ключевые слова: резистентность к антибиотикам, грамположительные бактерии, колистин, липопептидные антибиотики, мембранные липиды