Clear Sky Science · ru
Структурная основа динамических конформаций AP-4 и его взаимодействия с ARF1
Как клетки сортируют и отправляют свои грузы
Каждая клетка — как оживлённый склад: она постоянно сортирует и отправляет тысячи белковых «посылок» по назначению. Когда эта система доставки даёт сбой в нервных клетках, последствия могут быть серьёзными — нарушения в работе мозга и движении. В этом исследовании раскрывают, как одна ключевая «перевалочная» машина, названная AP-4, меняет форму и объединяется с регулирующим белком ARF1, чтобы загружать груз в крошечные транспортные пузырьки, и почему её подвижность так важна для здоровых нейронов.
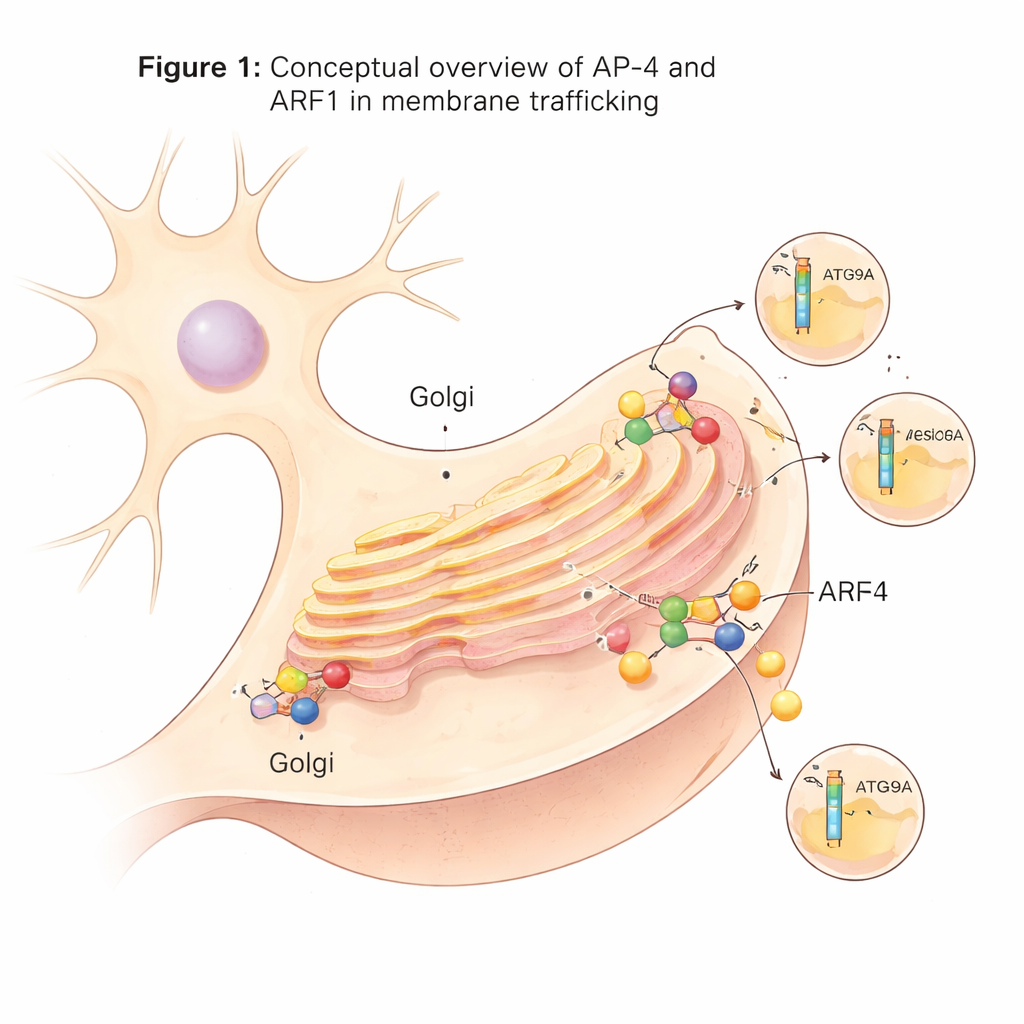
Специализированная «перевалочная» машина в нейронах
Внутри клетки множество транспортных везикул отщепляются от центральной станции сортировки — транс-гилубулиновой сети (trans-Golgi network). Эти везикулы зависят от адаптерных белковых комплексов (AP-комплексов), которые выполняют функцию погрузочных доков: распознают белки-грузы и помогают сформировать покрытые везикулы вокруг них. AP-4 — один из таких адаптеров и необычен тем, что, в отличие от многих других, он не использует обычный скелетный белок клаТрин. Хотя AP-4 присутствует во многих тканях, в нейронах он играет особенно важную роль. При отсутствии или дефекте AP-4 у людей ключевые грузы, такие как белок, связанный с аутофагией ATG9A, и некоторые рецепторы глутамата не перемещаются должным образом, что приводит к тяжёлому нарушению развития, известному как синдром дефицита AP-4.
Комплекс, меняющий форму в покое
Авторы использовали крио-электронную микроскопию — мощный метод визуализации больших белковых ансамблей — чтобы определить трёхмерную структуру «сердцевины» комплекса AP-4 в растворе. AP-4 состоит из четырёх субъединиц, которые вместе образуют структуру, напоминающую чашу. Они обнаружили, что AP-4 не находится в одной жёсткой конформации. Вместо этого он естественно переключается между «закрытой» формой, в которой одна субъединица (С-концевой домен средней субъединицы) уложена в центр «чаши», и «открытой» формой, когда этот фрагмент выходит наружу и становится очень гибким. Дополнительные эксперименты одиночной молекулярной флуоресценции показали, что эта субъединица фактически занимает по крайней мере три положения — закрытое, частично открытое и полностью открытое — что свидетельствует о том, что AP-4 по своей природе динамичен ещё до присоединения к мембранам.
Роль ARF1: рекрутер, а не главный переключатель
Многие родственные адаптерные комплексы переводятся из неактивного в активное состояние при связывании с малыми регуляторными белками, называемыми ARF. Чтобы понять, как это происходит у AP-4, исследователи определили структуры AP-4 в комплексе с ARF1 — малым GTP-связывающим белком, прикрепляющимся к мембранам. Они установили, что ARF1 в основном присоединяется к одной из больших субъединиц AP-4 вблизи её N-конца, подобно другим AP-комплексам. Удивительно, но связывание ARF1 не вызывает драматической перестройки AP-4. Закрытые и открытые формы сосуществуют, а общая архитектура комплекса остаётся во многом неизменной. Биохимические тесты подтвердили, что специфические контактные точки между ARF1 и AP-4 необходимы для привлечения к мембранам, но один только ARF1 не фиксирует AP-4 в едином активном состоянии.
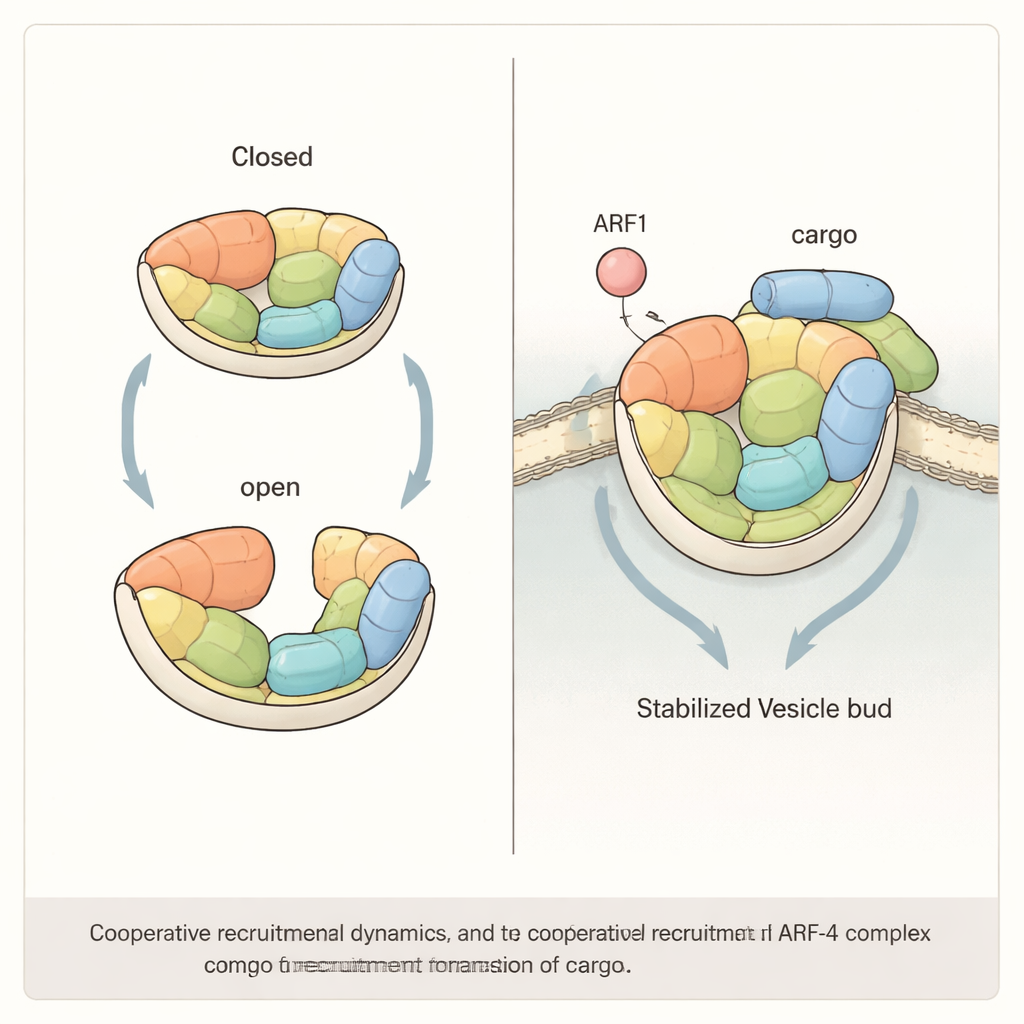
Взаимодействие регулятора и груза
Дальнейшие эксперименты показали, что эффективное привлечение AP-4 к мембранам, вероятно, требует сотрудничества между ARF1 и самими белками-грузами. Воссоздав систему на искусственных шариках и липосомах, авторы обнаружили, что либо ARF1, либо короткий хвостовой пептид груза ATG9A способен притянуть AP-4, но когда оба фактора присутствуют одновременно, они привлекают заметно больше AP-4, чем можно было бы ожидать при суммировании их отдельных эффектов. Когда исследователи внесли мутации, «ужесточающие» структуру AP-4 — уменьшающие его способность переключаться между открытым и закрытым состояниями — этот синергетический эффект исчезал. В человеческих клетках, лишённых ключевой субъединицы AP-4, восстановление только таких «жёстких» мутантных версий комплекса не смогло вернуть нормальную траснпортировку ATG9A из Гольджи, что подчёркивает: гибкость AP-4 — не просто любопытная особенность, а функциональное требование.
Почему гибкость важна для здоровья мозга
В целом работа рисует образ AP-4 как адаптера, меняющего форму и примеряющего несколько конформаций в растворе и на мембранах. Вместо того чтобы быть выключателем «вкл/выкл», ARF1 выступает рекрутером на мембране, который в сотрудничестве с белками-грузами стабилизирует AP-4 в продуктивных конфигурациях, пригодных для образования везикул. Нарушение этого баланса — будь то ослабление связывания с ARF1 или грузом, или «замораживание» AP-4 в одной форме — нарушает вывоз грузов из Гольджи и может способствовать развитию неврологических расстройств. Раскрывая структурную основу динамического поведения AP-4, это исследование даёт основу для понимания связанных с AP-4 заболеваний и намекает на возможные стратегии восстановления нормального транспорта в поражённых нейронах.
Цитирование: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Ключевые слова: транспорт мембран, адаптерный комплекс AP-4, ARF1, образование везикул, неврологическое развитие, расстройство