Clear Sky Science · ru
Фотогенерируемое селективное формирование N–N связи с использованием высвобождения и переноса нитрена
Освещение нового способа соединять атомы азота
Атомы азота находятся в основе многих лекарств, средств защиты растений и современных материалов. Химики умеют эффективно присоединять азот к углероду, но прямое соединение двух атомов азота даётся значительно сложнее. В этом исследовании представлен металло‑свободный метод, активируемый светом, который позволяет контролируемо «стыковать» атомы азота, открывая более простой путь к широкому кругу полезных соединений.
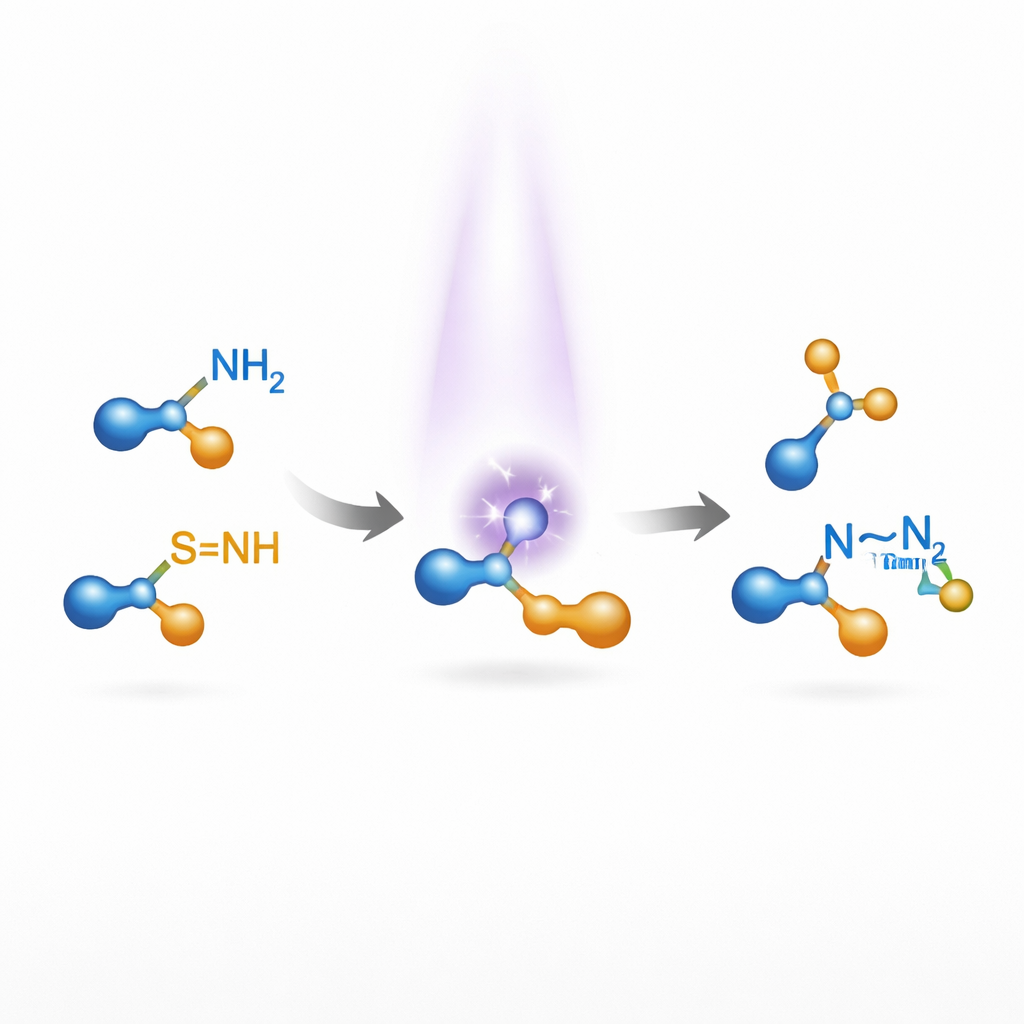
Почему трудно соединить азот с азотом
Многие природные продукты и лекарства содержат пары атомов азота, связанных друг с другом; такая структура может существенно влиять на поведение молекулы в организме или в материалах. Существующие способы собрать такие фрагменты N–N обычно стартуют с заранее подготовленных азот-азотных соединений, например гидразинов или диазосоединений, и затем модифицируются поэтапно. Прямое формирование связи N–N из простых аминов привлекательно, но затруднительно: азот гораздо более электроотрицателен, и два атома азота не образуют естественным образом стабильную неполярную связь. Ранее достигнутые успехи в основном опирались на переходные металлы в качестве катализаторов и часто работали лишь для узких семейств соединений, что ограничивало их применимость в поисковой химии.
Использование света для укрощения реактивного посредника
Авторы обратились к нитренам — чрезвычайно реакционноспособным, кратковременным азотсодержащим видам, которые теоретически могут вклиниться в другие связи. Традиционная нитреновая химия обычно требует металлкатализаторов и подвержена побочным реакциям из‑за высокой энергии нитренов. Исследователи задали себе вопрос, можно ли генерировать нитрены с помощью света бережнее и контролируемее, без металлов, и затем использовать их для связывания простых аминов в продукты, содержащие N–N. Ключевая идея заключалась в использовании сульфилиминов — семейства молекул, легко поддающихся модификации и поглощающих ультрафиолетовое и близкое к видимому излучение. При облучении такие сульфилимины могут распадаться с высвобождением фрагмента нитрена и образованием безвредного серосодержащего побочного продукта.
Широкий металло‑свободный рецепт для пар азота
После систематического тестирования исследователи выделили конкретный сульфилимин, который под светом 365 нм в хлороформе эффективно реагирует со множеством аминов, давая гидразидные продукты — молекулы с вновь образованной N–N связью рядом с карбонильной группой. Они оптимизировали такие параметры, как структура сульфилимина, растворитель и интенсивность света, чтобы предпочесть желаемый продукт обычным побочным продуктам, таким как уреиды. При этих мягких условиях широкий набор аминов — ароматических, алифатических и циклических — успешно сцеплялся. Они также показали, что многие различные сульфилимины с ароматическими и алифатическими ацилирующими группами и сульфонильными заместителями хорошо участвуют в реакции, давая десятки различных продуктов, содержащих N–N. Важно, что метод годится для поздней стадии синтеза — для модификации сложных биологически активных молекул, таких как распространённые противовоспалительные препараты и хиральные строительные блоки, что демонстрирует его практичность для медицины и материаловедения.
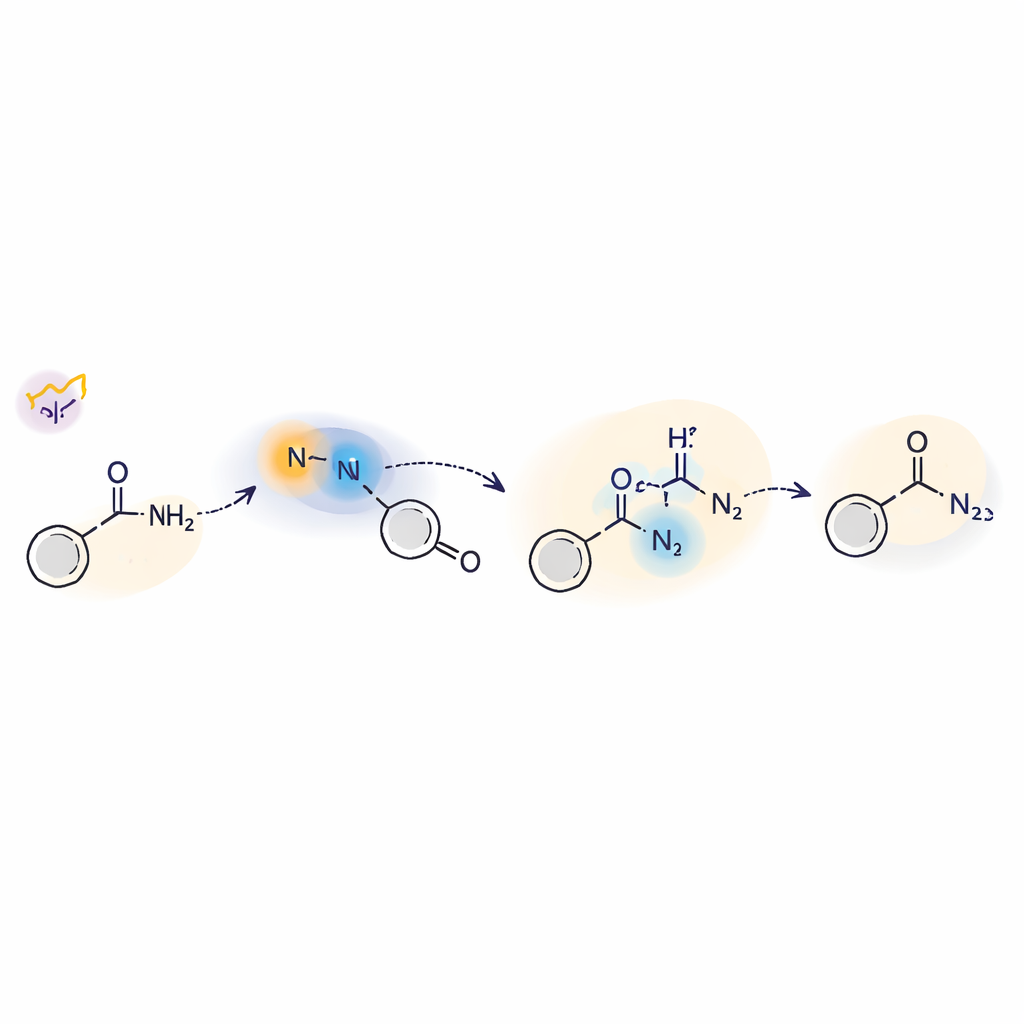
Заглянув внутрь фотодвижущего шага
Чтобы понять, как работает эта светозапускаемая химия, команда сочетала эксперименты и теорию. Они использовали ловушки радикалов, изотопное маркирование и электронный парамагнитный резонанс, чтобы показать появление свободных нитреновых интермедиатов и азот-центрированных радикалов в ходе реакции. Временная лазерная спектроскопия выявила две ключевые формы нитрена: короткоживущий триплет и более долго живущий синглет. Синглет реагирует непосредственно с аминами посредством разновидности нуклеофильной атаки, тогда как триплет может участвовать в переносе атома водорода. Вычисления поддержали механизм, при котором свет возбуждает сульфилимин, его связь S–N разрывается, и образовавшийся нитрен вовлекается в реакцию с амином через синглетный и триплетный пути, прежде чем перейти в финальную структуру гидразида.
Что это означает для будущих молекул
Эта работа показывает, что продуманно разработанные сульфилимины могут выступать в роли «резервуаров нитрена», высвобождая реакционноспособные азотные фрагменты по требованию под действием света, без участия металлов. Используя обе «личности» нитренов — синглетную и триплетную — и поддерживая их концентрацию низкой, метод обеспечивает селективное образование N–N связей для широкого набора строительных блоков. Для неспециалистов вывод таков: у химиков появился более простой, чище и гибкий способ сшивать атомы азота, что может ускорить создание новых лекарств, агрохимикатов и азотсодержащих материалов.
Цитирование: Yu, M., Feng, J., Wang, X. et al. Photo-induced selective N-N bond construction via harnessing nitrene release and transfer. Nat Commun 17, 2084 (2026). https://doi.org/10.1038/s41467-026-68674-z
Ключевые слова: нитреновая химия, фотоиндуцированные реакции, образование N–N связи, сульфилимины, гидразиды