Clear Sky Science · ru
Фотосинтез глицина через C−N‑связывание отходного пластика и нитрата на диатомном катализаторе Pd−B
Превращение мусора в строительные блоки жизни
Пластиковые бутылки, контейнеры для еды и одежда из полиэстера повсюду — как и отходы, которые они оставляют. Одновременно многие заводы сбрасывают сточные воды с высоким содержанием нитратов, что может загрязнять реки и моря. В этом исследовании показано, как можно решить обе проблемы одновременно: используя солнечный свет и специально разработанный катализатор, превратить выброшенный пластик и нитрат в глицин — простую аминокислоту, широко применяемую в пищевой промышленности, медицине и сельском хозяйстве.
Почему глицин и отходы имеют значение
Глицин — один из базовых строительных блоков белков, его производство достигает сотен тысяч тонн в год. Традиционные промышленные методы, особенно классический процесс Штрекера, опираются на токсичные цианидные соединения и жесткие условия реакций, что вызывает опасения по безопасности и воздействию на окружающую среду. Между тем глобальное производство PET — используемого в бутылках, текстиле и упаковке — превышает 100 миллионов тонн в год, и более 80% этого пластика попадает на свалки или в окружающую среду. При химическом разложении PET одним из продуктов является этиленгликоль — малостойкая жидкость низкой стоимости, очистка которой дорога. Авторы задают простой вопрос: можно ли вместо того, чтобы считать этиленгликоль и нитраты отходами, использовать их в качестве сырья для получения ценного глицина, применяя только солнечный свет?
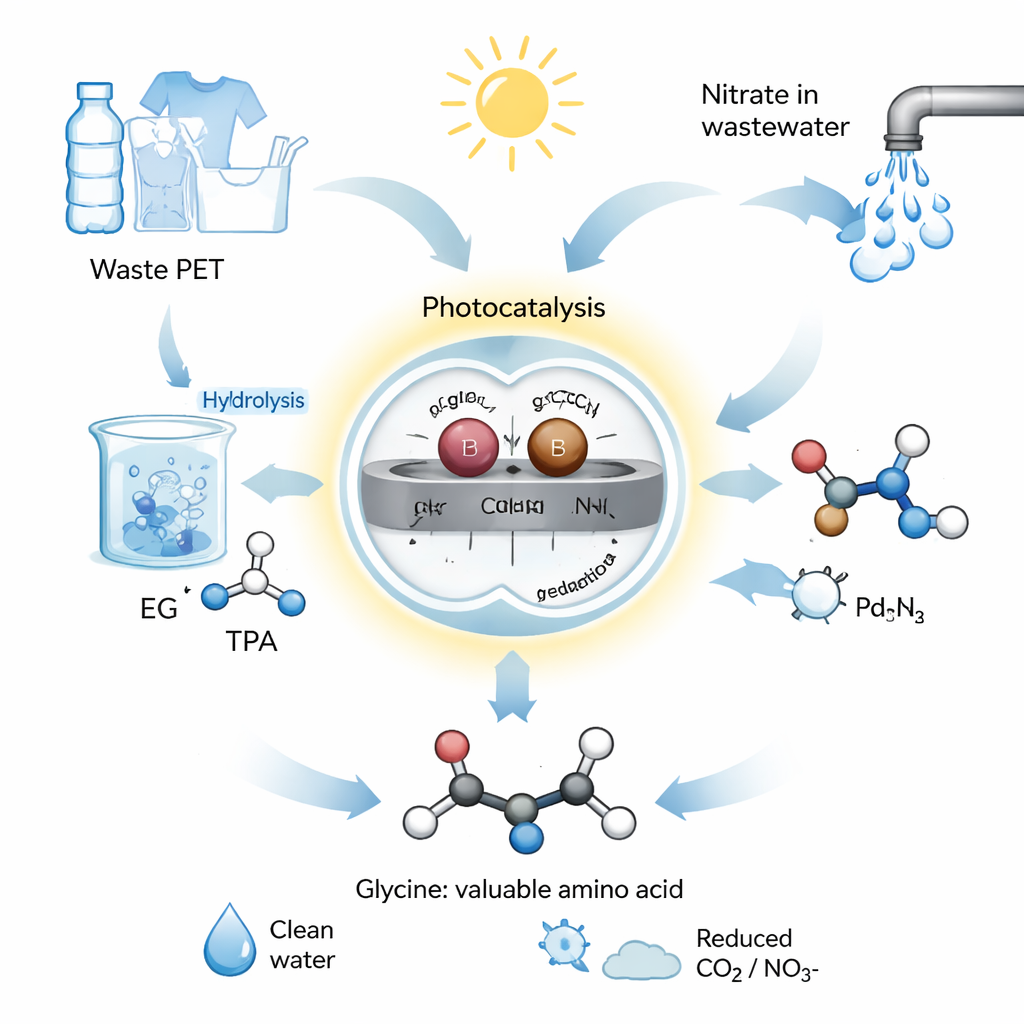
Химическая короткая дорога на солнечной энергии
Команда разработала фотокаталитическую систему, то есть использующую свет для приведения химических реакций в действие. Они создали катализатор на основе графитного нитрида углерода, полупроводника, и закрепили на его поверхности пары отдельных атомов палладия (Pd) и бора (B). Эти парные атомы действуют как микроскопическая команда из двух агентов, каждый из которых отвечает за свою половину химии. В их процессе отходы PET сначала гидролизуют — расщепляют в щелочной воде — чтобы выделить этиленгликоль. Этот этиленгликоль и нитрат из сточных вод затем помещают в воду с катализатором Pd–B и подвергают воздействию имитированного или естественного солнечного света. При таких мягких условиях система превращает смесь в глицин с высоким выходом и селективностью свыше 92%, то есть образуется очень мало нежелательных побочных продуктов.
Как работает атомное дуо
Успех катализатора зависит от того, как он управляет короткоживущими реакционными межпродуктами. Борные центры на поверхности «богаты дырками», то есть охотно принимают положительный заряд при поглощении света материалом. На этих B‑центрах этиленгликоль мягко окисляется — лишается водорода — с образованием гликольальдегида, нестабильной молекулы, которая обычно склонна к дальнейшему переокислению в кислоты или даже в диоксид углерода. Центры палладия, напротив, «богаты электронами». Они используют светогенерируемые электроны для поэтапного восстановления нитрата до аммония или аммиака. Ключевой стадией является углеродно‑азотное связывание между гликольальдегидом и этими азотсодержащими промежуточными продуктами с образованием этаноламина, который затем дополнительно окисляется, снова в основном на B‑центрах, с получением глицина. Благодаря стабилизации гликольальдегида ровно на столько, чтобы он вступил в реакцию, и пространственному разделению электронов и дырок пара Pd–B направляет химию в сторону желаемой аминокислоты, снижая образование побочных продуктов.
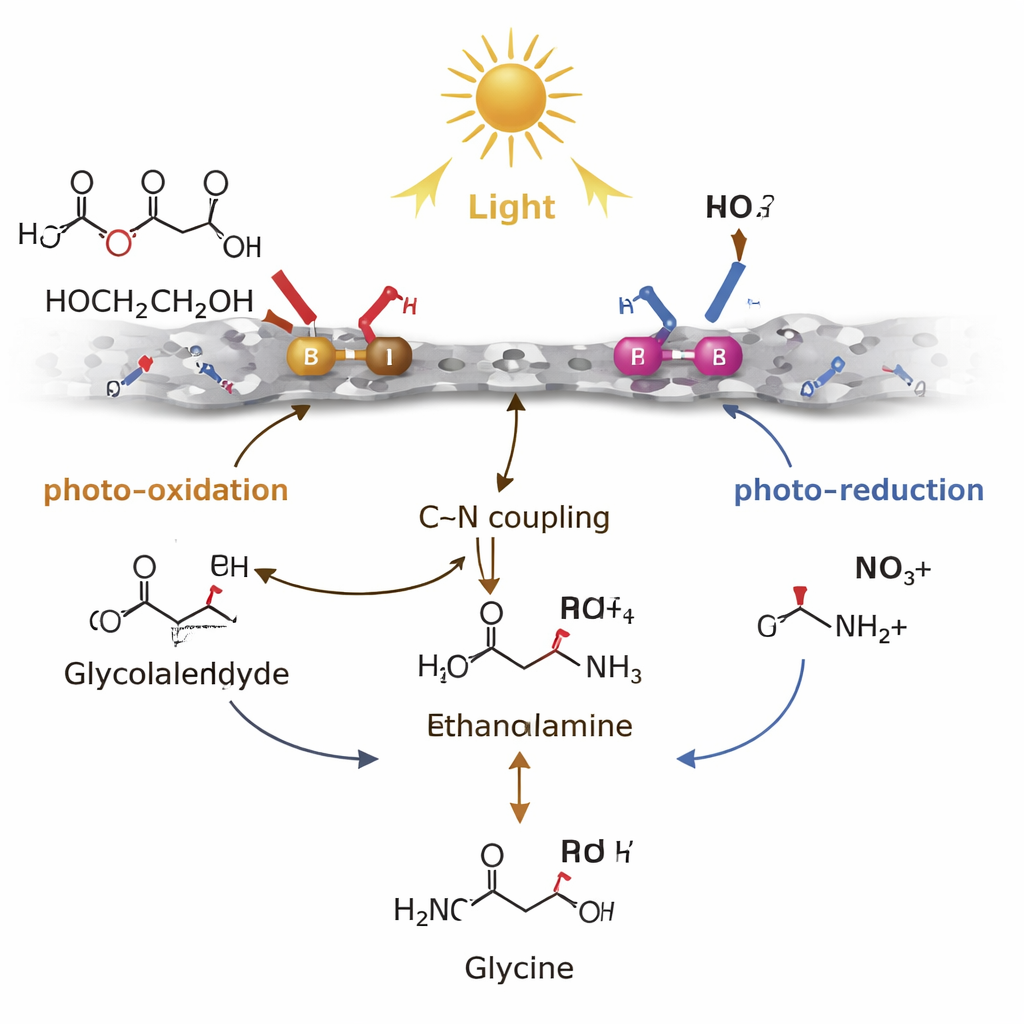
От лабораторного механизма к реальным отходам
Исследователи подтвердили каждую часть этого пути набором методов, отслеживая радикалы, промежуточные продукты и азотсодержащие продукты в реальном времени. Они сравнили разные материалы и металлы катализаторов и обнаружили, что опоры g‑C3N4 с изолированными парами Pd–B показали наилучшую работу, достигая скоростей образования глицина 2,9 миллимоль на грамм катализатора в час. Катализатор сохранял активность при многократных циклах, и его структура оставалась стабильной. Важно, что команда вышла за рамки чисто лабораторных реагентов. Они продемонстрировали получение граммового количества глицина, начиная с реального постпотребительского PET — порошка, бутылок, одежды, пакетов и прочего — в сочетании с нитратными растворами и даже сложными сточными водами. Они также показали, что родственные спирты из биомассы, такие как глицерин, могут служить альтернативными источниками углерода, расширяя практическую применимость подхода.
Выгодный путь для отходов и климата
Чтобы приблизить концепцию к практике, авторы испытали процесс под естественным солнечным светом, сфокусированным простой линзой Френеля. Система стабильно производила глицин с высокой селективностью, а моделирование указывает, что масштабирование может предотвратить значительные выбросы диоксида углерода и не допустить сброса нитратов в окружающую среду. Проще говоря, эта работа описывает способ превращения гор использованного пластика и загрязненной воды в полезную аминокислоту, используя только свет и точно настроенный катализатор. Хотя перед промышленным внедрением остаются инженерные задачи, исследование демонстрирует, как дизайн катализатора на атомном уровне может объединить два крупных потока отходов в один ценный химический продукт.
Цитирование: Ya, Z., Li, M., Fu, D. et al. Glycine photosynthesis via C−N coupling of waste plastic and nitrate over diatomic Pd−B catalyst. Nat Commun 17, 1887 (2026). https://doi.org/10.1038/s41467-026-68666-z
Ключевые слова: глицин, переработка пластика, фотокатализ, нитратные сточные воды, одноатомные катализаторы