Clear Sky Science · ru
Регуляция сборки адаптера AP1 би-руким шапероном MEA1
Почему этот скрытый помощник в клетке важен
В каждой человеческой клетке тысячи крошечных посылок доставляют белки туда, где они нужны, или в «центр утилизации» для разрушения. Этот трафик поддерживает клетки в рабочем состоянии и контролирует нашу иммунную систему. В обзоре, который здесь суммируется, раскрыт ранее малоизвестный белок MEA1, оказавшийся необходимым для сборки одного из ключевых сортировочных механизмов, загружающих эти посылки. Понимание работы MEA1 помогает объяснить, как клетки управляют важными грузами, в том числе молекулами, которые включают и выключают противовирусные иммунные ответы.
Контроль трафика в центральном почтовом отделении клетки
Большая часть доставки в клетке проходит через органеллу, называемую аппаратом Гольджи — стопку плоских мешочков, действующих как центральное почтовое отделение. Из Гольджи грузы можно отправлять на поверхность клетки для использования или направлять во внутренние компартменты для уничтожения. В центре этого маршрута находится белковый комплекс AP1. AP1 распознаёт метки на транспортируемых белках, способствует изгибу мембраны и привлекает внешнюю оболочку из клатрина для образования мелких транспортных везикул. Без правильно собранного AP1 критически важные грузы накапливаются не в тех местах, и нормальные сигнальные пути, включая связанные с иммунитетом, могут нарушаться. 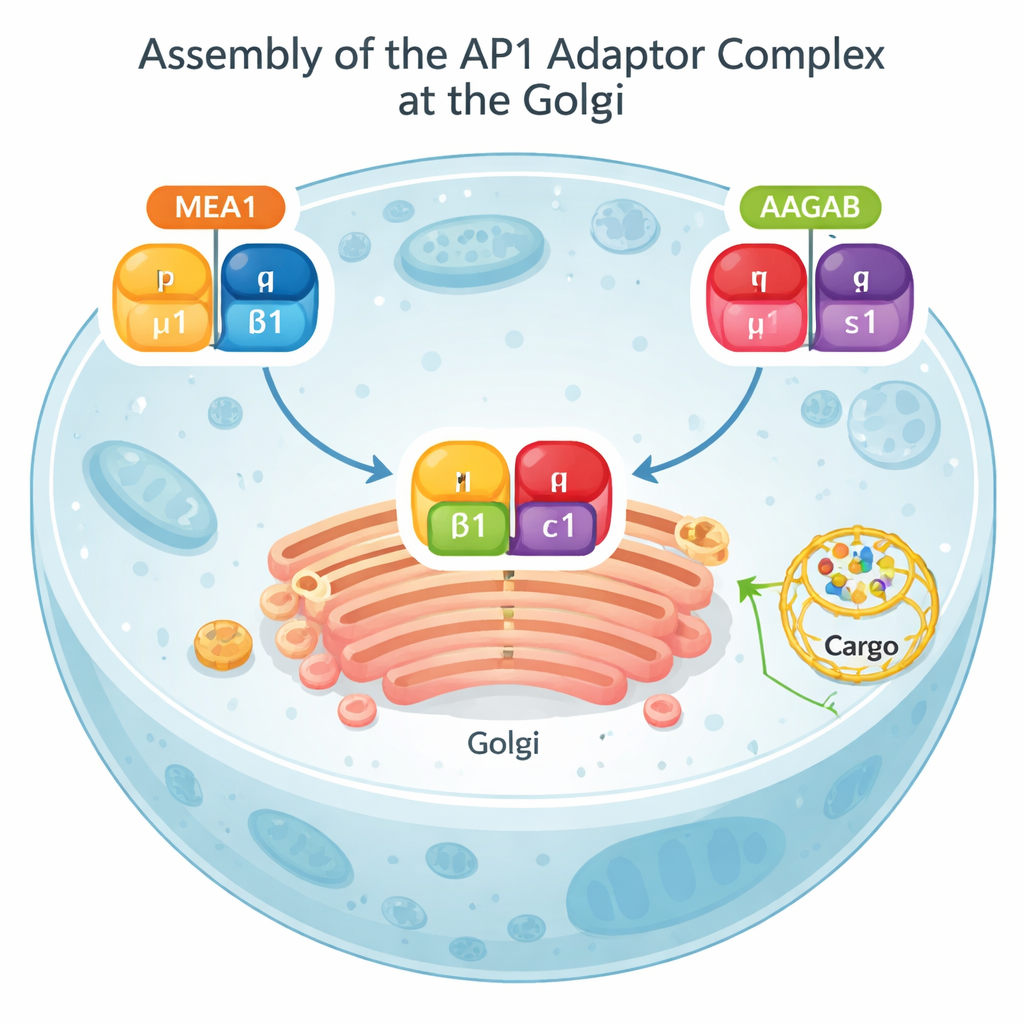
Поиск отсутствующего сборщика
Авторы поставили цель выявить белки, физически ассоциирующие с AP1 и могущие помогать его сборке. Они проанализировали крупную базу данных взаимодействий белков, отфильтровали кандидатов, маловероятных для работы с AP1, а затем использовали инструмент искусственного интеллекта AlphaFold, чтобы предсказать, как оставшиеся белки могут контактировать с отдельными частями AP1. Этот поиск выделил MEA1 — небольшой ранее нехарактеризованный белок, присутствующий во многих тканях. Последующие эксперименты в человеческих клетках подтвердили, что MEA1 связывается с двумя специфическими субъединицами AP1, известными как μ1 и β1, как в изолированном виде, так и в их естественных, немодифицированных формах.
MEA1 сохраняет целостность AP1 и движение грузов в клетке
Чтобы выяснить функцию MEA1, исследователи удалили ген MEA1 в линиях человеческих клеток. При отсутствии MEA1 все четыре компонента AP1 значительно уменьшились, и характерные точки AP1 рядом с аппаратом Гольджи почти исчезли. Это имело очевидные функциональные последствия. Один из грузов AP1, рецептор фолата FOLR1, накапливался на поверхности клетки вместо направления внутрь — признак дефектной сортировки AP1. Другой груз, сигнализирующий иммунный белок STING, больше не упаковывался эффективно в везикулы, направляющиеся в лизосомы, клеточные «пункты утилизации». В результате активированный STING и его партнёр-киназа TBK1 удерживались на высоких уровнях, что указывает на то, что «выключатель» этого антивирусного пути не работал должным образом. Повторное введение MEA1 восстановило уровни AP1 и исправило эти дефекты транспортировки.
Двурукий шаперон и процесс сборки через столкновение
Биохимические тесты и модели AlphaFold показали, что MEA1 ведёт себя как «двурукий» шаперон сборки: его передняя часть захватывает субъединицу μ1, а задняя — β1. По отдельности μ1 и β1 нестабильны и склонны к агрегации или разрушению; в связке с MEA1 они становятся растворимыми и готовы к сборке. Другой известный шаперон, AAGAB, выполняет аналогичную работу для оставшихся двух субъединиц AP1, γ и σ1. Когда комплексы MEA1–μ1–β1 и AAGAB–γ–σ1 встречаются, их субъединицы объединяются в полноценный четырёхчастный адаптер AP1. В этот момент оба шаперона отпускают свои субъединицы и возвращаются в цитозоль, а вновь сформированный AP1 перемещается к мембранам для выполнения сортировочной функции. Этот механизм «столкновения двух шаперонов» демонстрирует, что сборка AP1 тщательно координирована, а не предоставлена случайным столкновениям.
Общие выводы о клеточном контроле качества
Помимо AP1, исследование указывает на более общую стратегию, которую клетки могут использовать для сборки многих крупных белковых машин. MEA1 также слабо способствует работе другого адаптерного комплекса, AP2, и вместе с AAGAB и третьим шапероном CCDC32 он иллюстрирует более широкий путь, который авторы называют «Шаперон-ассистированной сборкой адаптерных белков». В этой схеме специализированные шапероны стабилизируют хрупкие субъединицы, сводят нужные пары вместе и временно блокируют сайты связывания грузов до тех пор, пока комплекс полностью не сформирован и безопасен для использования. 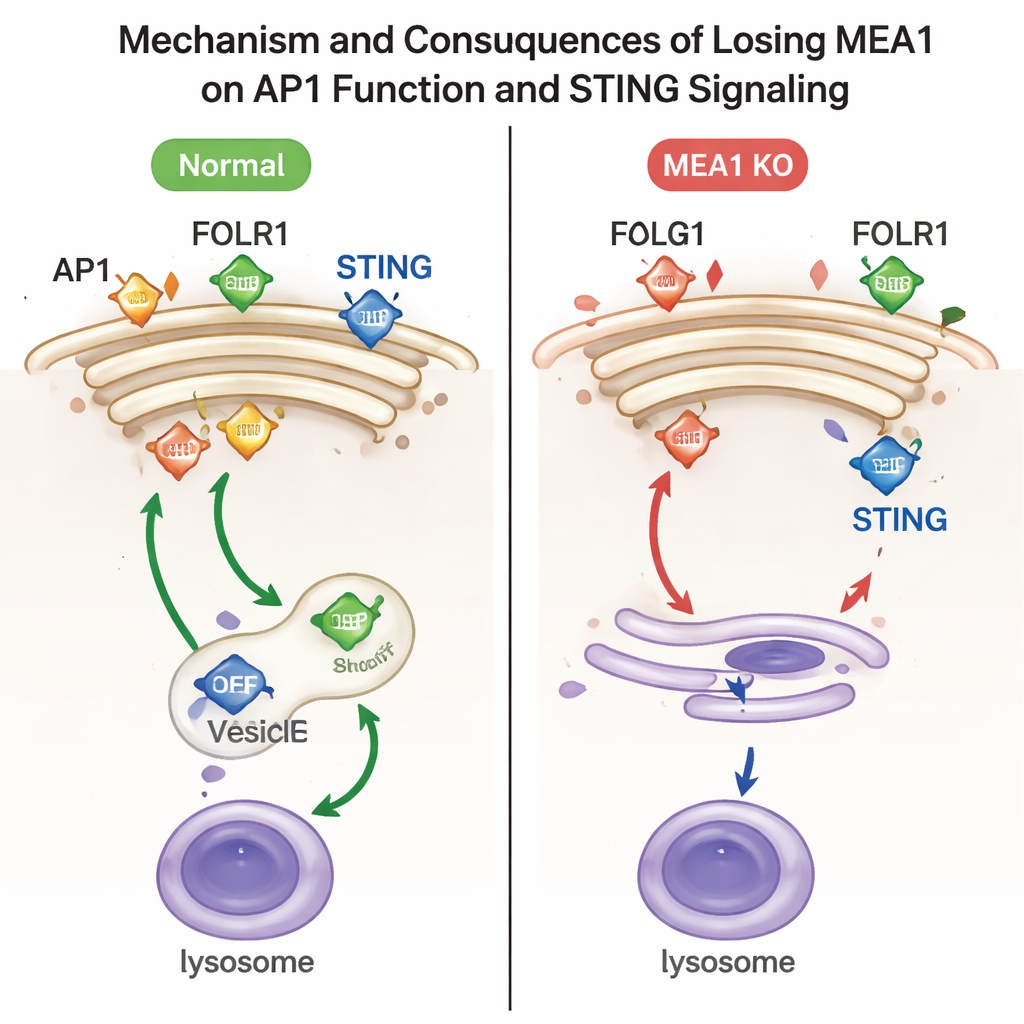
Что это значит для здоровья и болезней
Для неспециалистов главный вывод таков: MEA1 — важный невидимый работник, который помогает собирать AP1, ключевую сортировочную машину в наших клетках. При отсутствии MEA1 AP1 разваливается, возникают транспортные заторы, и важные регуляторы, такие как STING, неправильно отключаются. Это новое понимание может в перспективе помочь объяснить некоторые иммунные расстройства или другие заболевания, связанные с нарушением транспорта белков, и раскрывает общий принцип того, как клетки безопасно собирают сложные молекулярные машины из нестабильных частей.
Цитирование: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Ключевые слова: транспорт белков, адаптерный белок AP1, молекулярные шапероны, STING-сигнализация, клеточная биология