Clear Sky Science · ru
Молекулярное распознавание тиреоглобулина сортиллином
Как клетки щитовидной железы решают, когда выпустить гормон
Тиреоидные гормоны задают наш метаболический «термостат», влияя на всё — от частоты сердечных сокращений до температуры тела. Эти гормоны синтезируются и хранятся внутри гигантского белка, называемого тиреоглобулином. В этом исследовании показано, как другой белок, сортиллин, помогает клеткам щитовидной железы выбирать, какую форму тиреоглобулина вернуть внутрь клетки для распада и последующего выделения гормона в кровь — решение, которое в конечном счёте влияет на количество доступного для организма тиреоидного гормона.
Запасной белок, ожидающий обработки
Тиреоглобулин — массивный белок в форме буквы Y, который продуцируется и секретируется клетками щитовидной железы в желеобразную среду, называемую коллоидом. Там он служит и сырьём, и хранилищем для тиреоидного гормона: определённые строительные блоки (аминокислоты) внутри тиреоглобулина химически йодируются и превращаются в гормоны, оставаясь встроенными в большой белок. Чтобы освободить эти гормоны, тиреоглобулин должен быть повторно захвачен клеткой, расщеплён в перерабатывающих компартментах — лизосомах, — а образовавшиеся молекулы гормонов экспортированы в кровь.
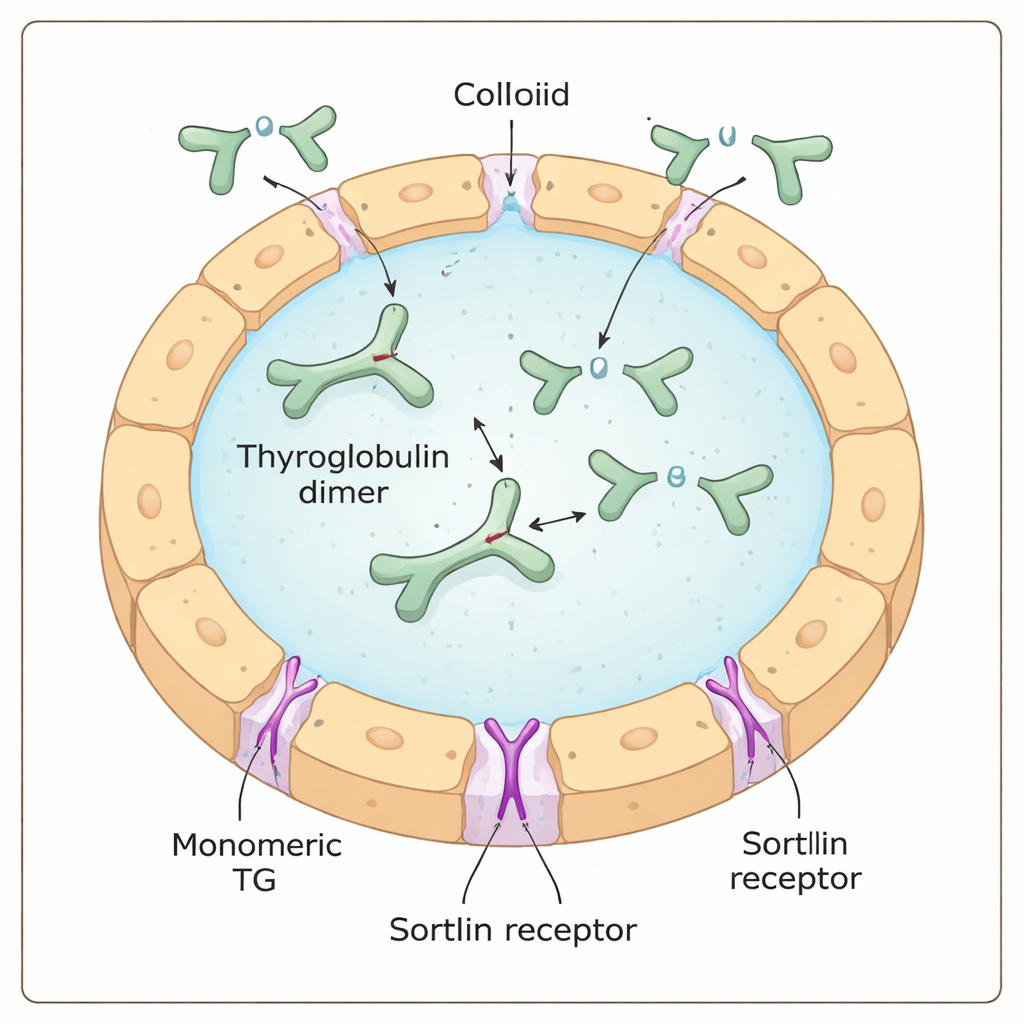
Клеточный шлагбаум с скрытым предпочтением
Рецептор сортиллин предлагали в качестве одного из «шлагбаумов», которые связывают тиреоглобулин на поверхности клетки и направляют его внутрь. Ранее считалось, что сортиллин предпочитает сильно йодированный тиреоглобулин, что намекало на способность рецептора «чувствовать» содержание йода напрямую. Однако, сочетая биохимические тесты, измерения массы отдельных молекул и исследования поглощения в клетках, авторы показали, что сортиллин значительно предпочитает одноцепочечную, мономерную форму тиреоглобулина его более распространённой парной, димерной форме. Чем больше мономера в образце, тем эффективнее он образовывал комплексы с сортиллином и захватывался клетками щитовидной железы, независимо от степени йодирования.
Приближение к точке контакта
Чтобы понять это предпочтение на атомном уровне, команда обратилась к высокоразрешающей криоэлектронной микроскопии и масс-спектрометрии с кросс-ссылками. Эти методы показали, что сортиллин распознаёт короткий, гибкий хвост на С-конце (одном конце) мономерного тиреоглобулина. Этот хвост проникает в центральную полость сортиллина, напоминающую десятилопастный пропеллер, и фиксируется в двух небольших «горячих точках» внутри. Любопытно, что в димерной форме часть области вокруг этого хвоста оказывается скрытой и недоступной для сортиллина, что объясняет плохую совместимость с димером. Данные указывают на то, что внеклеточное подрезание или ослабление тиреоглобулина — через естественное протеолизное разрушение — способствует превращению димеров в мономеры, которые сортиллин может захватить.
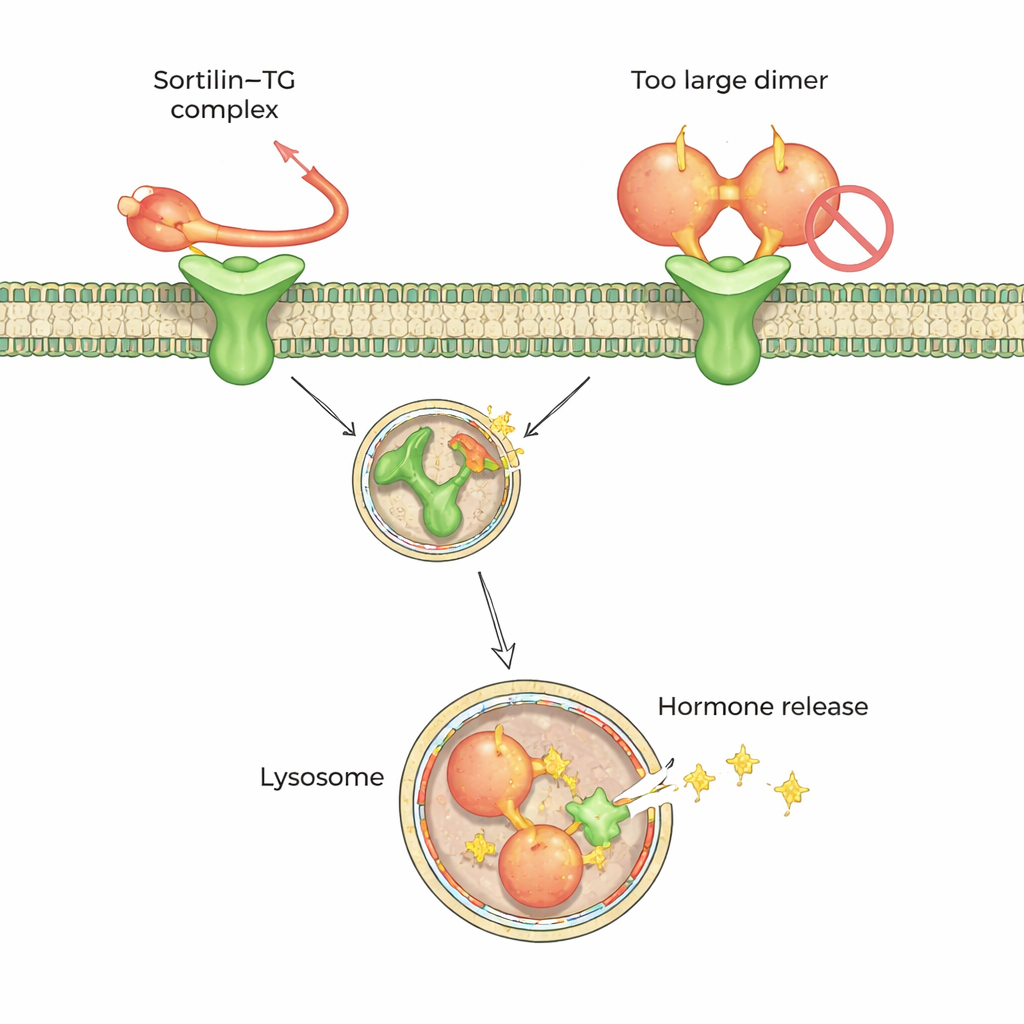
Общий код швартовки для множества грузовых белков
Сортиллин — не только белок щитовидной железы; он участвует в транспорте многих различных молекул по организму, включая факторы, связанные с сердечными и мозговыми заболеваниями. Сочетая свою структурную работу с продвинутыми инструментами предсказания структуры, такими как AlphaFold и AlphaPulldown, исследователи сравнили, как десятки известных партнёров сортиллина могут связываться с его пропеллерной полостью. Они обнаружили повторяющийся паттерн: многие грузы представляют собой неструктурированный пептидный сегмент примерно из двадцати аминокислот, который помещается в тот же карман, что и хвост тиреоглобулина, иногда направляясь в ту же сторону, что и известный мозговой пептид нейротензин, а иногда в противоположную. Несмотря на обратную ориентацию, эти пептиды имеют сходные черты — на одном конце кислородсодержащая или отрицательно заряженная группа, на другом — объёмный ароматический остаток, а между ними гибкий, часто богатый пролином отрезок.
Почему йод важен меньше, чем форма
Поскольку ключевой контакт между сортиллином и тиреоглобулином — это гибкий хвост, авторы проверили, изменится ли связывание, если украшать тирозин в хвосте дополнительным йодом, формирующим гормон. Изменений не оказалось: синтетический пептид с полностью сформированным тиреоидным гормоном вёл себя почти так же, как немодифицированный вариант. Моделирование показало, что йодированное кольцо торчит в раствор и не создаёт новых тесных контактов. В сочетании с экспериментами по поглощению это поддерживает пересмотренную картину: сортиллин не «считает» атомы йода на тиреоглобулине. Вместо этого он распознаёт, расслаблена ли или частично протеолизирована ли молекула так, что её мономерная форма и хвост оказываются доступными.
Что это значит для здоровья щитовидной железы
Для неспециалиста основная мысль такова: выпуск тиреоидного гормона контролируется не столько встроенным датчиком йода, сколько механической проверкой формы и гибкости белка. Сортиллин действует как сканер на поверхности клетки, ищущий молекулы тиреоглобулина, ослабленные или подрезанные до мономеров, затем втягивающий их внутрь для окончательной высвобождения гормона и переработки йода. Эта работа проясняет ключевой этап в биологии тиреоидных гормонов и даёт основание полагать, что лекарственные средства, нацеленные на блокирование сортиллина — которые сейчас исследуют для других заболеваний — могут непреднамеренно изменить обращение с тиреоидными гормонами, нарушив этот этап распознавания.
Цитирование: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Ключевые слова: тиреоидный гормон, тиреоглобулин, сортиллин, транспорт белков, эндоцитоз