Clear Sky Science · ru
Мостовая спираль Cas12a — аллостерический регулятор формирования R-петли и активации RuvC
Почему это важно для редактирования генов
Многие мощные инструменты редактирования генов, в том числе те, что используются в новых терапиях и быстрых диагностических тестах, опираются на белки CRISPR, разрезающие ДНК в выбранных участках. Но если эти молекулярные «ножницы» срежут не там, где нужно, это может вызвать вредные побочные эффекты. В этой работе детально изучена крошечная подвижная часть в редакторе Cas12a, называемая мостовой спиралью, и показано, как ее конформационные изменения действуют как внутренний предохранитель, связывающий распознавание цели с резкой ДНК. Понимание этого переключателя дает карту для проектирования CRISPR-инструментов, которые будут одновременно точными и безопасными для медицины и биотехнологий.
Молекулярный зажим с подвижными элементами
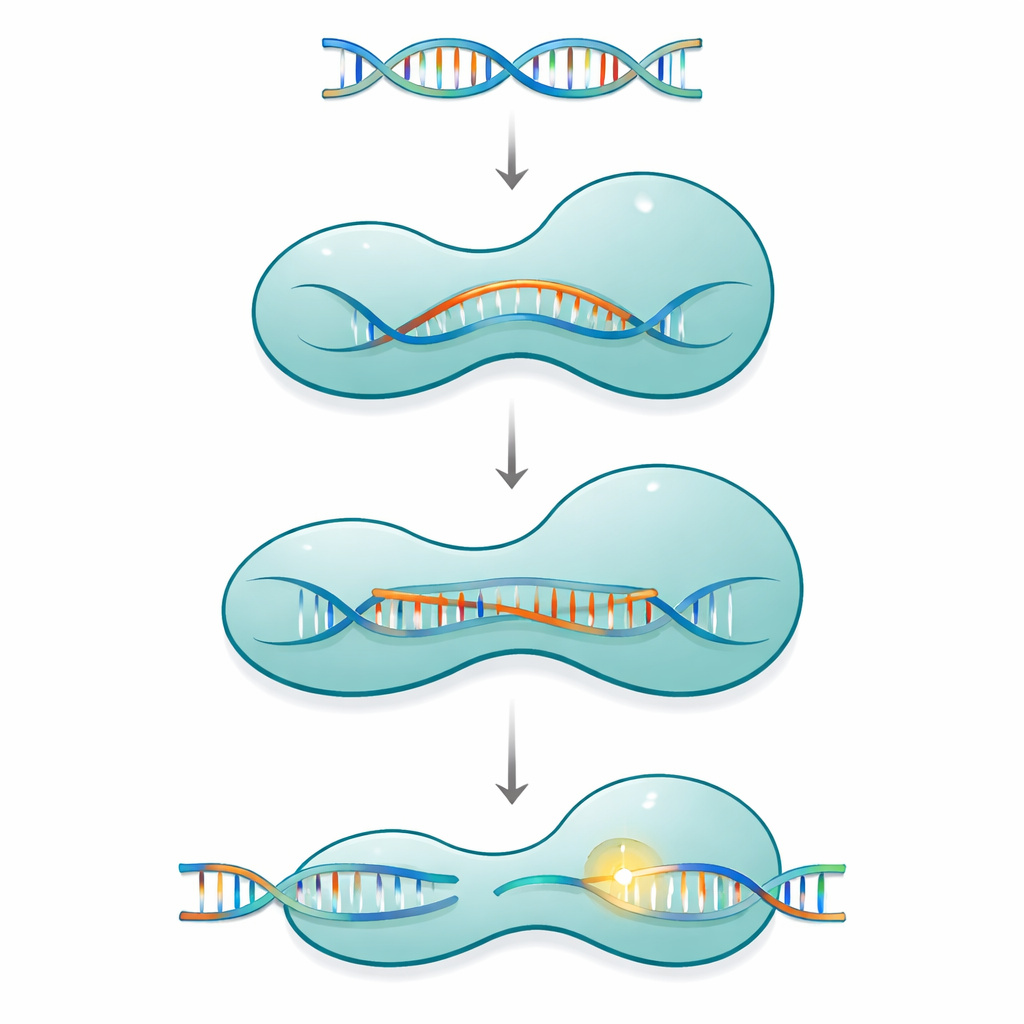
Cas12a принадлежит к семейству одно-белковых систем CRISPR, которые используют короткую направляющую РНК для поиска и разрезания совпадающей ДНК в вирусах или в геноме клетки. Белок имеет форму двухрукого зажима: сторона распознавания проверяет последовательность, а сторона резки содержит химический аппарат. Эти две половины соединены тонким положительно заряженным сегментом, называемым мостовой спиралью. По мере связывания Cas12a с направляющей РНК, а затем с ДНК-мишенью белок не ведет себя как жесткий инструмент. Вместо этого он проходит серию больших и малых конформационных изменений, постепенно закрываясь вокруг растущей гибридной структуры РНК–ДНК, известной как R-петля, и полностью активирует сайт разрезания только тогда, когда образовалась достаточно длинная последовательность правильного спаривания оснований.
Изучение встроенного предохранителя
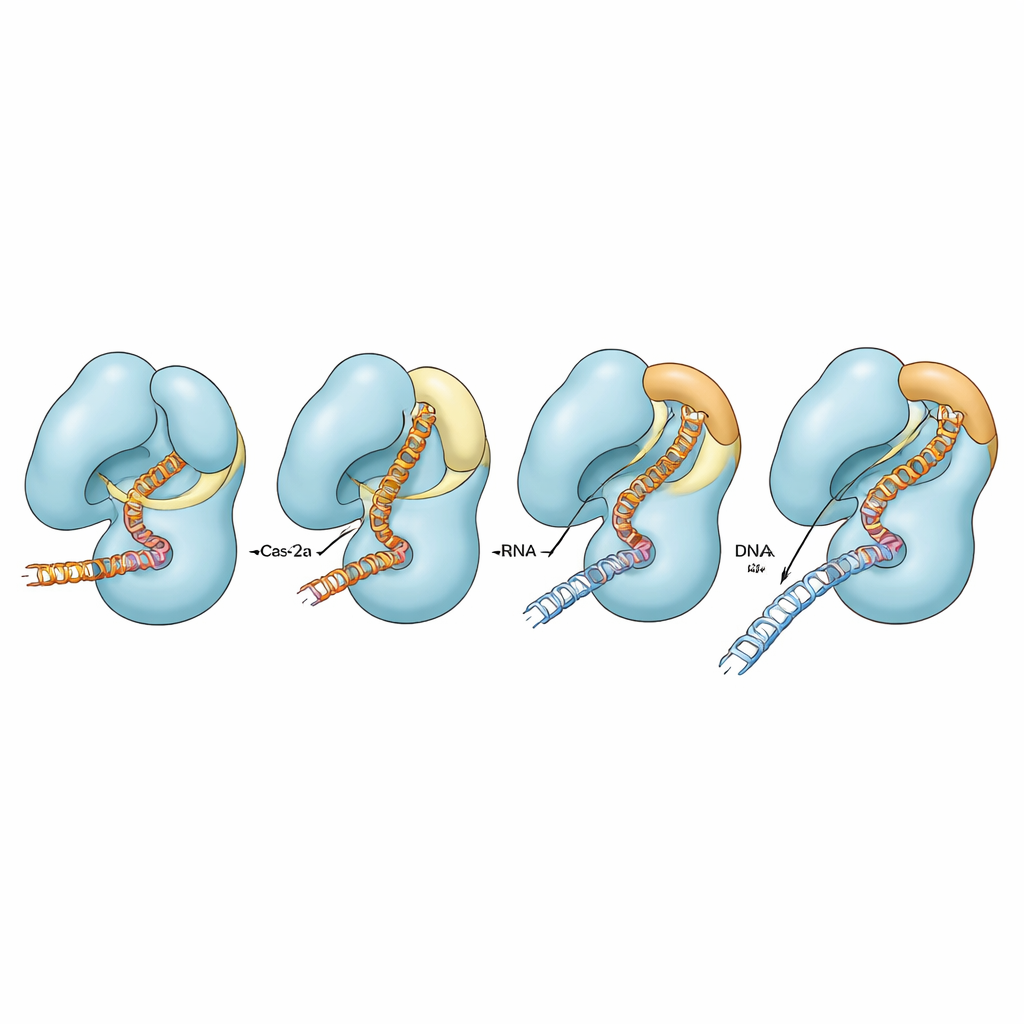
Исследователи сосредоточились на Cas12a из бактерии Francisella novicida и ранее созданной версии, в которой два аминокислотных остатка в мостовой спирали были заменены на пролины — изменение, известное тем, что оно укорачивает или ломает спирали. Этот вариант, названный FnoCas12aKD2P, разрезает ДНК более избирательно, но медленнее, чем природный белок. С помощью крио-электронной микроскопии они зафиксировали пять различных структурных снимков этого варианта, связанного с направляющей РНК и фрагментом целевой ДНК. Эти снимки показывают белок на разных стадиях его пути активации — от раннего распознавания ДНК до более поздних состояний, в которых часть гибрида РНК–ДНК сформирована, но полная готовность к разрезанию еще не достигнута.
Как конформационные изменения приводят к точной резке
Сравнение варианта с ранее определёнными структурами нормального Cas12a выявило четкий паттерн. В природном белке сегмент мостовой спирали переходит из свободной петли в более длинную, прямую спираль и изгибается в сторону растущего гибрида РНК–ДНК, приближаясь к нему. Одновременно соседняя спираль в каталитическом домене ослабляется, а небольшой участок, называемый «крышкой», которая в норме блокирует активный центр, превращается из петли в спираль и откидывается. В совокупности эти согласованные движения открывают карман, позволяющий входить одной цепи ДНК и быть разрезанной. В варианте с пролинами мостовая спираль не может полностью совершить переход «петля→спираль» или правильно согнуться. В результате гибрид РНК–ДНК остается искажённым и дальше от активного центра, крышка остается в закрытом петлеобразном состоянии, и комплекс редко достигает полностью прекаталитической конформации. Этот механический узкий участок замедляет разрезание по целевому участку и затрудняет прохождение несовпадающей ДНК через внутренние контрольные точки.
Тонкая настройка точности через изменение контактов
Чтобы проверить, как разные контакты вокруг крышки и мостовой спирали влияют на активность, авторы модифицировали конкретные заряженные остатки, связывающие эти регионы. В нормальном Cas12a разрушение этих контактов оказывало лишь умеренное влияние на разрезание идеально совпадающей ДНК, хотя при некоторых условиях это влияло на эффективность разрезания второй цепи ДНК при наличии несовпадений. В ослабленном фоне мостовой спирали те же замены значительно уменьшали или почти полностью устраняли разрезание обеих цепей, особенно когда направляющая РНК и ДНК не совпадали полностью. Компьютерные моделирования подтверждали эти выводы, показывая, что только когда мостовая спираль может полностью принять свою спиральную форму, мост, соседняя спираль, крышка и нуклеиновые кислоты двигаются в скоординированном режиме. Когда спираль нарушена, эти движения частично или полностью рассинхронизируются, и ферменту становится трудно завершить свой каталитический цикл.
Руководство по проектированию CRISPR-инструментов следующего поколения
В целом работа выявляет мостовую спираль как внутренний рычаг контроля, связывающий длину и качество гибрида РНК–ДНК с открытием кармана для резки в Cas12a. Заставляя белок проходить определённую последовательность конформационных изменений перед разрезанием ДНК, этот механизм естественным образом обеспечивает распознавание несовпадений. Результаты помогают объяснить, почему целевые изменения в этой небольшой области могут приводить к вариантам Cas12a с уменьшенным количеством побочных разрезов и сниженой «коллатеральной» активностью по ДНК — свойствами, желательными для более безопасного редактирования генома и диагностики. В более широком смысле исследование подчёркивает, как тонкие сдвиги в коротких спиралях могут координировать дальнодействующую связь в больших молекулярных машинах, предлагая общие принципы для инженерии нуклеиновых фрагментов-обрабатывающих ферментов высокой точности.
Цитирование: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Ключевые слова: CRISPR-Cas12a, точность редактирования генов, мостовая спираль, формирование R-петли, аллостерическая регуляция