Clear Sky Science · ru
NeoPrecis: повышение точности прогнозов ответа на иммунотерапию за счёт интеграции квалифицированных нейоантигенных профилей с учётом клононности
Почему одни раки реагируют на иммунотерапию, а другие — нет
Иммунотерапия изменила подход к лечению рака, но многие пациенты по‑прежнему не получают от неё выгоды, а у некоторых развиваются серьёзные побочные эффекты. Важный вопрос в том, почему одни опухоли замечаются и уничтожаются иммунной системой, а другие ускользают. В этом исследовании представлена NeoPrecis — вычислительный метод, который внимательнее рассматривает «флаги», которые опухоли показывают иммунной системе — так называемые неоантигены — и использует эту информацию для более точного прогнозирования, какие пациенты с высокой вероятностью ответят на современные иммунотерапевтические препараты.
Новые флаги на раковых клетках
Раковые клетки накапливают мутации в ДНК, которые могут менять белки, которые они синтезируют. Небольшие фрагменты этих изменённых белков, называемые неоантигенами, могут выводиться на поверхность клетки и распознаваться Т‑клетками как чужеродные. В течение многих лет врачи и исследователи опирались на грубые метрики, такие как нагрузка мутаций в опухоли — общее число мутаций — чтобы оценить вероятность ответа на ингибиторы контрольных точек. Но это инструмент грубой силы: не каждая мутация создаёт заметную или привлекательную мишень для Т‑клеток, к тому же опухоли часто представляют собой мозаику разных клеточных субпопуляций. NeoPrecis разработана, чтобы выйти за рамки простого подсчёта мутаций и вместо этого оценивать, сколько из них на самом деле являются перспективными мишенями по всему объёму опухоли.
Одновременный анализ трёх ключевых компонентов
NeoPrecis оценивает каждую мутацию по трём параметрам: насколько она распространена в опухоли, будет ли она представлена на поверхности клетки и насколько вероятно, что её заметят Т‑клетки. Распространённость оценивают по данным секвенирования ДНК и РНК, которые показывают, насколько часто встречается мутация и насколько сильно она экспрессируется. Представление моделируется через связывание с молекулами MHC класса I и II, которые работают как билборды, демонстрирующие фрагменты белков Т‑клеткам. Самая новая часть — компонент распознавания Т‑клеток NeoPrecis‑Immuno. Эта модель обучается на больших базах данных известных взаимодействий Т‑клеток с пептидами, чтобы оценить, насколько мутировавший фрагмент отличается от нормального аналога в аспекте, важном для распознавания Т‑клетками, одновременно учитывая конкретные варианты MHC у каждого человека.
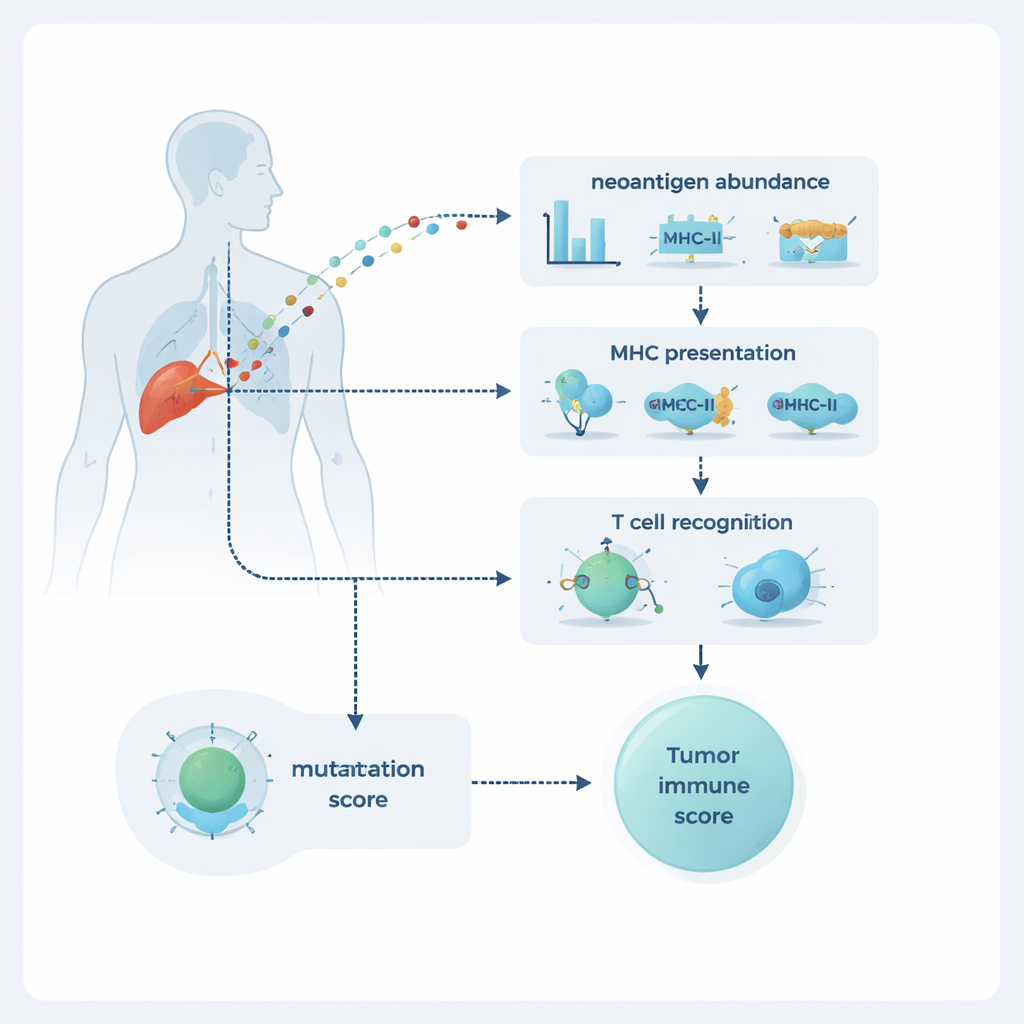
Обучая компьютер тому, что «видят» Т‑клетки
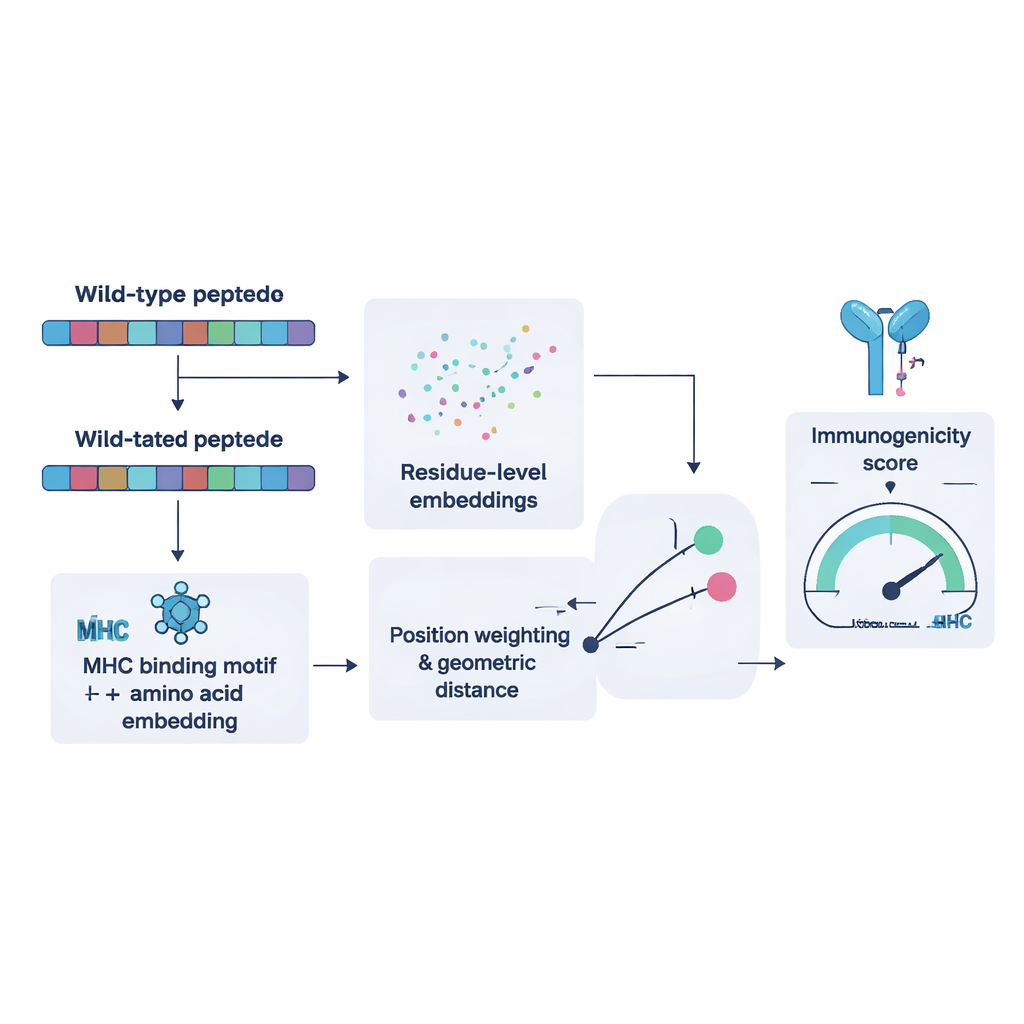
Чтобы обучить NeoPrecis‑Immuno, исследователи собрали тысячи примеров, где одна и та же Т‑клетка распознаёт несколько схожих пептидов и другие, которые она не распознаёт. Они использовали эти примеры, чтобы научить модель тому, что мутантные фрагменты, сильно похожие на нормальные, с меньшей вероятностью вызовут иммунный ответ, поскольку такие самоподобные мишени обычно отбрасываются в процессе развития Т‑клеток. Модель представляет каждый пептид как точку в математическом пространстве, сформированном как последовательностью аминокислот, так и предпочтениями связывания конкретных молекул MHC данного человека. Затем она измеряет, насколько далеко мутантный пептид отстоит от оригинала. Бóльшие расстояния, информированные мотивами последовательности, соответствуют более высокой вероятности иммуногенности. При проверке на независимых наборах данных по раку NeoPrecis‑Immuno сопоставимо конкурировала с существующими инструментами или превосходила их, особенно при работе с MHC класса II, которые представляют антигены вспомогательным Т‑клеткам, поддерживающим и усиливающим противоопухолевые ответы.
От отдельных мутаций к картине всей опухоли
Отдельные мутации — лишь часть истории; важно также, как они распределены в опухоли. Некоторые мутации «клональные», встречаются почти в каждой раковой клетке, в то время как другие «субклональные», присутствуют только в отдельных очагах. NeoPrecis строит «ландшафт неоантигенов», суммируя оценки иммуногенности по мутациям и накладывая информацию о том, каким субклональным популяциям они принадлежат и насколько распространены эти популяции. Это даёт показатели на уровне опухоли, которые выделяют раки, богатые сильными, широко распространёнными неоантигенами — особенно теми, которые могут быть представлены как на MHC класса I, так и на MHC класса II и потенциально вызвать скоординированные ответы вспомогательных и киллерных Т‑клеток. В группах пациентов с меланомой и немелкоклеточным раком лёгкого, леченных ингибиторами контрольных точек, показатели на основе NeoPrecis точнее разделяли отвечающих и неотвечающих по сравнению со стандартными подсчётами мутаций, и были особенно полезны при сложных, гетерогенных опухолях лёгкого.
Что это значит для пациентов
Для пациентов перспектива NeoPrecis — более точное подбор иммунотерапии тем, кто наименее вероятно получит выгоду, и лучшее понимание причин, по которым некоторые опухоли устойчивы к лечению. Сосредоточившись на качестве и распределении неоантигенов, а не только на их количестве, эта методика помогает объяснить, почему опухоли с похожей мутационной нагрузкой могут вести себя очень по‑разному. В будущем такие детальные карты иммунно‑видимого ландшафта опухоли могут направлять не только использование ингибиторов контрольных точек, но и разработку персонализированных раковых вакцин, которые приоритизируют наиболее мощные и широко распространённые мишени в каждой конкретной опухоли пациента.
Цитирование: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Ключевые слова: иммунотерапия рака, неоантигены, гетерогенность опухоли, ингибиторы контрольных точек, вычислительная онкология