Clear Sky Science · ru
Stenotrophomonas способствует прогрессированию опухолей желудочно-кишечного тракта через деградацию STING в опухолевых клетках и ослабление иммунного ответа
Скрытые микробы внутри опухолей
Большинство людей знают, что микробы в кишечнике влияют на пищеварение и даже на настроение, но немногие подозревают, что живые бактерии могут фактически обитать внутри самих раковых клеток. Это исследование показывает, как обычная встречающаяся в окружающей среде бактерия Stenotrophomonas прячется внутри опухолей желудочно-кишечного тракта и тихо способствует их росту, одновременно притупляя иммунную защиту организма и снижая эффективность современных онкоиммунотерапий.
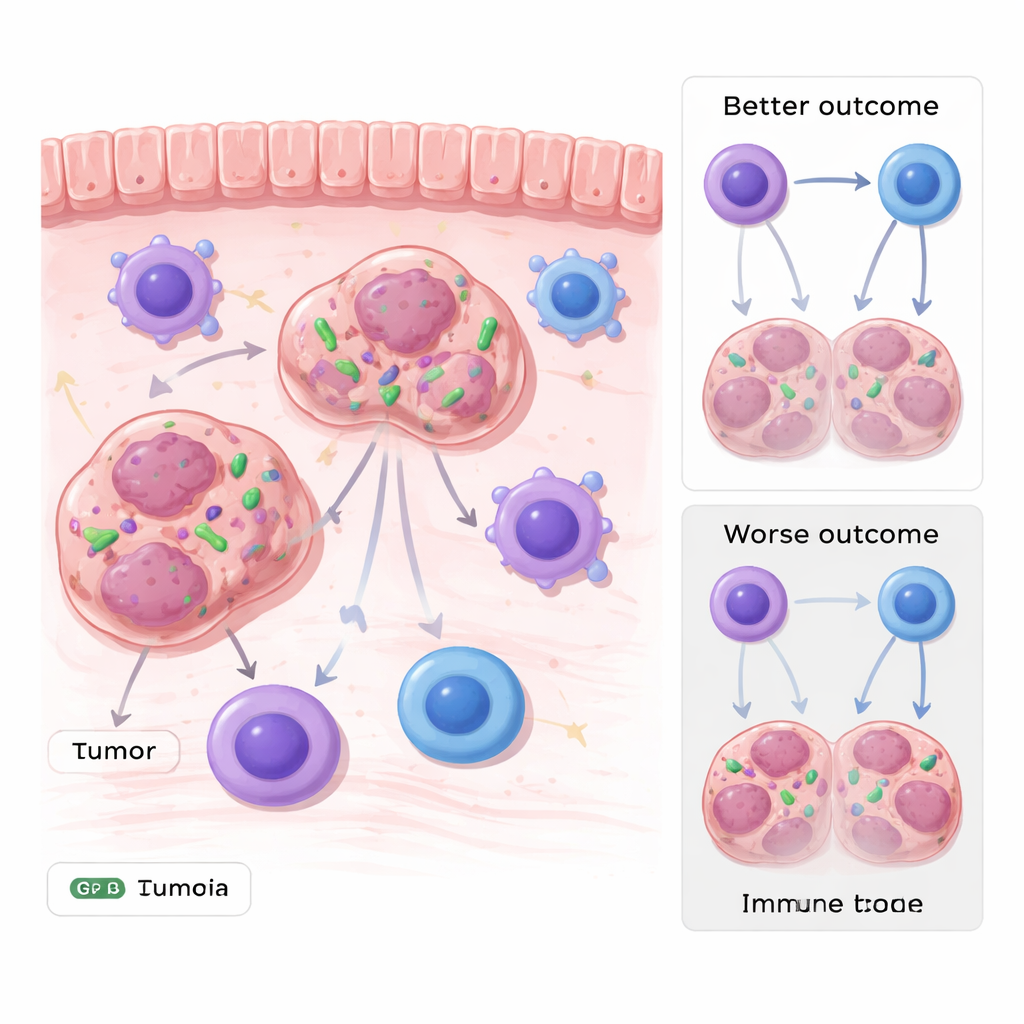
Бактерии, живущие в раковых клетках
Опухоли желудочно-кишечного тракта, такие как рак желудка и колоректальный рак, развиваются в постоянном контакте с богатыми бактериальными сообществами пищеварительного тракта. Проанализировав несколько генетических наборов данных от пациентов и затем подтвердив результаты в образцах опухолей, исследователи обнаружили, что ДНК Stenotrophomonas была необычно обильна в нескольких типах опухолей ЖКТ. Важно, что её присутствие было не просто поверхностным загрязнением: методы визуализации, включая флуоресцентные зонды и электронную микроскопию, выявили целые бактерии в цитоплазме опухолевых клеток. Пациенты с более высоким содержанием этой бактерии в опухоли имели, как правило, худший прогноз, что связывает микроорганизм с неблагоприятным исходом.
Как микроб смещает иммунный баланс
Далее команда задалась вопросом, совпадают ли эти скрытые бактерии с агрессивными опухолями случайно или они активно способствуют заболеванию. На мышиных моделях они инфицировали опухолевые клетки флуоресцентно меченой Stenotrophomonas перед имплантацией в животных. Опухоли, содержащие бактерию, росли быстрее и становились крупнее, чем без неё, в нескольких типах раковых клеток. При изучении окружающего иммунного ландшафта выяснилось, что общее число иммунных клеток, включая Т‑лимфоциты и макрофаги, было схожим. Критическое различие заключалось в специализированном подмножестве макрофагов, экспрессирующих молекулу MHC‑II, которая помогает представлять фрагменты опухоли киллерам‑Т. В опухолях с Stenotrophomonas число MHC‑II‑положительных макрофагов заметно снижалось, а Т‑клетки проявляли более слабую противоопухолевую активность.
Короткое замыкание системы клеточной тревоги
Чтобы понять механизм, исследователи сосредоточились на ключевом пути сигнализации внутри клетки, известном как STING, который обычно распознаёт чужеродную ДНК и вызывает выброс антивирусных «сигналов тревоги» — интерферонов типа I. В лабораторных экспериментах опухолевые клетки, инфицированные Stenotrophomonas, вырабатывали значительно меньше интерферона бета, а гены, обычно активируемые этим путем, были подавлены. В работе показано, что бактерия индуцирует стресс в белково‑свёрточной сети клетки — эндоплазматическом ретикулуме — и затем захватывает маршрут контроля качества, называемый ER‑ассоциированной деградацией. Через белковый помощник SEL1L этот путь помечает белок STING для уничтожения в протеасомном «шреддере» клетки. При истощении уровней STING опухолевая клетка посылает более слабый сигнал тревоги, что ведёт к снижению производства интерферонов и, далее, к ослаблению активации MHC‑II‑положительных макрофагов.
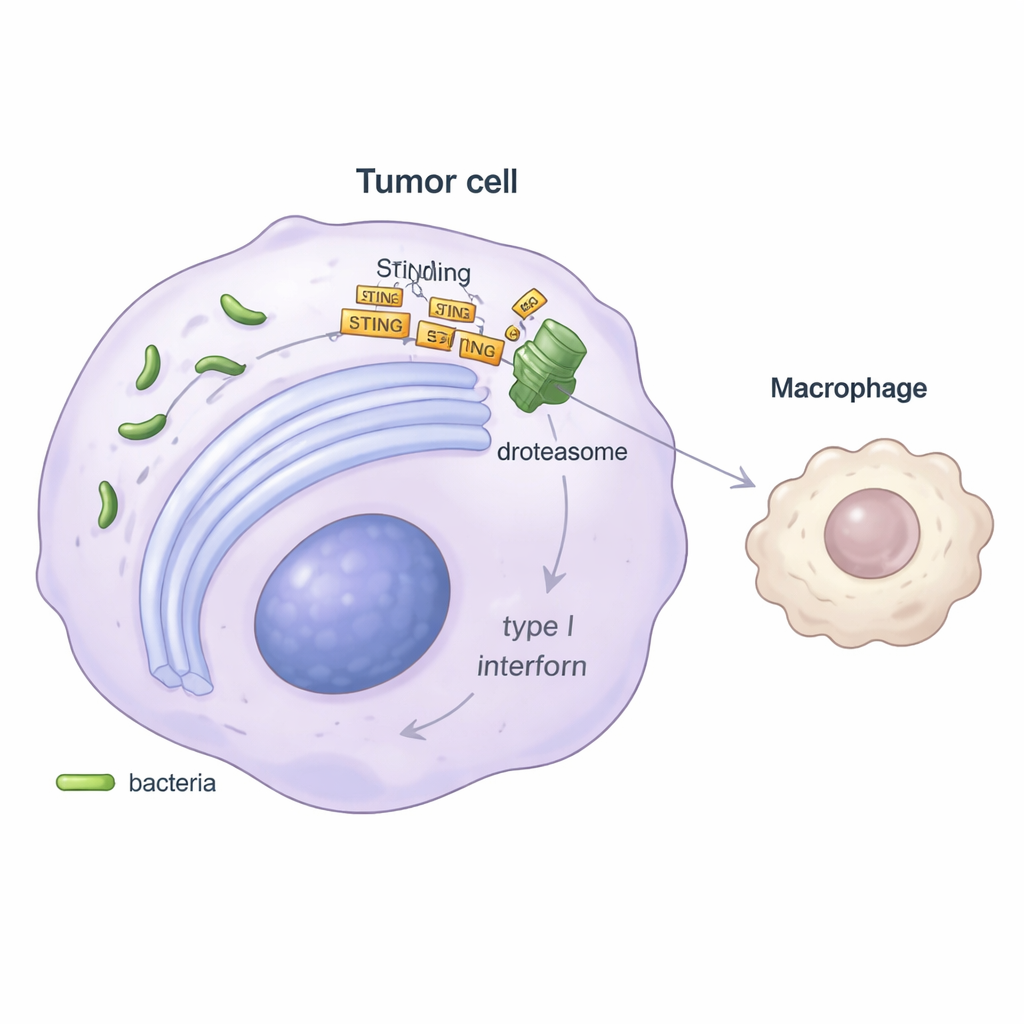
Подрыв иммунотерапии — и возможное решение
Поскольку современные иммунотерапии, такие как анти‑PD‑1, опираются на энергичные ответы Т‑клеток, команда проверила, как внутриклеточная Stenotrophomonas влияет на лечение. У мышей опухоли с бактерией хуже отвечали на анти‑PD‑1 по сравнению с бактериями‑свободными опухолями, даже в сочетании с химиотерапией. Т‑клетки в этих опухолях демонстрировали сниженные маркёры активности и деления, что согласуется с плохой иммунной стимуляцией. Поразительно, что при лечении животных антибиотиком левофлоксацином, который эффективно убивает Stenotrophomonas, рост опухолей замедлялся, а чувствительность к анти‑PD‑1 улучшалась. Восстановление сигнальной передачи интерферонов с помощью клинического препарата интерферона также могло вернуть популяцию полезных MHC‑II‑положительных макрофагов и возродить Т‑клеточное цитотоксическое действие в некоторых случаях, подчёркивая центральную роль этого пути.
Что это значит для пациентов
Для непрофессионального читателя ключевая мысль такова: некоторые раки желудочно‑кишечного тракта могут иметь «собственный» внутренний микробиом, который помогает им уклоняться от иммунной атаки. Stenotrophomonas, разрушая систему тревоги STING внутри опухолевых клеток, притупляет иммунные сигналы, которые в норме мобилизуют макрофагов и киллер‑Т‑клетки. Это не только ускоряет рост опухоли, но и может объяснять, почему некоторые пациенты не получают выгоды от мощных иммунотерапий. Хотя для изменения клинической практики требуется больше исследований, полученные данные позволяют предположить, что тестирование опухолей на наличие таких бактерий — и прицельное их лечение антибиотиками или препаратами, стабилизирующими STING — однажды может улучшить исход у больных раком желудка и колоректальным раком.
Цитирование: Feng, H., Chen, K., Xi, Z. et al. Stenotrophomonas promotes gastrointestinal tumor progression via STING degradation in tumour cells and mitigated immune response. Nat Commun 17, 2042 (2026). https://doi.org/10.1038/s41467-026-68649-0
Ключевые слова: опухолевый микробиом, рак желудочно-кишечного тракта, Stenotrophomonas, путь STING, онкоиммунотерапия